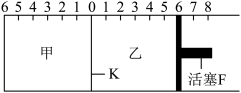
(1)如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入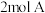 和
和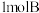 ,乙中充入
,乙中充入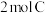 和
和 ,此时K停在0处。在一定条件下发生可逆反应:
,此时K停在0处。在一定条件下发生可逆反应: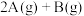

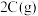 ;反应达到平衡后,再恢复至原温度。
;反应达到平衡后,再恢复至原温度。
回答下列问题:
①可根据________ 现象来判断甲、乙中反应都已达到平衡。
②达到平衡时,隔板K最终停留在0刻度左侧a处,则a的取值范围是_________ 。
(2)若一开始就将K、F固定,其它条件均同(1),则达到平衡时:
①甲、乙中C的物质的量的关系是甲__________ 乙(填“>”、“<”或“=” )。
②如果测得甲中A的转化率为b,则乙中C的转化率为____________ 。
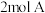 和
和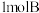 ,乙中充入
,乙中充入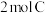 和
和 ,此时K停在0处。在一定条件下发生可逆反应:
,此时K停在0处。在一定条件下发生可逆反应: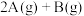

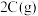 ;反应达到平衡后,再恢复至原温度。
;反应达到平衡后,再恢复至原温度。
回答下列问题:
①可根据
②达到平衡时,隔板K最终停留在0刻度左侧a处,则a的取值范围是
(2)若一开始就将K、F固定,其它条件均同(1),则达到平衡时:
①甲、乙中C的物质的量的关系是甲
②如果测得甲中A的转化率为b,则乙中C的转化率为
更新时间:2019-12-15 12:07:43
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】可逆反应3A(g) 3B(?)+C(?) △H>0达到化学平衡后,
3B(?)+C(?) △H>0达到化学平衡后,
(1)升高温度,用“变大”、“变小”、“不变”或“无法确定”填空。
a.若B、C都是气体,气体的平均相对分子质量①___ ;
b.若B、C都不是气体,气体的平均相对分子质量②____ ;
c.若B是气体,C不是气体,气体的平均相对分子质量③___ ;
(2)如果平衡后保持温度不变,将容器体积增加一倍,新平衡时A的浓度是原来的60%,则B是④___ 态,C是⑤___ 态。
 3B(?)+C(?) △H>0达到化学平衡后,
3B(?)+C(?) △H>0达到化学平衡后,(1)升高温度,用“变大”、“变小”、“不变”或“无法确定”填空。
a.若B、C都是气体,气体的平均相对分子质量①
b.若B、C都不是气体,气体的平均相对分子质量②
c.若B是气体,C不是气体,气体的平均相对分子质量③
(2)如果平衡后保持温度不变,将容器体积增加一倍,新平衡时A的浓度是原来的60%,则B是④
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
已知在400 ℃时,N2(g)+3H2(g) 2NH3(g)的K=0.5。
2NH3(g)的K=0.5。
①在400 ℃时,2NH3(g) N2(g)+3H2(g)的K′=
N2(g)+3H2(g)的K′=________ (填数值)。
②400 ℃时,在0.5 L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2 mol、1 mol、2 mol,则此时反应υ(N2)正________ υ(N2)逆(填“>”、“<”“=”或“不能确定”)。
③若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡________ (填“向左”、“向右”或“不”)移动;使用催化剂________ (填“增大”、“减小”或“不改变”)反应的ΔH。
已知在400 ℃时,N2(g)+3H2(g)
 2NH3(g)的K=0.5。
2NH3(g)的K=0.5。①在400 ℃时,2NH3(g)
 N2(g)+3H2(g)的K′=
N2(g)+3H2(g)的K′=②400 ℃时,在0.5 L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2 mol、1 mol、2 mol,则此时反应υ(N2)正
③若在恒温、恒压条件下向平衡体系中通入氩气,则合成氨反应的平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】对于以下三个反应,从反应开始进行到达到平衡后,保持温度、体积不变,按要求回答下列问题。
(1)PCl5(g) PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
再充入PCl5(g),平衡向____ 方向移动,达到平衡后,PCl5(g)的转化率____ ,PCl5(g)的百分含量____ 。
(2)2HI(g) I2(g)+H2(g)
I2(g)+H2(g)
再充入HI(g),平衡向____ 方向移动,达到平衡后,HI的分解率____ ,HI的百分含量____ 。
(3)2NO2(g) N2O4(g)
N2O4(g)
再充入NO2(g),平衡向____ 方向移动,达到平衡后,NO2(g)的转化率____ ,NO2(g)的百分含量____ 。
(1)PCl5(g)
 PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)再充入PCl5(g),平衡向
(2)2HI(g)
 I2(g)+H2(g)
I2(g)+H2(g)再充入HI(g),平衡向
(3)2NO2(g)
 N2O4(g)
N2O4(g)再充入NO2(g),平衡向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】合成氨是人类科学技术上的一项重大突破,反应原理为N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:
2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:

(1)①步骤Ⅱ中制氢气的原理如下:
a.CH4(g)+H2O(g) CO(g)+3H2(g);K1
CO(g)+3H2(g);K1
b.CO(g)+H2O(g) CO2(g)+H2(g);K2
CO2(g)+H2(g);K2
则反应CH4(g)+2H2O(g) CO2(g)+4H2(g);K=
CO2(g)+4H2(g);K=_______________ (用含K1、K2的代数式表示)。
②T1温度时,对于反应:CO(g)+ H2O(g) CO2(g)+ H2(g),向2 L的恒容密闭容器中通入一定量的CO和H2O(g)。若达到平衡后,反应放热Q kJ,保持其他条件不变,只是向原平衡体系中再通入0.20 mol H2O(g),则下列说法正确的是
CO2(g)+ H2(g),向2 L的恒容密闭容器中通入一定量的CO和H2O(g)。若达到平衡后,反应放热Q kJ,保持其他条件不变,只是向原平衡体系中再通入0.20 mol H2O(g),则下列说法正确的是_____________ 。
A.CO的转化率将增大 B.达到新平衡时的反应热ΔH > —Q
C.气体的密度将不变 D.H2O的体积分数增大
(2)将3 molH2和2 molN2充入某恒温恒压容器中,发生合成氨的反应:3H2(g) +N2(g) 2NH3(g)
2NH3(g)
①达平衡时NH3的浓度为c mol·L-1。保持温度不变,按下列配比分别充入该容器,平衡后NH3的浓度不为c mol·L-1的是_________ 。
A.6mol H2 + 4mol N2
B.0.75mol H2 + 0.75mol N2 + 0.5mol NH3
C.3mol H2+ 1mol N2 + 2mol NH3
② 若是在恒温恒容的容器中反应,达到平衡时NH3的浓度为c1 mol·L-1,则c________ c1(填“<”“>”或“=”),原因是________________________________________ 。
 2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:
2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:
(1)①步骤Ⅱ中制氢气的原理如下:
a.CH4(g)+H2O(g)
 CO(g)+3H2(g);K1
CO(g)+3H2(g);K1b.CO(g)+H2O(g)
 CO2(g)+H2(g);K2
CO2(g)+H2(g);K2则反应CH4(g)+2H2O(g)
 CO2(g)+4H2(g);K=
CO2(g)+4H2(g);K=②T1温度时,对于反应:CO(g)+ H2O(g)
 CO2(g)+ H2(g),向2 L的恒容密闭容器中通入一定量的CO和H2O(g)。若达到平衡后,反应放热Q kJ,保持其他条件不变,只是向原平衡体系中再通入0.20 mol H2O(g),则下列说法正确的是
CO2(g)+ H2(g),向2 L的恒容密闭容器中通入一定量的CO和H2O(g)。若达到平衡后,反应放热Q kJ,保持其他条件不变,只是向原平衡体系中再通入0.20 mol H2O(g),则下列说法正确的是A.CO的转化率将增大 B.达到新平衡时的反应热ΔH > —Q
C.气体的密度将不变 D.H2O的体积分数增大
(2)将3 molH2和2 molN2充入某恒温恒压容器中,发生合成氨的反应:3H2(g) +N2(g)
 2NH3(g)
2NH3(g)①达平衡时NH3的浓度为c mol·L-1。保持温度不变,按下列配比分别充入该容器,平衡后NH3的浓度不为c mol·L-1的是
A.6mol H2 + 4mol N2
B.0.75mol H2 + 0.75mol N2 + 0.5mol NH3
C.3mol H2+ 1mol N2 + 2mol NH3
② 若是在恒温恒容的容器中反应,达到平衡时NH3的浓度为c1 mol·L-1,则c
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(Ⅰ)如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处。在一定条件下发生可逆反应:2A(g)+B(g) 2C(g); 反应达到平衡后,再恢复至原温度。回答下列问题:
2C(g); 反应达到平衡后,再恢复至原温度。回答下列问题:
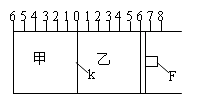
(1)可根据__________ 现象来判断甲、乙都已达到平衡。
(2)达到平衡时,隔板K最终停留在0刻度左侧a处,则a的取值范围是____________ 。
(3)若达到平衡时,隔板K最终停留在左侧刻度1处,则甲中C的物质的量为_____ mol,乙中C的转化率________ 50%(填:>、<、=),此时,乙中可移动活塞F最终停留在右侧刻度________ 处(填下列序号:① <6 ② >6 ③ =6)
(Ⅱ)若一开始就将K、F固定,其它条件均不变,则达到平衡时:
(1)测得甲中A的转化率为b,则乙中C的转化率为_________ ;
(2)假设乙、甲两容器中的压强比用d表示,则d的取值范围是_______________ 。
 2C(g); 反应达到平衡后,再恢复至原温度。回答下列问题:
2C(g); 反应达到平衡后,再恢复至原温度。回答下列问题:
(1)可根据
(2)达到平衡时,隔板K最终停留在0刻度左侧a处,则a的取值范围是
(3)若达到平衡时,隔板K最终停留在左侧刻度1处,则甲中C的物质的量为
(Ⅱ)若一开始就将K、F固定,其它条件均不变,则达到平衡时:
(1)测得甲中A的转化率为b,则乙中C的转化率为
(2)假设乙、甲两容器中的压强比用d表示,则d的取值范围是
您最近一年使用:0次
【推荐3】T℃时,将3molA和2molB气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A(气)+B(气)  xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为O.4mol/L,请填写下列空白:
xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为O.4mol/L,请填写下列空白:
(1)反应达到平衡时,A、B两反应物的转化率之比为α(A):α(B)=___________ 。
(2)若继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,下列说法中正确的是__ (填写字母序号)。
A.化学平衡向正反应方向移动 B.化学平衡向逆反应方向移动
C.化学平衡不会发生移动 D.正、逆反应的化学反应速率保持不变
(3)在T℃时,若向原平衡混合物的容器中再充入amolC,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则至少应再充入__________ (填A或B)________ mol(用a表示)。
 xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为O.4mol/L,请填写下列空白:
xC(气),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为O.4mol/L,请填写下列空白:(1)反应达到平衡时,A、B两反应物的转化率之比为α(A):α(B)=
(2)若继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,下列说法中正确的是
A.化学平衡向正反应方向移动 B.化学平衡向逆反应方向移动
C.化学平衡不会发生移动 D.正、逆反应的化学反应速率保持不变
(3)在T℃时,若向原平衡混合物的容器中再充入amolC,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则至少应再充入
您最近一年使用:0次



