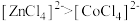T℃时,发生可逆反应A(s)+2B(g) 2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 molC和2 molD加入乙容器中。起始时,两容器中的压强相等,t1时两容器内均达到平衡状态(如图所示,隔板K固定不动)。下列说法正确的是
2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 molC和2 molD加入乙容器中。起始时,两容器中的压强相等,t1时两容器内均达到平衡状态(如图所示,隔板K固定不动)。下列说法正确的是
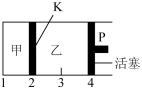
 2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 molC和2 molD加入乙容器中。起始时,两容器中的压强相等,t1时两容器内均达到平衡状态(如图所示,隔板K固定不动)。下列说法正确的是
2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 molC和2 molD加入乙容器中。起始时,两容器中的压强相等,t1时两容器内均达到平衡状态(如图所示,隔板K固定不动)。下列说法正确的是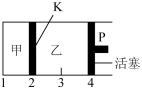
| A.向甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度与乙中C的浓度相等 |
| B.t1时,甲、乙两容器中的压强仍相等 |
| C.移动活塞P,使乙的容积和甲的相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
| D.分别向甲、乙中加入等量的氦气,甲中反应速率和乙中的反应速率均不变 |
更新时间:2019/12/25 10:01:39
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】在一密闭容器中,物质 发生三个脱水的竞争反应:①
发生三个脱水的竞争反应:①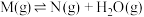

②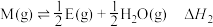 ③
③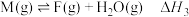 反应历程如图所示。相同条件下,下列说法正确的是
反应历程如图所示。相同条件下,下列说法正确的是
 发生三个脱水的竞争反应:①
发生三个脱水的竞争反应:①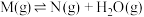

②
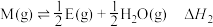 ③
③ 反应历程如图所示。相同条件下,下列说法正确的是
反应历程如图所示。相同条件下,下列说法正确的是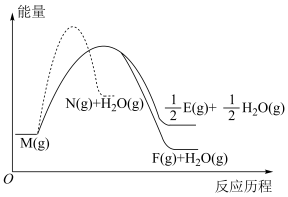
| A.由图可知,物质M比物质N稳定 |
| B.反应①比反应②和③更快达到化学平衡 |
C.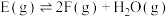 的反应热 的反应热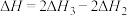 |
| D.平衡后压缩容器,物质E的物质的量不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】为减少碳的排放,科学家提出利用CO2和H2反应合成甲醇,其反应原理为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。下列有关说法不正确的是
CH3OH(g)+H2O(g)。下列有关说法不正确的是
 CH3OH(g)+H2O(g)。下列有关说法不正确的是
CH3OH(g)+H2O(g)。下列有关说法不正确的是| A.恒温恒容下,该反应达到平衡时,各物质的物质的量分别为1mol、3mol、1mol和1mol,若此时各物质的物质的量分别增加1mol,平衡正向移动。 |
| B.恒温恒压下,该反应达到平衡时,各物质的物质的量分别为1mol、1mol、1mol和1mol,若此时通入12molCO2,平衡正向移动 |
| C.恒温恒容下,先向容器中加入1molCO2,再慢慢通入H2,发生反应,CH3OH的平衡物质的量逐渐增加 |
| D.恒温恒容下,先向容器中加入1molCO2,再慢慢通入H2,发生反应,CH3OH的平衡体积分数先增大后减小 |
您最近一年使用:0次
单选题-单题
|
较难
(0.4)
名校
【推荐1】采用 与
与 反应合成可再生能源甲醇,反应如下:
反应合成可再生能源甲醇,反应如下: ,在一个容积可变的密闭容器中充有
,在一个容积可变的密闭容器中充有 和
和 ,在催化剂作用下发生反应。
,在催化剂作用下发生反应。 的平衡转化率
的平衡转化率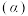 与温度
与温度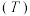 ,压强
,压强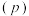 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 与
与 反应合成可再生能源甲醇,反应如下:
反应合成可再生能源甲醇,反应如下: ,在一个容积可变的密闭容器中充有
,在一个容积可变的密闭容器中充有 和
和 ,在催化剂作用下发生反应。
,在催化剂作用下发生反应。 的平衡转化率
的平衡转化率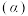 与温度
与温度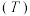 ,压强
,压强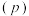 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
A. 点的正反应速率大于 点的正反应速率大于 点的逆反应速率 点的逆反应速率 |
B.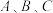 三点的平衡常数 三点的平衡常数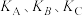 的大小关系为: 的大小关系为: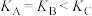 |
C.若达到平衡状态 时,容器的体积为 时,容器的体积为 ,则在平衡状态 ,则在平衡状态 时容器的体积为 时容器的体积为 |
D. 点时,若再充入 点时,若再充入 的 的 ,再次平衡时 ,再次平衡时 转化率 转化率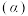 减小 减小 |
您最近一年使用:0次
【推荐2】汽车排气系统中的三元催化剂能将尾气中的 与
与 转化为无污染气体,反应为
转化为无污染气体,反应为 。
。 ,向
,向 恒容密闭容器中通入
恒容密闭容器中通入 和
和 ,一定条件下测得
,一定条件下测得 的物质的量随时间变化关系如表所示:
的物质的量随时间变化关系如表所示:
下列说法不正确的是
 与
与 转化为无污染气体,反应为
转化为无污染气体,反应为 。
。 ,向
,向 恒容密闭容器中通入
恒容密闭容器中通入 和
和 ,一定条件下测得
,一定条件下测得 的物质的量随时间变化关系如表所示:
的物质的量随时间变化关系如表所示: | 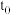 |  |  |  |  |
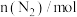 | 0 | 0.35 | 0.7 | 0.8 | 0.8 |
A. |
B.若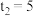 ,则 ,则 内 内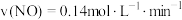 |
C.该温度下的化学平衡常数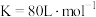 |
D.其他条件不变,若起始时通入 和 和 ,达平衡时 ,达平衡时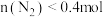 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
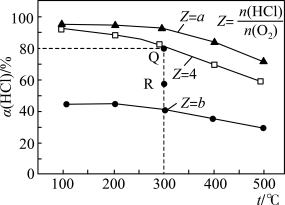
【推荐3】有Ⅰ~Ⅳ四个体积均为 0.5 L 的恒容密闭容器,在Ⅰ、Ⅱ、Ⅲ中按不同投料比(Z)充入 HCl 和 O2(如下表),加入催化剂发生反应 4HCl(g)+O2(g)  2Cl2(g)+2H2O(g) ΔH,HCl 的平衡转化率(α)与 Z 和温度(T)的关系如图 所示。下列说法正确的是
2Cl2(g)+2H2O(g) ΔH,HCl 的平衡转化率(α)与 Z 和温度(T)的关系如图 所示。下列说法正确的是
 2Cl2(g)+2H2O(g) ΔH,HCl 的平衡转化率(α)与 Z 和温度(T)的关系如图 所示。下列说法正确的是
2Cl2(g)+2H2O(g) ΔH,HCl 的平衡转化率(α)与 Z 和温度(T)的关系如图 所示。下列说法正确的是| 容器 | 起始时 | ||
| t/℃ | n(HCl)·mol-1 | Z | |
| I | 300 | 0.25 | a |
| II | 300 | 0.25 | b |
| III | 300 | 0.25 | 4 |

| A.ΔH<0,b<4<a |
| B.300 ℃该反应的平衡常数的值为 64 |
| C.容器Ⅲ某时刻处在 R 点,则 R 点的 v 正>v 逆,压强:p(R)>p(Q) |
| D.若起始时,在容器Ⅳ中充入 0.25 mol Cl2和 0.25 mol H2O(g),300 ℃达平衡时容器中 c(HCl)=0.1 mol·L-1 |
您最近一年使用:0次
【推荐1】在容积为500mL的真空密闭容器中充入0.009molHI,保持448℃恒温条件下发生反应: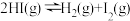
 ,达到平衡时,测得
,达到平衡时,测得 。下列说法正确的是
。下列说法正确的是
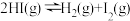
 ,达到平衡时,测得
,达到平衡时,测得 。下列说法正确的是
。下列说法正确的是| A.向容器内再充入一定量HI,平衡正向移动,达到新平衡时各组分百分含量和浓度均不变 |
| B.升高体系温度,正、逆反应速率均增大,平衡正向移动,但体系压强保持不变 |
C.保持恒温,压缩容器容积,气体颜色变深,说明平衡正向移动,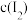 增大 增大 |
D.448℃时,反应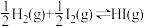 的平衡常数 的平衡常数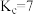 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】一定温度下,向体积为5L的密闭容器中充入0.5mol  和0.5mol
和0.5mol  ,发生反应:
,发生反应:

测得气体混合物中HI的物质的量分数X(HI)与反应时间t的关系如下表
下列说法正确的是
 和0.5mol
和0.5mol  ,发生反应:
,发生反应:

测得气体混合物中HI的物质的量分数X(HI)与反应时间t的关系如下表
| X(HI)/% | 0 | 50 | 68 | 76 | 80 | 80 |
| t/min | 0 | 20 | 40 | 60 | 80 | 100 |
A.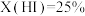 时, 时, |
| B.当容器内气体的密度不再变化时,反应到达平衡 |
C.0~20min的平均速率 |
D.该温度下反应的平衡常数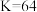 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】苯乙烯是生产各种塑料的重要单体,其制备原理C6H5—C2H5(g) C6H5CH=CH2(g)+H2(g),实际生产中常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),图为乙苯的平衡转化率与水蒸气的用量、体系总压强的关系。下列说法正确的是
C6H5CH=CH2(g)+H2(g),实际生产中常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),图为乙苯的平衡转化率与水蒸气的用量、体系总压强的关系。下列说法正确的是

 C6H5CH=CH2(g)+H2(g),实际生产中常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),图为乙苯的平衡转化率与水蒸气的用量、体系总压强的关系。下列说法正确的是
C6H5CH=CH2(g)+H2(g),实际生产中常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),图为乙苯的平衡转化率与水蒸气的用量、体系总压强的关系。下列说法正确的是
| A.b点和c点温度和压强相同,则反应速率相同 |
| B.恒容时加入稀释剂,C6H5—C2H5平衡转化率不变 |
| C.a点转化率为75%,则混合气体中苯乙烯的体积分数为1/3 |
| D.b点转化率为50%,若起始向2L恒容容器中充入1mol乙苯,则平衡常数为0.5mol·L-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
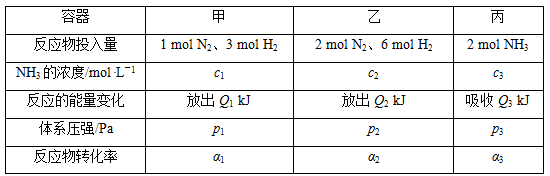
【推荐1】在温度相同、容积均为2 L的3个恒容密闭容器中,按不同方式投入反应物,保持恒温,测得反应达到平衡时的有关数据如下。下列说法正确的是( )
已知N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1
2NH3(g) ΔH=-92.4 kJ·mol-1
已知N2(g)+3H2(g)
 2NH3(g) ΔH=-92.4 kJ·mol-1
2NH3(g) ΔH=-92.4 kJ·mol-1
| A.2p1=2p3<p2 |
| B.达到平衡时丙容器中NH3的体积分数最大 |
| C.α2+α3<1 |
| D.Q1+Q3=92.4 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入物质,发生反应:PCl3(g)+Cl2(g) PCl5(g) ΔH<0,测得反应的相关数据如下:
PCl5(g) ΔH<0,测得反应的相关数据如下:
下列说法正确的是( )
 PCl5(g) ΔH<0,测得反应的相关数据如下:
PCl5(g) ΔH<0,测得反应的相关数据如下:| 容器1 | 容器2 | 容器3 | |
| 温度/℃ | 200 | 300 | 200 |
| 起始物质投入量 | 1molPCl3、2molCl2 | 2molPCl3、1molCl2 | 2molCl2、2molPCl5 |
| 平衡c(PCl5)/mol·L-1 | c1 | c2 | c3 |
| 化学平衡常数 | K1 | K2 | K3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
| 物质的转化率α | α1(PCl3) | α2(Cl2) | α3(PCl5) |
下列说法正确的是( )
| A.K1<K2 |
| B.c1<c2 |
| C.p3=2p1 |
| D.α1(PCl3)+α3(PCl5)<1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】相同温度下,体积均为1 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g) ΔH=-92.6 kJ·mol-1。测得数据如表:
2NH3(g) ΔH=-92.6 kJ·mol-1。测得数据如表:
下列叙述不正确的是
 2NH3(g) ΔH=-92.6 kJ·mol-1。测得数据如表:
2NH3(g) ΔH=-92.6 kJ·mol-1。测得数据如表:| 容器编号 | 起始时各物质的物质的量/mol | 达到平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| (1) | 2 | 3 | 0 | 27.78 kJ |
| (2) | 1.6 | 1.8 | 0.8 | Q |
| A.容器(1)(2)中反应达平衡时压强相等 |
| B.容器(2)中反应开始时v(正)>v(逆) |
| C.容器(2)中反应达平衡时,吸收的热量Q为9.26 kJ |
| D.容器(1)中反应达平衡时若移走1 mol N2和1.5 mol H2,再次达到新平衡时n(NH3)<0.3 mol |
您最近一年使用:0次

 呈粉红色,
呈粉红色, 呈蓝色,
呈蓝色,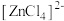 为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: ,用该溶液做实验,溶液的颜色变化如下:
,用该溶液做实验,溶液的颜色变化如下:
 中σ键数之比为3:2
中σ键数之比为3:2