大力发展电动汽车,可以有效控制空气污染.目前机动车常使用的电池有铅蓄电池、锂电池等.
Ⅰ 铅蓄电池充放电的总反应为:
铅蓄电池充放电的总反应为:

 ,锂硫电池充放电的总反应为:
,锂硫电池充放电的总反应为:

 .
.
 放电时,铅蓄电池的负极反应式为
放电时,铅蓄电池的负极反应式为 ______ .
 锂硫电池工作时,电子经外电路流向
锂硫电池工作时,电子经外电路流向 ______  填“正极”或“负极”
填“正极”或“负极” .
.
 当消耗相同质量的负极活性物质时,锂硫电池的理论放电量是铅蓄电池的
当消耗相同质量的负极活性物质时,锂硫电池的理论放电量是铅蓄电池的 ______ 倍.
Ⅱ 由方铅矿
由方铅矿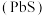 制备铅蓄电池电极材料
制备铅蓄电池电极材料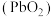 的方法如下:
的方法如下:

 油画所用的白色颜料
油画所用的白色颜料 置于空气中,遇
置于空气中,遇 气体变成黑色PbS,从而使油画的色彩变暗,用
气体变成黑色PbS,从而使油画的色彩变暗,用 清洗,可使油画“复原”.
清洗,可使油画“复原”.
 的作用是
的作用是 ______ .
 已知硫化铅溶于水时存在溶解平衡:
已知硫化铅溶于水时存在溶解平衡: ,试分析
,试分析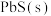 能溶于稀
能溶于稀 的原因
的原因 ______ .
 滤液X是一种可循环使用的物质,其溶质主要是
滤液X是一种可循环使用的物质,其溶质主要是 ____  填化学式
填化学式 ,若X中残留的
,若X中残留的 过多,循环使用时可能出现的问题是
过多,循环使用时可能出现的问题是 ____ .
 与次氯酸钠溶液反应可制得
与次氯酸钠溶液反应可制得 ,写出该反应的离子方程式
,写出该反应的离子方程式 ______ .
 以石墨为电极,电解
以石墨为电极,电解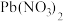 溶液也可以制得
溶液也可以制得 ,则阳极的电极反应式为
,则阳极的电极反应式为 ______ ;电解时为提高Pb元素的利用率,常在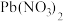 溶液中加入适量
溶液中加入适量 ,理由是
,理由是 ______ .
Ⅰ
 铅蓄电池充放电的总反应为:
铅蓄电池充放电的总反应为:

 ,锂硫电池充放电的总反应为:
,锂硫电池充放电的总反应为:

 .
. 放电时,铅蓄电池的负极反应式为
放电时,铅蓄电池的负极反应式为  锂硫电池工作时,电子经外电路流向
锂硫电池工作时,电子经外电路流向  填“正极”或“负极”
填“正极”或“负极” .
. 当消耗相同质量的负极活性物质时,锂硫电池的理论放电量是铅蓄电池的
当消耗相同质量的负极活性物质时,锂硫电池的理论放电量是铅蓄电池的 Ⅱ
 由方铅矿
由方铅矿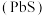 制备铅蓄电池电极材料
制备铅蓄电池电极材料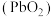 的方法如下:
的方法如下:
 油画所用的白色颜料
油画所用的白色颜料 置于空气中,遇
置于空气中,遇 气体变成黑色PbS,从而使油画的色彩变暗,用
气体变成黑色PbS,从而使油画的色彩变暗,用 清洗,可使油画“复原”.
清洗,可使油画“复原”. 的作用是
的作用是  已知硫化铅溶于水时存在溶解平衡:
已知硫化铅溶于水时存在溶解平衡: ,试分析
,试分析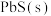 能溶于稀
能溶于稀 的原因
的原因  滤液X是一种可循环使用的物质,其溶质主要是
滤液X是一种可循环使用的物质,其溶质主要是  填化学式
填化学式 ,若X中残留的
,若X中残留的 过多,循环使用时可能出现的问题是
过多,循环使用时可能出现的问题是  与次氯酸钠溶液反应可制得
与次氯酸钠溶液反应可制得 ,写出该反应的离子方程式
,写出该反应的离子方程式  以石墨为电极,电解
以石墨为电极,电解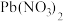 溶液也可以制得
溶液也可以制得 ,则阳极的电极反应式为
,则阳极的电极反应式为 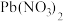 溶液中加入适量
溶液中加入适量 ,理由是
,理由是
更新时间:2020-01-10 08:28:17
|
相似题推荐
【推荐1】某冶炼厂采用萃取法回收镓锗铜后的废渣中含有Zn(II)、Fe(II)、Al(III)、Mn(II)、Cd(II)、As(V)的硫酸盐及氧化物。现欲利用废渣采用以下工艺流程制备工业活性氧化锌和无水硫酸钠。

该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)酸浸氧化
①“酸浸氧化”时温度对金属离子沉淀率的影响如下图,由图可知“酸浸氧化”的最佳温度为______ 。

②“酸浸氧化”中Fe2+和Mn2+均被Na2S2O8氧化,其中Mn2+被氧化后生成难溶于水的黑色沉淀。写出Mn2+被氧化的离子方程式________________ 。
(2)“中和沉淀”前后溶液中相关元素的含量(g/L)如下表所示:
①“中和沉淀”中随滤渣除去的元素除Al外,还有_________ (填元素符号)。
②“中和沉淀”后滤液②的pH=4.0,由此估算氢氧化铝的溶度积常数为_______ (保留两位有效数字)。
(3)“除镉”中加入的试剂X与溶液中的镉离子发生置换反应,则滤渣③的主要成分为_______ 。
(4)若碱式碳酸锌的化学式为ZnCO3•2Zn(OH)2•H2O,写出“沉锌”反应的化学方程式是:_______ 。

该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ | Zn2+ | Cd2+ |
| 开始沉淀pH | 1.9 | 7.0 | 3.0 | 8.1 | 6.4 | 7.5 |
| 完全沉淀pH | 3.2 | 9.0 | 4.7 | 10.1 | 8.0 | 9.7 |
(1)酸浸氧化
①“酸浸氧化”时温度对金属离子沉淀率的影响如下图,由图可知“酸浸氧化”的最佳温度为

②“酸浸氧化”中Fe2+和Mn2+均被Na2S2O8氧化,其中Mn2+被氧化后生成难溶于水的黑色沉淀。写出Mn2+被氧化的离子方程式
(2)“中和沉淀”前后溶液中相关元素的含量(g/L)如下表所示:
| Zn | As | Fe | Al | Cd | |
| 中和前 | 45 | 0.35 | 0.8 | 3.1 | 4 |
| 中和后 | 43 | 0.12 | 0.08 | 0.1 | 3.9 |
②“中和沉淀”后滤液②的pH=4.0,由此估算氢氧化铝的溶度积常数为
(3)“除镉”中加入的试剂X与溶液中的镉离子发生置换反应,则滤渣③的主要成分为
(4)若碱式碳酸锌的化学式为ZnCO3•2Zn(OH)2•H2O,写出“沉锌”反应的化学方程式是:
您最近一年使用:0次
【推荐2】电子工业中,常用氯化铁溶液作为印刷电路铜板蚀刻液。请按要求回答下列问题:
(1)常温下,若向氯化铁溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该反应的离子方程式为______ ,该过程中调节溶液的pH为5,则 为
为______  。(已知:
。(已知: )
)
(2)某探究小组设计如下线路处理 溶液蚀刻铜板后的废液和资源回收:
溶液蚀刻铜板后的废液和资源回收:

①用足量 溶液蚀刻铜板后的废液中含有的金属阳离子有
溶液蚀刻铜板后的废液中含有的金属阳离子有______ 。
② 蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是
蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是______ 。
③步骤①中加入 溶液的目的是
溶液的目的是______ 。
④已知:生成氢氧化物沉淀的pH
根据表中数据推测调节pH的范围是______ 。
⑤步骤②通常加入 来调节pH,写出步骤②的离子方程式
来调节pH,写出步骤②的离子方程式______ 。
(1)常温下,若向氯化铁溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该反应的离子方程式为
 为
为 。(已知:
。(已知: )
)(2)某探究小组设计如下线路处理
 溶液蚀刻铜板后的废液和资源回收:
溶液蚀刻铜板后的废液和资源回收:
①用足量
 溶液蚀刻铜板后的废液中含有的金属阳离子有
溶液蚀刻铜板后的废液中含有的金属阳离子有②
 蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是
蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是③步骤①中加入
 溶液的目的是
溶液的目的是④已知:生成氢氧化物沉淀的pH
 |  |  | |
| 开始沉淀时 | 4.7 | 7.0 | 1.9 |
| 沉淀完全时 | 6.7 | 9.0 | 3.2 |
⑤步骤②通常加入
 来调节pH,写出步骤②的离子方程式
来调节pH,写出步骤②的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】铁、铜及其化合物在日常生活及工业生产中有着非常广泛的用途。请回答下列问题:
i.FeCl3是常用的金属蚀刻剂和净水剂。
(1)FeCl3净水的原理是___________ (用离子方程式表示)。
(2)配制FeCl3溶液时,某同学误将FeCl3固体直接放入NaHCO3溶液中,看到红褐色沉淀和大量气泡,用离子方程式解释原因___________ 。
ii.CuCl2常用作电镀添加剂、催化剂等。难溶金属的氢氧化物在不同pH下的溶解度( )如下图。
)如下图。

(3)pH=3时溶液中铜元素的主要存在形式是___________ 。
(4)若要除去CuCl2溶液中的少量 ,应该控制溶液的pH为
,应该控制溶液的pH为___________ 。
A.<1 B.4左右 C.>6
(5)在 溶液中含有少量的
溶液中含有少量的 杂质,
杂质,___________ (填“能”或“不能”)通过调节溶液pH的方法来除去。
(6)已知一些难溶物的溶度积常数如下表:
某工业废水中含有 、
、 、
、 ,最适宜向此工业废水中加入过量的
,最适宜向此工业废水中加入过量的___________ 除去它们。(选填序号)
A.NaOH B.FeS C.Na2S
i.FeCl3是常用的金属蚀刻剂和净水剂。
(1)FeCl3净水的原理是
(2)配制FeCl3溶液时,某同学误将FeCl3固体直接放入NaHCO3溶液中,看到红褐色沉淀和大量气泡,用离子方程式解释原因
ii.CuCl2常用作电镀添加剂、催化剂等。难溶金属的氢氧化物在不同pH下的溶解度(
 )如下图。
)如下图。
(3)pH=3时溶液中铜元素的主要存在形式是
(4)若要除去CuCl2溶液中的少量
 ,应该控制溶液的pH为
,应该控制溶液的pH为A.<1 B.4左右 C.>6
(5)在
 溶液中含有少量的
溶液中含有少量的 杂质,
杂质,(6)已知一些难溶物的溶度积常数如下表:
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
 |  | 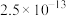 | 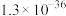 | 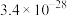 |  |  |
 、
、 、
、 ,最适宜向此工业废水中加入过量的
,最适宜向此工业废水中加入过量的A.NaOH B.FeS C.Na2S
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】某实验小组同学对电化学原理进行了一系列的探究实验活动。
(1)如下图为某实验小组依据氧化还原反应:(用离子方程式表示)___________ 。设计的原电池装置,反应前,电极质量相等,一段时间后,两电极相差12g,导线中通过___________ mol电子。
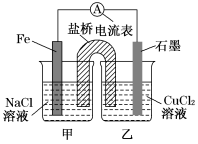
(2)其他条件不变,若将CuCl2溶液换为NaCl溶液,石墨电极为___________ (填写正、负、阴、阳),这时乙池溶液呈碱性,可向溶液中滴加酚酞指示剂,指示剂变红色。用吸管吸出铁片附近的溶液少许于试管中,向其中滴加少量的新制饱和氯水,写出发生的离子方程式___________ ,然后滴加几滴硫氰化钾溶液,溶液变红,继续滴加过量新制氯水,颜色褪去,同学们对些做了多种假设,某同学的假设是:“溶液中的+3价铁被氧化为更高价态”。如果+3价铁被氧化为FeO ,试写出该反应的离子方程式:
,试写出该反应的离子方程式:___________ 。
(3)如下图其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示。一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是___________ ,电极反应式___________ ;乙装置中石墨(1)为___________ 极(填写正、负、阴、阳),乙装置中与铜丝相连石墨电极上发生的反应式为___________ ,产物常用___________ 检验,反应的离子方程式___________ 。

(1)如下图为某实验小组依据氧化还原反应:(用离子方程式表示)

(2)其他条件不变,若将CuCl2溶液换为NaCl溶液,石墨电极为
 ,试写出该反应的离子方程式:
,试写出该反应的离子方程式:(3)如下图其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示。一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】当今,世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。
Ⅰ.105℃时,将足量的某碳酸氢盐(MHCO3)固体置于真空恒容容器中,存在如下平衡:2MHCO3(s) M2CO3(s)+H2O(g)+CO2(g)。上述反应达平衡时体系的总压为46kPa。
M2CO3(s)+H2O(g)+CO2(g)。上述反应达平衡时体系的总压为46kPa。
(1)保持温度不变,开始时在体系中先通入一定量的CO2(g),再加入足量M2CO3(s),欲使平衡时体系中水蒸气的分压小于5kPa,CO2(g)的初始压强应大于_______ kPa。
Ⅱ.以 和
和 为原料合成尿素
为原料合成尿素 是固定和利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
是固定和利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g) NH2COONH4(s) △H1=-159.47kJ/mol
NH2COONH4(s) △H1=-159.47kJ/mol
反应Ⅱ:NH2COONH4(s) CO(NH2)2(s)+H2O(g) △H2=+72.49kJ/mol
CO(NH2)2(s)+H2O(g) △H2=+72.49kJ/mol
请回答下列问题:
(2)写出 和
和 为原料生成尿素和气态水的热化学方程式
为原料生成尿素和气态水的热化学方程式___________ ,反应Ⅰ自发进行的条件是______ 。
(3)以 和
和 为原料合成尿素的反应中,影响
为原料合成尿素的反应中,影响 转化率的因素很多,图1为某特定条件下,不同水碳比
转化率的因素很多,图1为某特定条件下,不同水碳比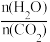 和温度影响
和温度影响 转化率变化的趋势曲线。下列说法错误的是______(填正确答案标号)。
转化率变化的趋势曲线。下列说法错误的是______(填正确答案标号)。

(4)某研究小组为探究反应Ⅰ中影响c( )的因素,在恒温下将0.4molNH3和0.2molCO2放入容积为2L的密闭容器中,t1时达到平衡,其c(
)的因素,在恒温下将0.4molNH3和0.2molCO2放入容积为2L的密闭容器中,t1时达到平衡,其c( )随时间t变化趋势曲线如下图2所示。则0~t1时段,用
)随时间t变化趋势曲线如下图2所示。则0~t1时段,用 表示的平均反应速率为
表示的平均反应速率为________ mol/(L·min)(用含t1的式子表示),该反应的平衡常数为______ (mol/L)3。

Ⅲ.电催化还原 受到广泛的研究,一种原理如图所示:
受到广泛的研究,一种原理如图所示:

(5)写出A电极发生的电极方程式:_________________ 。
Ⅰ.105℃时,将足量的某碳酸氢盐(MHCO3)固体置于真空恒容容器中,存在如下平衡:2MHCO3(s)
 M2CO3(s)+H2O(g)+CO2(g)。上述反应达平衡时体系的总压为46kPa。
M2CO3(s)+H2O(g)+CO2(g)。上述反应达平衡时体系的总压为46kPa。(1)保持温度不变,开始时在体系中先通入一定量的CO2(g),再加入足量M2CO3(s),欲使平衡时体系中水蒸气的分压小于5kPa,CO2(g)的初始压强应大于
Ⅱ.以
 和
和 为原料合成尿素
为原料合成尿素 是固定和利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
是固定和利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:反应Ⅰ:2NH3(g)+CO2(g)
 NH2COONH4(s) △H1=-159.47kJ/mol
NH2COONH4(s) △H1=-159.47kJ/mol反应Ⅱ:NH2COONH4(s)
 CO(NH2)2(s)+H2O(g) △H2=+72.49kJ/mol
CO(NH2)2(s)+H2O(g) △H2=+72.49kJ/mol请回答下列问题:
(2)写出
 和
和 为原料生成尿素和气态水的热化学方程式
为原料生成尿素和气态水的热化学方程式(3)以
 和
和 为原料合成尿素的反应中,影响
为原料合成尿素的反应中,影响 转化率的因素很多,图1为某特定条件下,不同水碳比
转化率的因素很多,图1为某特定条件下,不同水碳比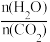 和温度影响
和温度影响 转化率变化的趋势曲线。下列说法错误的是______(填正确答案标号)。
转化率变化的趋势曲线。下列说法错误的是______(填正确答案标号)。
A.其他条件相同时,为提高 的转化率,生产中可以采取的措施是降低水碳比 的转化率,生产中可以采取的措施是降低水碳比 |
| B.移走部分尿素平衡向正方向移动 |
C.当温度低于190℃,随温度升高 转化率逐渐增大,其原因可能是温度升高平衡向正方向移动 转化率逐渐增大,其原因可能是温度升高平衡向正方向移动 |
D.当温度高于190℃后,随温度升高 转化率逐渐减小,其原因可能是温度升高发生了副反应 转化率逐渐减小,其原因可能是温度升高发生了副反应 |
 )的因素,在恒温下将0.4molNH3和0.2molCO2放入容积为2L的密闭容器中,t1时达到平衡,其c(
)的因素,在恒温下将0.4molNH3和0.2molCO2放入容积为2L的密闭容器中,t1时达到平衡,其c( )随时间t变化趋势曲线如下图2所示。则0~t1时段,用
)随时间t变化趋势曲线如下图2所示。则0~t1时段,用 表示的平均反应速率为
表示的平均反应速率为
Ⅲ.电催化还原
 受到广泛的研究,一种原理如图所示:
受到广泛的研究,一种原理如图所示:
(5)写出A电极发生的电极方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】“低碳经济”已成为全世界科学家研究的重要课题,为减小和消除 对环境的影响,大力提倡新能源电车出行,科学家们为解决电车能源问题,探索出如下三种方案。
对环境的影响,大力提倡新能源电车出行,科学家们为解决电车能源问题,探索出如下三种方案。
Ⅰ.方案一:光解水,制造氢氧燃料电池
(1)下图是某科研机构利用太阳光,在催化剂表面实现高效分解水来制备氢气的历程,关于该历程,下列说法不正确的是_______。

Ⅱ.方案二:将 与
与 反应合成甲醇,制备甲醇燃料电池。制备甲醇的过程可能涉及的反应如下:
反应合成甲醇,制备甲醇燃料电池。制备甲醇的过程可能涉及的反应如下:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
(2)求
_______  ,反应Ⅰ能自发进行的条件是
,反应Ⅰ能自发进行的条件是_______ 。
(3)一定条件下,在2L的密闭容器中发生反应Ⅰ,起始物 和
和 的浓度随时间变化如图1所示,平衡时
的浓度随时间变化如图1所示,平衡时 的体积分数
的体积分数_______ ;若保持其它反应条件不变,起始时仅将容器体积变为3L,请在图1上画出 的浓度随时间变化的趋势图
的浓度随时间变化的趋势图_______ 。

(4)若密闭容器中只发生反应Ⅱ,以下能说明该反应达到平衡状态的是_______(选填字母)。
(5)若CO2和 按一定比例在装有催化剂的反应器中发生反应Ⅰ,一定时间内甲醇的产率和催化剂的催化活性与温度的关系如图2所示。当温度为470K时,图中P点
按一定比例在装有催化剂的反应器中发生反应Ⅰ,一定时间内甲醇的产率和催化剂的催化活性与温度的关系如图2所示。当温度为470K时,图中P点_______ (填“是”或“不是”)处于平衡状态,说出理由_______ ;490K之后,甲醇产率下降,请分析其变化产生的原因_______ 。

Ⅲ.方案三:以二氧化碳为原料,开发新型电池
(6)科学家可以利用如下图装置,“溶解”水中的二氧化碳,生成电能和氢气,请写出二氧化碳生成氢气的电极反应式_______ 。

 对环境的影响,大力提倡新能源电车出行,科学家们为解决电车能源问题,探索出如下三种方案。
对环境的影响,大力提倡新能源电车出行,科学家们为解决电车能源问题,探索出如下三种方案。Ⅰ.方案一:光解水,制造氢氧燃料电池
(1)下图是某科研机构利用太阳光,在催化剂表面实现高效分解水来制备氢气的历程,关于该历程,下列说法不正确的是_______。

| A.该法制氢能量变化是光能→化学能 | B.过程Ⅰ的能量变化等于2倍氢氧键键能 |
C.过程Ⅲ的反应方程为: | D.该历程降低了水分解的反应热 |
Ⅱ.方案二:将
 与
与 反应合成甲醇,制备甲醇燃料电池。制备甲醇的过程可能涉及的反应如下:
反应合成甲醇,制备甲醇燃料电池。制备甲醇的过程可能涉及的反应如下:反应Ⅰ:

反应Ⅱ:

反应Ⅲ:

(2)求

 ,反应Ⅰ能自发进行的条件是
,反应Ⅰ能自发进行的条件是(3)一定条件下,在2L的密闭容器中发生反应Ⅰ,起始物
 和
和 的浓度随时间变化如图1所示,平衡时
的浓度随时间变化如图1所示,平衡时 的体积分数
的体积分数 的浓度随时间变化的趋势图
的浓度随时间变化的趋势图
(4)若密闭容器中只发生反应Ⅱ,以下能说明该反应达到平衡状态的是_______(选填字母)。
| A.CO与CO2浓度比为1∶1 |
B. |
| C.绝热条件下,该密闭体系压强不再变化 |
| D.容器中混合气体的平均摩尔质量不再发生变化 |
 按一定比例在装有催化剂的反应器中发生反应Ⅰ,一定时间内甲醇的产率和催化剂的催化活性与温度的关系如图2所示。当温度为470K时,图中P点
按一定比例在装有催化剂的反应器中发生反应Ⅰ,一定时间内甲醇的产率和催化剂的催化活性与温度的关系如图2所示。当温度为470K时,图中P点
Ⅲ.方案三:以二氧化碳为原料,开发新型电池
(6)科学家可以利用如下图装置,“溶解”水中的二氧化碳,生成电能和氢气,请写出二氧化碳生成氢气的电极反应式

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量), 当闭合该装置的电键 K 时,观察到电流计的指针发生了偏转。请回答下列问题:
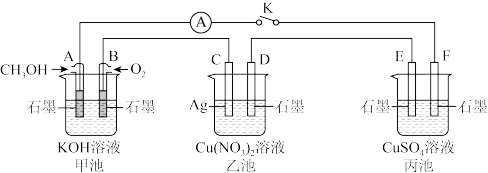
(1)乙池为_____ (填“原电池”.“电解池”或“电镀池”) C 电极的电极反应式为________ 。
(2)丙池中 E 电极为____ (填“正极”.“负极”.“阴极”或“阳极”),电极的电极反应式为__________ 。该池总反应的化学方程式为________________ 。
(3)当乙池中C极质量减轻 54 g 时,甲池中电极理论上消耗 O2的为____ L(标准状况)。
(4)一段时间后,断开电键 K,下列物质能使丙池恢复到反应前浓度的是____ (填选项字母)。
A.Cu B.CuO C.Cu(OH)2 D.CuCO3

(1)乙池为
(2)丙池中 E 电极为
(3)当乙池中C极质量减轻 54 g 时,甲池中电极理论上消耗 O2的为
(4)一段时间后,断开电键 K,下列物质能使丙池恢复到反应前浓度的是
A.Cu B.CuO C.Cu(OH)2 D.CuCO3
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】根据所学知识,回答下列问题:
(1)在25℃、 下,已知完全燃烧4.4g丙烷气体,生成
下,已知完全燃烧4.4g丙烷气体,生成 和液态水时,释放
和液态水时,释放 热量,
热量, 的燃烧热
的燃烧热
___________  。
。
(2)已知: 。现有
。现有 和
和 的混合气体共
的混合气体共 ,完全燃烧时释放
,完全燃烧时释放 热量,则在混合气体中
热量,则在混合气体中 和
和 的体积比是
的体积比是___________ ;
(3)一个化学过程的示意图如图。已知甲池的总反应为 。
。

①图中甲池是___________ 装置;A(石墨)电极的名称是___________ 。
②写出通入 的电极的电极反应式:
的电极的电极反应式:___________ 。
③乙池中发生反应的化学方程式为___________ 。当乙池中B(Ag)电极的质量增加5.40g时,甲池中理论上消耗___________  (标准状况下)
(标准状况下) 。
。
(1)在25℃、
 下,已知完全燃烧4.4g丙烷气体,生成
下,已知完全燃烧4.4g丙烷气体,生成 和液态水时,释放
和液态水时,释放 热量,
热量, 的燃烧热
的燃烧热
 。
。(2)已知:
 。现有
。现有 和
和 的混合气体共
的混合气体共 ,完全燃烧时释放
,完全燃烧时释放 热量,则在混合气体中
热量,则在混合气体中 和
和 的体积比是
的体积比是(3)一个化学过程的示意图如图。已知甲池的总反应为
 。
。
①图中甲池是
②写出通入
 的电极的电极反应式:
的电极的电极反应式:③乙池中发生反应的化学方程式为
 (标准状况下)
(标准状况下) 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】电化学在工业生产中具有重要作用。
Ⅰ.氯碱工业
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,请按要求回答相关问题:
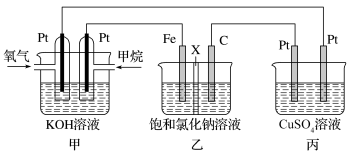
(1)甲池为___________ (填“电解池”或“原电池”);丙池中左侧Pt电极作__________ 极;乙池中X为___________ (填“阳离子交换膜”或“阴离子交换膜”)。
(2)乙池涉及的总反应的离子方程式为____________________________ 。
(3)丙池右侧Pt电极的电极反应式为______________________ 。
Ⅱ.冶金工业
一种从高炉气回收 制储氢物质
制储氢物质 的综合利用示意图如图所示,请按要求回答相关问题:
的综合利用示意图如图所示,请按要求回答相关问题:
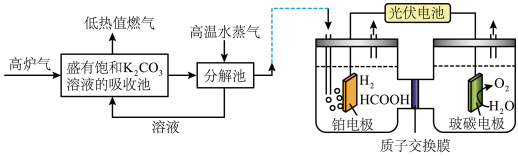
(4)某温度下,当吸收池中溶液的 时,此时该溶液中
时,此时该溶液中
__________ [已知:该温度下 ,
, ]。
]。
(5)利用电化学原理控制反应条件能将 电催化还原为
电催化还原为 ,写出铂电极上生成
,写出铂电极上生成 的电极反应式:
的电极反应式:________________________ ;电解过程中还伴随着析氢反应 ,若生成
,若生成 的电解效率为80%,生成氢气的电解效率为20%,当电路中转移
的电解效率为80%,生成氢气的电解效率为20%,当电路中转移 时,阴极室溶液的质量增加
时,阴极室溶液的质量增加_____________ g[B的电解效率 ]。
]。
Ⅰ.氯碱工业
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,请按要求回答相关问题:

(1)甲池为
(2)乙池涉及的总反应的离子方程式为
(3)丙池右侧Pt电极的电极反应式为
Ⅱ.冶金工业
一种从高炉气回收
 制储氢物质
制储氢物质 的综合利用示意图如图所示,请按要求回答相关问题:
的综合利用示意图如图所示,请按要求回答相关问题:
(4)某温度下,当吸收池中溶液的
 时,此时该溶液中
时,此时该溶液中
 ,
, ]。
]。(5)利用电化学原理控制反应条件能将
 电催化还原为
电催化还原为 ,写出铂电极上生成
,写出铂电极上生成 的电极反应式:
的电极反应式: ,若生成
,若生成 的电解效率为80%,生成氢气的电解效率为20%,当电路中转移
的电解效率为80%,生成氢气的电解效率为20%,当电路中转移 时,阴极室溶液的质量增加
时,阴极室溶液的质量增加 ]。
]。
您最近一年使用:0次



