坦桑石是一种世界公认的新兴宝石,这种宝石于1967年首次在赤道雪山脚下的阿鲁沙地区被发现。坦桑石的主要化学成分为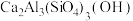 ,还可含有V、Cr、Mn等元素。
,还可含有V、Cr、Mn等元素。
 下列状态的铝中,电离最外层的一个电子所需能量最大的是
下列状态的铝中,电离最外层的一个电子所需能量最大的是________  填序号
填序号 。
。
①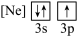 ②
②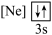 ③
③ ④
④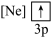
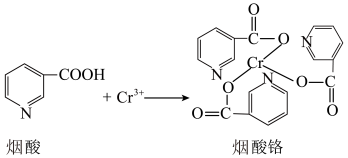
 烟酸铬是铬的一种化合物,其合成过程如下:
烟酸铬是铬的一种化合物,其合成过程如下:
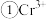 核外电子排布式为
核外电子排布式为________ 。
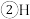 、C、N、O的电负性由大到小的顺序是
、C、N、O的电负性由大到小的顺序是_________ 。
 烟酸中碳、氮原子的杂化方式分别为
烟酸中碳、氮原子的杂化方式分别为________ 、________ 。
 分子中的大
分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数
键的电子数 如二氧化碳分子中的大
如二氧化碳分子中的大 键可表示为
键可表示为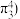 ,则烟酸中的大
,则烟酸中的大 键应表示为
键应表示为___________ 。
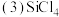 、
、 都极易水解。
都极易水解。 、
、 都属于
都属于______  填“极性”或“非极性”
填“极性”或“非极性” 分子,其熔点的关系为
分子,其熔点的关系为
________  填“
填“ ”“
”“ ”或“
”或“ ”
”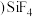 。
。
 将Mn掺入GaAs晶体
将Mn掺入GaAs晶体 图甲
图甲 可得到稀磁性半导体材料
可得到稀磁性半导体材料 图乙
图乙 ,图甲、图乙晶体结构不变。
,图甲、图乙晶体结构不变。
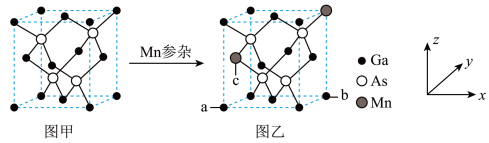
 图乙中a点和b点的原子坐标参数分别为
图乙中a点和b点的原子坐标参数分别为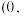 0,
0, 和
和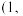 1,
1, ,则c点的原子坐标参数为
,则c点的原子坐标参数为________ 。
 设图甲晶体的密度为
设图甲晶体的密度为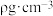 ,用
,用 表示阿伏加 德罗常数的数值,则该晶胞中距离最近的两个镓原子之间的距离为
表示阿伏加 德罗常数的数值,则该晶胞中距离最近的两个镓原子之间的距离为________________ pm。
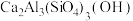 ,还可含有V、Cr、Mn等元素。
,还可含有V、Cr、Mn等元素。  下列状态的铝中,电离最外层的一个电子所需能量最大的是
下列状态的铝中,电离最外层的一个电子所需能量最大的是 填序号
填序号 。
。①
 ②
②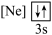 ③
③ ④
④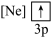
 烟酸铬是铬的一种化合物,其合成过程如下:
烟酸铬是铬的一种化合物,其合成过程如下:
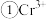 核外电子排布式为
核外电子排布式为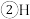 、C、N、O的电负性由大到小的顺序是
、C、N、O的电负性由大到小的顺序是 烟酸中碳、氮原子的杂化方式分别为
烟酸中碳、氮原子的杂化方式分别为 分子中的大
分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数
键的电子数 如二氧化碳分子中的大
如二氧化碳分子中的大 键可表示为
键可表示为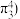 ,则烟酸中的大
,则烟酸中的大 键应表示为
键应表示为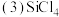 、
、 都极易水解。
都极易水解。 、
、 都属于
都属于 填“极性”或“非极性”
填“极性”或“非极性” 分子,其熔点的关系为
分子,其熔点的关系为
 填“
填“ ”“
”“ ”或“
”或“ ”
”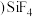 。
。 将Mn掺入GaAs晶体
将Mn掺入GaAs晶体 图甲
图甲 可得到稀磁性半导体材料
可得到稀磁性半导体材料 图乙
图乙 ,图甲、图乙晶体结构不变。
,图甲、图乙晶体结构不变。
 图乙中a点和b点的原子坐标参数分别为
图乙中a点和b点的原子坐标参数分别为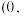 0,
0, 和
和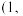 1,
1, ,则c点的原子坐标参数为
,则c点的原子坐标参数为 设图甲晶体的密度为
设图甲晶体的密度为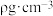 ,用
,用 表示阿伏加 德罗常数的数值,则该晶胞中距离最近的两个镓原子之间的距离为
表示阿伏加 德罗常数的数值,则该晶胞中距离最近的两个镓原子之间的距离为
更新时间:2020-01-27 15:46:04
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】A、B、C、D、E、F六种元素为前四周期元素,原子序数依次增大。A的最高正价和最低负价的绝对值相等,B的基态原子的电子分布在3个不同的能级且各能级中电子数相等。D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子的s能级的电子总数与p能级的电子数相等,F的基态原子在同周期元素中未成对电子数最多。请回答下列问题:
(1)F元素在周期表中的位置_________ ;F元素价电子排布式为 ___________ 。
(2)B、C、D、E的原子的第一电离能由小到大的顺序为________ 。(用元素符号回答)
(3)下列关于B2A2分子和A2D2分子的说法正确的是____________ 。
A.分子中都含有σ键和π键
B.都是含极性键和非极性键的直线型分子
C.B2A2的沸点明显低于A2D2
D.都具有还原性
(4) 由 A、C 两种元素可以形成一种 CA5的既含离子键又含共价键的化合物,其电子式为_______ ;
(5) 金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。面心立方晶胞和体心立方晶胞中实际 含有的Fe原子个数之比为_____________ 。

(1)F元素在周期表中的位置
(2)B、C、D、E的原子的第一电离能由小到大的顺序为
(3)下列关于B2A2分子和A2D2分子的说法正确的是
A.分子中都含有σ键和π键
B.都是含极性键和非极性键的直线型分子
C.B2A2的沸点明显低于A2D2
D.都具有还原性
(4) 由 A、C 两种元素可以形成一种 CA5的既含离子键又含共价键的化合物,其电子式为
(5) 金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。面心立方晶胞和体心立方晶胞中实际 含有的Fe原子个数之比为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】C、N、P、Si是重要的非金属元素,在生产、生活中有重要应用。回答下列问题:
(1)下列氮原子的电子排布图表示的状态中,能量最高的是_______(填序号)。
(2)原子中运动的电子有两种相反的自旋状态,一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态Si原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Si原子,其价电子自旋磁量子数的代数和为_______ 。
(3) 中共用电子对偏向C,
中共用电子对偏向C, 中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为_______ 。
(4) 分子的中心原子的价层电子对数为
分子的中心原子的价层电子对数为_______ ,分子的立体构型为三角双锥形, 属于
属于_______ 分子(填“极性”或“非极性”),其中心原子杂化类型为_______ (填序号)。
A. B.
B. C.
C. D.
D.
(5)试用下表中的键能数据解释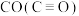 比
比 相对活泼的原因:
相对活泼的原因:_______ 。
(1)下列氮原子的电子排布图表示的状态中,能量最高的是_______(填序号)。
A.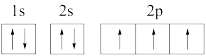 | B.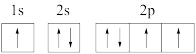 |
C.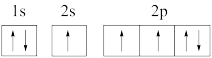 | D.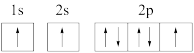 |
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态Si原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Si原子,其价电子自旋磁量子数的代数和为(3)
 中共用电子对偏向C,
中共用电子对偏向C, 中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为(4)
 分子的中心原子的价层电子对数为
分子的中心原子的价层电子对数为 属于
属于A.
 B.
B. C.
C. D.
D.
(5)试用下表中的键能数据解释
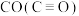 比
比 相对活泼的原因:
相对活泼的原因:| C—O | C=O |  | |
键能 | 357.7 | 798.9 | 1071.9 |
| N—N | N=N |  | |
键能 | 154.8 | 418.4 | 941.7 |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】按要求回答下列问题
(1)中国古代四大发明之一-黑火药,它的爆炸反应为:2KNO3 + 3C+S A + N2↑+ 3CO2↑(已配平)
A + N2↑+ 3CO2↑(已配平)
①除S外,上列元素的电负性从大到小依次为_______ 。
②在生成物中,A的电子式_______ ,含极性共价键的分子的中心原子轨道杂化类型为_______ 。
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为_______ 。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为_______ ,Q2+的未成对电子数是_______ 。
(3)ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
①O、S、Se原子的第一电离能由大到小的顺序为_______ 。
②H2Se的酸性比H2S_______ (填“强”或“弱”)。气态SeO3分子的价层电子对互斥模型为_______ ,SeO 离子中Se的杂化方式为
离子中Se的杂化方式为_______ 。
(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是_______ 。
(5)已知Ti3+可形成配位数为6的配合物。现有紫色和绿色两种含钛晶体的配合物,其组成均为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种晶体的样品配成溶液;
b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤,经洗涤干燥后称量,发现绿色晶体产生沉淀的质量为紫色晶体产生沉淀质量的三分之二。则绿色晶体的配合物为_______ 。
(1)中国古代四大发明之一-黑火药,它的爆炸反应为:2KNO3 + 3C+S
 A + N2↑+ 3CO2↑(已配平)
A + N2↑+ 3CO2↑(已配平)①除S外,上列元素的电负性从大到小依次为
②在生成物中,A的电子式
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为
(3)ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
①O、S、Se原子的第一电离能由大到小的顺序为
②H2Se的酸性比H2S
 离子中Se的杂化方式为
离子中Se的杂化方式为(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是
(5)已知Ti3+可形成配位数为6的配合物。现有紫色和绿色两种含钛晶体的配合物,其组成均为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种晶体的样品配成溶液;
b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤,经洗涤干燥后称量,发现绿色晶体产生沉淀的质量为紫色晶体产生沉淀质量的三分之二。则绿色晶体的配合物为
您最近一年使用:0次
【推荐1】2022年2月我国科学家在《科学》杂志发表反型钙钛矿太阳能电池研究方面的最新科研成果论文,为钙钛矿电池研究开辟新方向。
(1)基态钛原子的px原子轨道上的电子数为____ 个。与钛同周期的第ⅡB族和ⅢA族两种元素中第一电离能较大的是____ (写元素符号)。
(2)Ti的配合物有多种。Ti(CO)6、Ti(H2O) 、TiF
、TiF 的配体所含原子中电负性由大到小的顺序是
的配体所含原子中电负性由大到小的顺序是____ (写元素符号);Ti(H2O) 中∠H—O—H
中∠H—O—H____ (填“大于”、“小于”或“等于”)单个水分子中∠H—O—H;Ti(NO3)4的球棍结构如图,Ti的配位数是____ ,N原子的杂化方式为____ 。
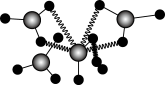
(3)反型钙钛矿电池无需使用具有光催化活性的TiO2(通过氮掺杂生成TiO2-aNb,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。

则TiO2-aNb晶体中a=____ 。已知原子1、2的分数坐标为(0,0, )和(1,0,0),则原子3的坐标分别为
)和(1,0,0),则原子3的坐标分别为____ ,设阿伏加德罗常数的值为NA,TiO2的密度为____ g·cm-3(列出计算式)
(1)基态钛原子的px原子轨道上的电子数为
(2)Ti的配合物有多种。Ti(CO)6、Ti(H2O)
 、TiF
、TiF 的配体所含原子中电负性由大到小的顺序是
的配体所含原子中电负性由大到小的顺序是 中∠H—O—H
中∠H—O—H
(3)反型钙钛矿电池无需使用具有光催化活性的TiO2(通过氮掺杂生成TiO2-aNb,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。

则TiO2-aNb晶体中a=
 )和(1,0,0),则原子3的坐标分别为
)和(1,0,0),则原子3的坐标分别为
您最近一年使用:0次
【推荐2】[选修3——物质结构与性质] 元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。
(1)在Y的最高价氧化物分子中,Y原子轨道的杂化类型是_______________ 。
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是_______________________ ;Z的氢化物在固态时的密度比在液态时还小,其原因是_________
(3)Y与Z可形成YZ42-。
①YZ42-的空间构型为________________ (用文字描述)。
②写出一种与YZ42-互为等电子体的分子的化学式:_________________ 。
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1 mol该配合物中含有σ键的数目为_______ 。
(5)X与Y所形成化合物晶体的晶胞如图所:
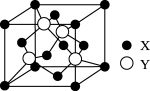
①在该晶体中,X离子的配位数为__________ ,与Y距离最近且距离相等的Y原子的数目为________ 。
②该晶胞的边长为a cm,该晶体的密度为__________________ g·cm-3。
(1)在Y的最高价氧化物分子中,Y原子轨道的杂化类型是
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是
(3)Y与Z可形成YZ42-。
①YZ42-的空间构型为
②写出一种与YZ42-互为等电子体的分子的化学式:
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1 mol该配合物中含有σ键的数目为
(5)X与Y所形成化合物晶体的晶胞如图所:

①在该晶体中,X离子的配位数为
②该晶胞的边长为a cm,该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】元素周期表中第四周期过渡元素在工业及生活方面有重要应用。请回答下列问题:
(1)“钛”被称为21世纪金属,画出基态钛的价电子的电子排布图_______ 。
(2)CrO5中有4个-1价的O。CrO5中σ键与π键个数比为_______ 。
(3)[Co(NH3)4Cl2]+呈八面体结构,则其结构有_______ 种。能区别[Co(NH3)4Cl2]Cl和[Co(NH3)4Cl2]NO3两种溶液的试剂是_______ (填标号)。
a.浓氨水 b.NaOH溶液 c.稀H2SO4 d.AgNO3溶液
(4)K3[Fe(CN)6]是鉴别Fe2+的重要试剂,这四种元素的电负性从大到小的顺序是_______ (填元素符号),写出与CN-互为等电子体的两种微粒_______ 。K3[Fe(CN)6]中碳的杂化方式与下列物质中碳杂化方式相同的是_______ (填标号)。
A.CH2Cl2 B.C2H2 C.溴苯 D.HCN
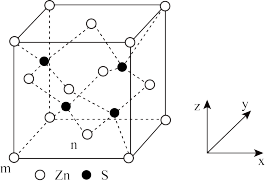
(5)ZnS的晶胞如图所示,若m点坐标为(0,0,0),n点坐标为( ,
, ,0)此晶胞中与n点最远的S的坐标为
,0)此晶胞中与n点最远的S的坐标为_______ 。若Zn与S弹性相切,其半径分别为apm和bpm,则ZnS的密度为_______ g·cm-3(设NA为阿伏加德罗常数的值)。
(1)“钛”被称为21世纪金属,画出基态钛的价电子的电子排布图
(2)CrO5中有4个-1价的O。CrO5中σ键与π键个数比为
(3)[Co(NH3)4Cl2]+呈八面体结构,则其结构有
a.浓氨水 b.NaOH溶液 c.稀H2SO4 d.AgNO3溶液
(4)K3[Fe(CN)6]是鉴别Fe2+的重要试剂,这四种元素的电负性从大到小的顺序是
A.CH2Cl2 B.C2H2 C.溴苯 D.HCN
(5)ZnS的晶胞如图所示,若m点坐标为(0,0,0),n点坐标为(
 ,
, ,0)此晶胞中与n点最远的S的坐标为
,0)此晶胞中与n点最远的S的坐标为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】氮是生命体的重要组成元素,自然界中氮的循环对于生命活动有重要意义。
(1)一种利用锂及其化合物的循环,将空气中的N2转化为NH3的过程如图所示。

①N2和CO是分子量相同的双原子分子,但液态N2的沸点要__ (填“ ”、“
”、“ ”或“
”或“ ”)液态CO。
”)液态CO。
②写出转化(Ⅱ)的化学方程式:___ 。
③转化(Ⅲ)是电解熔融LiOH,该反应的化学方程式为___ 。
(2)氮肥厂的废水中氮元素以NH3•H2O、NH3和NH 的形式存在,直接排放会造成水体富营养化。一种电化学氧化处理氨氮废水的原理是在酸性废水中加入NaCl进行电解,阳极产生的HClO可氧化氨氮,将其转化为N2。电解过程中,废水中初始Cl-浓度对氨氮去除速率及能耗(处理一定量氨氮消耗的电能)的影响关系如图所示。
的形式存在,直接排放会造成水体富营养化。一种电化学氧化处理氨氮废水的原理是在酸性废水中加入NaCl进行电解,阳极产生的HClO可氧化氨氮,将其转化为N2。电解过程中,废水中初始Cl-浓度对氨氮去除速率及能耗(处理一定量氨氮消耗的电能)的影响关系如图所示。

①电解过程中阴极附近溶液的pH___ (填“升高”、“降低”或“不变”)。
②当Cl-浓度减小时,氨氮去除速率下降,能耗却增加的原因是___ 。
③保持加入NaCl的量不变,当废水的pH低于4时,氨氮去除速率也会降低的原因是___ 。
(1)一种利用锂及其化合物的循环,将空气中的N2转化为NH3的过程如图所示。

①N2和CO是分子量相同的双原子分子,但液态N2的沸点要
 ”、“
”、“ ”或“
”或“ ”)液态CO。
”)液态CO。②写出转化(Ⅱ)的化学方程式:
③转化(Ⅲ)是电解熔融LiOH,该反应的化学方程式为
(2)氮肥厂的废水中氮元素以NH3•H2O、NH3和NH
 的形式存在,直接排放会造成水体富营养化。一种电化学氧化处理氨氮废水的原理是在酸性废水中加入NaCl进行电解,阳极产生的HClO可氧化氨氮,将其转化为N2。电解过程中,废水中初始Cl-浓度对氨氮去除速率及能耗(处理一定量氨氮消耗的电能)的影响关系如图所示。
的形式存在,直接排放会造成水体富营养化。一种电化学氧化处理氨氮废水的原理是在酸性废水中加入NaCl进行电解,阳极产生的HClO可氧化氨氮,将其转化为N2。电解过程中,废水中初始Cl-浓度对氨氮去除速率及能耗(处理一定量氨氮消耗的电能)的影响关系如图所示。
①电解过程中阴极附近溶液的pH
②当Cl-浓度减小时,氨氮去除速率下降,能耗却增加的原因是
③保持加入NaCl的量不变,当废水的pH低于4时,氨氮去除速率也会降低的原因是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】2023年6月,科学家首次合成含铍-铍键的固态化合物,相关成果发表于《科学》杂志。该分子入选2023年最“炫”分子榜单,其结构如图所示,回答下列问题:
(2)固态双铍化合物的化学式为______ ,它含有______ (填标号)。
A.极性键 B.非极性键 C.金属键 D. 键
键
(3)卤化铍的熔点如表所示:
① 属于
属于______ (填“极性”或“非极性”)分子。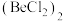 中Be原子的杂化方式相同,且所有原子都在同一平面上。b的结构式为
中Be原子的杂化方式相同,且所有原子都在同一平面上。b的结构式为______ (标出配位键)。
③ 、
、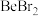 、
、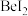 的熔点依次升高的原因是
的熔点依次升高的原因是______ 。
(4)Be的某种氧化物晶体是制备氟硼铍酸钾晶体的原料之一,其晶胞结构如图所示。设晶胞边长为a pm,用 表示阿伏加德罗常数的值,则该晶体的密度为
表示阿伏加德罗常数的值,则该晶体的密度为______  (用含a和
(用含a和 的式子表示)。
的式子表示)。

A. | B. | C.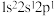 | D.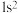 |
(2)固态双铍化合物的化学式为
A.极性键 B.非极性键 C.金属键 D.
 键
键(3)卤化铍的熔点如表所示:
|
|
|
|
|
熔点/℃ | 552 | 399 | 488 | 510 |
 属于
属于②氯化铍在气态时存在 分子(a)和二聚分子
分子(a)和二聚分子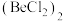 (b),固态时则具有如图所示的链状结构(c)
(b),固态时则具有如图所示的链状结构(c)
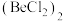 中Be原子的杂化方式相同,且所有原子都在同一平面上。b的结构式为
中Be原子的杂化方式相同,且所有原子都在同一平面上。b的结构式为③
 、
、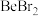 、
、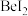 的熔点依次升高的原因是
的熔点依次升高的原因是(4)Be的某种氧化物晶体是制备氟硼铍酸钾晶体的原料之一,其晶胞结构如图所示。设晶胞边长为a pm,用
 表示阿伏加德罗常数的值,则该晶体的密度为
表示阿伏加德罗常数的值,则该晶体的密度为 (用含a和
(用含a和 的式子表示)。
的式子表示)。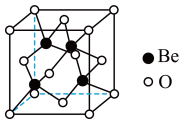
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】苯乙烯是生产塑料和合成橡胶的重要有机原料,可由乙苯催化脱氢获得。
(1)科技工作者结合实验与计算机模拟结果,研究了一个乙苯分子在催化剂表面脱氢制苯乙烯的反应,其历程如图1所示(吸附在催化剂表面的物质用*标注):
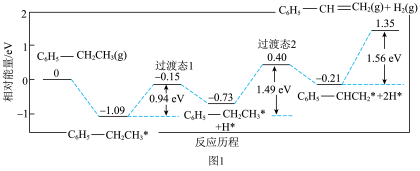
乙苯脱氢制苯乙烯反应的焓变
___________ (填“>”“<”或“=”)0,为提高乙苯的平衡转化率,应选择的反应条件为___________ (填标号)。
A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压
(2)有研究者发现,在 气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图2:
气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图2:
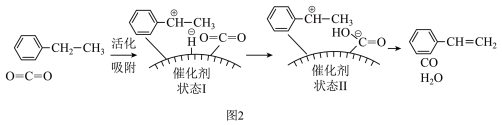
①该过程的总反应的化学方程式为___________ 。
② 属于
属于___________ (填“极性”或“非极性”)分子;干冰中每个 分子周围有
分子周围有___________ 个紧邻分子。
③从资源综合利用角度分析, 氧化乙苯脱氢制苯乙烯的优点是
氧化乙苯脱氢制苯乙烯的优点是___________ 。
(3)100kPa恒压下,将2mol乙苯蒸气通入体积可变的密闭容器中发生乙苯脱氢制苯乙烯反应。
① ℃时,反应经过10min达到平衡,此时苯乙烯的体积分数为0.375,则乙苯的转化率为
℃时,反应经过10min达到平衡,此时苯乙烯的体积分数为0.375,则乙苯的转化率为________ ,0~10min内的平均反应速率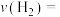
_______  ,该温度下的
,该温度下的
_______ kPa。
② ℃时,若再向体系中通入氮气,此时
℃时,若再向体系中通入氮气,此时
___________ (填“增大”“减小”或“不变”)。
(1)科技工作者结合实验与计算机模拟结果,研究了一个乙苯分子在催化剂表面脱氢制苯乙烯的反应,其历程如图1所示(吸附在催化剂表面的物质用*标注):

乙苯脱氢制苯乙烯反应的焓变

A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压
(2)有研究者发现,在
 气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图2:
气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图2:
①该过程的总反应的化学方程式为
②
 属于
属于 分子周围有
分子周围有③从资源综合利用角度分析,
 氧化乙苯脱氢制苯乙烯的优点是
氧化乙苯脱氢制苯乙烯的优点是(3)100kPa恒压下,将2mol乙苯蒸气通入体积可变的密闭容器中发生乙苯脱氢制苯乙烯反应。
①
 ℃时,反应经过10min达到平衡,此时苯乙烯的体积分数为0.375,则乙苯的转化率为
℃时,反应经过10min达到平衡,此时苯乙烯的体积分数为0.375,则乙苯的转化率为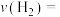
 ,该温度下的
,该温度下的
②
 ℃时,若再向体系中通入氮气,此时
℃时,若再向体系中通入氮气,此时
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】天宫二号空间实验室于2016年9月15 日在酒泉卫星发射中心发射成功。实验室承载了10余项太空实验,其中包含了好比科幻英雄“综合材料”多晶碲化锌(ZnTe)的实验。
(1)电负性Zn___________ Te(填“>”或“<”或“=”)。
(2)O、S、Se与Te元素位于同一主族。基态碲(Te)原子核外电子排布式为[Kr]________ ,有_______ 个未成对电子。
(3)H2O、H2S、H2Se沸点由低到高顺序为______ ,推断的依据是_______ ;SO2分子中S原子采取_____ 杂化;用价层电子对互斥理论解释SO42-的键角大于SO32-的原因是____________ 。
(4)向氯化锌溶液中加入过量的氨水,得到[Zn(NH3)4]Cl2,此配位化合物中含有的化学键有共价键、____ 、_______ 。
(5)碲化锌晶体有两种结构,其中一种晶胞结构如下图:
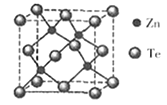
晶胞中含有_____ 个Te原子;与Te原子距离最近的Te原子有______ 个;若两个距离最近的Te原子间距为apm.则晶体密度为_________ g/cm3。
(1)电负性Zn
(2)O、S、Se与Te元素位于同一主族。基态碲(Te)原子核外电子排布式为[Kr]
(3)H2O、H2S、H2Se沸点由低到高顺序为
(4)向氯化锌溶液中加入过量的氨水,得到[Zn(NH3)4]Cl2,此配位化合物中含有的化学键有共价键、
(5)碲化锌晶体有两种结构,其中一种晶胞结构如下图:

晶胞中含有
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】【化学——选修3:物质结构与性质】磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
(1)基态P原子的核外电子排布式为 1 ,有 2 个未成对电子。
(2)磷的一种同素异形体——白磷(P4)的立体构型为 3 ,其键角为 4 ,推测其在CS2中的溶解度 5 (填“大于”或“小于”)在水中的溶解度。
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6º和107º,试分析PH3的键角小于NH3的原因 6 。
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如上左图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为 7 ,其中心原子杂化轨道类型为 8 ,B为 9 。
(5)磷化硼(BP)是一种超硬耐磨涂层材料,上右图为其立方晶胞,其中的每个原子均满足8电子稳定结构,试判断其熔点 10 (填“高于”或“低于”)金刚石熔点。
已知其B—P键长均为x cm,则其密度为 11 g﹒cm—3(列出计算式即可)。
(1)基态P原子的核外电子排布式为
(2)磷的一种同素异形体——白磷(P4)的立体构型为
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6º和107º,试分析PH3的键角小于NH3的原因

(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如上左图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为
(5)磷化硼(BP)是一种超硬耐磨涂层材料,上右图为其立方晶胞,其中的每个原子均满足8电子稳定结构,试判断其熔点
已知其B—P键长均为x cm,则其密度为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】精脱硫技术主要用于煤气中羰基硫(COS)和二硫化碳( )的转化。
)的转化。
(1)利用焦炉煤气中的 可脱除煤气中羰基硫(COS)。羰基硫氢化反应历程有途径Ⅰ和途径Ⅱ两种可能,如图所示。
可脱除煤气中羰基硫(COS)。羰基硫氢化反应历程有途径Ⅰ和途径Ⅱ两种可能,如图所示。

①已知羰基硫氢化反应速率较快,推测其更合理的反应历程是途径___________ (填“Ⅰ”或“Ⅱ”)。
②反应 的
的
___________ kJ⋅mol 。
。
(2) 可作羰基硫氢化反应的催化剂,催化机理如图所示。
可作羰基硫氢化反应的催化剂,催化机理如图所示。

不同钼(Mo)含量的 催化剂对COS转化率和
催化剂对COS转化率和 的选择性不同,实验数据如图:
的选择性不同,实验数据如图:
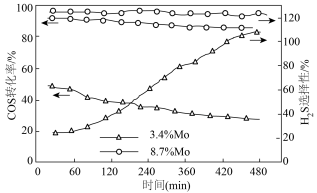
①根据图中数据,选择___________ (填“3.4% Mo”或“8.7% Mo”)作催化剂效果最好。
②当 选择性低于100%时表明部分COS气体与催化剂发生了反应,催化剂有吸硫现象,若
选择性低于100%时表明部分COS气体与催化剂发生了反应,催化剂有吸硫现象,若 选择性高于100%,可能的原因是
选择性高于100%,可能的原因是___________ 。
(3)金属Mo的晶胞如图所示,设晶体密度为ρ g⋅cm ,则晶胞参数为
,则晶胞参数为___________ pm(阿伏加德罗常数的值为 )。
)。

(4)一定温度下,向恒容密闭容器中充入物质的量之比为1∶4的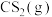 和
和 ,发生反应
,发生反应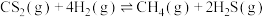 ,容器内气体压强随时间变化如表所示。
,容器内气体压强随时间变化如表所示。
①0~250 min内, 分压的平均变化值为
分压的平均变化值为___________ kPa⋅min 。
。
②该温度下,平衡常数
___________ (kPa)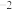 (列出计算式)。
(列出计算式)。
 )的转化。
)的转化。(1)利用焦炉煤气中的
 可脱除煤气中羰基硫(COS)。羰基硫氢化反应历程有途径Ⅰ和途径Ⅱ两种可能,如图所示。
可脱除煤气中羰基硫(COS)。羰基硫氢化反应历程有途径Ⅰ和途径Ⅱ两种可能,如图所示。
①已知羰基硫氢化反应速率较快,推测其更合理的反应历程是途径
②反应
 的
的
 。
。(2)
 可作羰基硫氢化反应的催化剂,催化机理如图所示。
可作羰基硫氢化反应的催化剂,催化机理如图所示。
不同钼(Mo)含量的
 催化剂对COS转化率和
催化剂对COS转化率和 的选择性不同,实验数据如图:
的选择性不同,实验数据如图:
①根据图中数据,选择
②当
 选择性低于100%时表明部分COS气体与催化剂发生了反应,催化剂有吸硫现象,若
选择性低于100%时表明部分COS气体与催化剂发生了反应,催化剂有吸硫现象,若 选择性高于100%,可能的原因是
选择性高于100%,可能的原因是(3)金属Mo的晶胞如图所示,设晶体密度为ρ g⋅cm
 ,则晶胞参数为
,则晶胞参数为 )。
)。
(4)一定温度下,向恒容密闭容器中充入物质的量之比为1∶4的
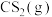 和
和 ,发生反应
,发生反应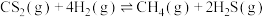 ,容器内气体压强随时间变化如表所示。
,容器内气体压强随时间变化如表所示。| 时间/min | 0 | 50 | 100 | 150 | 200 | 250 | 300 |
| 压强/kPa | 100 | 88.0 | 79.8 | 72.4 | 68.2 | 65.0 | 65.0 |
 分压的平均变化值为
分压的平均变化值为 。
。②该温度下,平衡常数

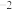 (列出计算式)。
(列出计算式)。
您最近一年使用:0次