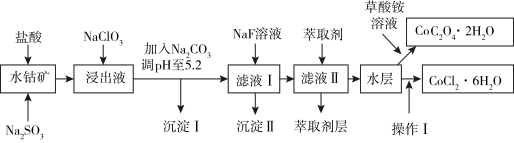
利用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)可制多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备流程:
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等;
②沉淀I中只含有两种沉淀;
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)浸出过程中Co2O3发生反应的离子反应方程式为______________ 。
(2)NaClO3在浸出液中发生的离子反应方程式为__________________ 。
(3)加入Na2CO3调pH至5.2,目的是_______________ ;萃取剂层含锰元素,则沉淀II的主要成分为_____________ 。
(4)操作I包括:将水层加入浓盐酸调整pH为2~3,___________ 、____________ 、过滤、洗涤、减压烘干等过程。
(5)粗产品中CoCl2·6H2O含量可通过以下方法测定:称取一定质量的粗产品溶于水,加入足量硝酸酸化的硝酸银溶液,过滤、洗涤、干燥后,通过测定沉淀质量来计算CoCl2·6H2O的质量分数。若操作I中因减压烘干使CoCl2·6H2O的结晶水减少,则以此方法测得的CoCl2·6H2O质量分数与实际值相比________ (填“偏高”“偏低”或“不变”)。
(6)将5.49g草酸亚钴晶体(CoC2O4·2H2O)置于空气中加热,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表所示:
经测定,整个受热过程,只产生水蒸气和CO2气体,则290~320℃温度范围,剩余的固体物质化学式为_______ 。(已知:CoC2O4·2H2O的摩尔质量为183 g/mol)

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等;
②沉淀I中只含有两种沉淀;
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)NaClO3在浸出液中发生的离子反应方程式为
(3)加入Na2CO3调pH至5.2,目的是
(4)操作I包括:将水层加入浓盐酸调整pH为2~3,
(5)粗产品中CoCl2·6H2O含量可通过以下方法测定:称取一定质量的粗产品溶于水,加入足量硝酸酸化的硝酸银溶液,过滤、洗涤、干燥后,通过测定沉淀质量来计算CoCl2·6H2O的质量分数。若操作I中因减压烘干使CoCl2·6H2O的结晶水减少,则以此方法测得的CoCl2·6H2O质量分数与实际值相比
(6)将5.49g草酸亚钴晶体(CoC2O4·2H2O)置于空气中加热,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表所示:
| 温度范围/℃ | 固体质量/g |
| 150~210 | 4.41 |
| 290~320 | 2.41 |
更新时间:2020-02-19 15:02:55
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验小组探究 和
和 的性质。
的性质。
【进行实验】
(1)写出实验1中 与盐酸反应的离子方程式
与盐酸反应的离子方程式___________ 。
(2)①实验2中,试剂a是___________ ,此实验得出的结论是___________ 。
②称量 固体168g,加热一段时间之后,剩余固体的质量为137g,则剩余固体中
固体168g,加热一段时间之后,剩余固体的质量为137g,则剩余固体中 与
与 的物质的量之比为
的物质的量之比为___________ 。
已知: 易溶于水。
易溶于水。
(3) 溶液与
溶液与 溶液混合的现象中,有些只观察到浑浊但没有观察到气体,可能原因是
溶液混合的现象中,有些只观察到浑浊但没有观察到气体,可能原因是___________ 。
(4)写出溶液中 与
与 反应的离子方程式
反应的离子方程式___________ 。
【反思评价】
(5)根据实验3,鉴别浓度均为0.50 的
的 和
和 的方法是:分别取等量溶液置于两试管中,
的方法是:分别取等量溶液置于两试管中,___________ 。
 和
和 的性质。
的性质。【进行实验】
| 序号 | 实验装置 | 主要实验步骤 | 实验现象 |
| 实验1 |  | 向2支试管中分别加入少量 和 和 溶液,再分别滴加盐酸 溶液,再分别滴加盐酸 | 2支试管中均有气泡产生 |
| 实验2 | 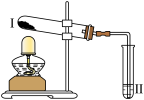 | 向Ⅱ中加入试剂a,向Ⅰ中加入少量 或 或 固体,分别加热一段时间 固体,分别加热一段时间 |  受热时Ⅱ中无明显现象, 受热时Ⅱ中无明显现象, 受热时Ⅱ出现浑浊 受热时Ⅱ出现浑浊 |
(1)写出实验1中
 与盐酸反应的离子方程式
与盐酸反应的离子方程式(2)①实验2中,试剂a是
②称量
 固体168g,加热一段时间之后,剩余固体的质量为137g,则剩余固体中
固体168g,加热一段时间之后,剩余固体的质量为137g,则剩余固体中 与
与 的物质的量之比为
的物质的量之比为| 实验3 |  |  | |||
浓度/ | 0.01 | 0.10 | 0.50 | 0.01 | |
 | 0.01 | 无明显现象 | 有浑浊 | 有浑浊 | 有浑浊 |
| 0.10 | 无明显现象 | 有浑浊 | 有浑浊,有微小气泡 | 有沉淀 | |
| 0.50 | 无明显现象 | 有浑浊 | 有浑浊,有大量气泡 | 有沉淀 | |
已知:
 易溶于水。
易溶于水。(3)
 溶液与
溶液与 溶液混合的现象中,有些只观察到浑浊但没有观察到气体,可能原因是
溶液混合的现象中,有些只观察到浑浊但没有观察到气体,可能原因是(4)写出溶液中
 与
与 反应的离子方程式
反应的离子方程式【反思评价】
(5)根据实验3,鉴别浓度均为0.50
 的
的 和
和 的方法是:分别取等量溶液置于两试管中,
的方法是:分别取等量溶液置于两试管中,
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】“建设生态文明是中华民族永续发展的千年大计。”控制和治理 、
、 是解决光化学烟雾、减少酸雨的有效途径,对构建生态文明有着极为重要的意义。回答下列问题:
是解决光化学烟雾、减少酸雨的有效途径,对构建生态文明有着极为重要的意义。回答下列问题:
(1) 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为_______ 。
(2)NO和 的处理。已除去
的处理。已除去 的硝酸尾气可用NaOH溶液吸收,主要反应如下:
的硝酸尾气可用NaOH溶液吸收,主要反应如下:
 、
、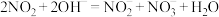
①吸收后的溶液经浓缩、结晶、过滤,得到 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是 ;吸收后排放的尾气中含量较高的氮氧化物是
;吸收后排放的尾气中含量较高的氮氧化物是_______ (填化学式)。
②Cu与适量浓硝酸反应生成0.9mol氮的氧化物(NO、 、
、 ),这些氧化物恰好能被500mL2mol⋅L-1NaOH溶液完全吸收,得到
),这些氧化物恰好能被500mL2mol⋅L-1NaOH溶液完全吸收,得到 和
和 的混合溶液,若参加反应的铜为51.2g,则生成
的混合溶液,若参加反应的铜为51.2g,则生成_______ mol 。
。
③在100mL稀 和稀
和稀 组成的混合溶液中,两种酸的物质的量浓度之和为0.4mol·L-1.向该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中
组成的混合溶液中,两种酸的物质的量浓度之和为0.4mol·L-1.向该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中 的物质的量浓度最大值为
的物质的量浓度最大值为_______ (反应前后溶液体积变化忽略不计)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。 和
和 ,其离子方程式为
,其离子方程式为_______ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是_______ 。
(4)吸收工厂烟气中的 ,能有效减少
,能有效减少 对空气的污染。
对空气的污染。
①富氧煅烧燃煤产生的低浓度的 可以在炉内添加
可以在炉内添加 通过以下方式脱除:
通过以下方式脱除:_______ 。
②氨水吸收 。当通入
。当通入 至溶液
至溶液 左右时,主要反应的离子方程式为
左右时,主要反应的离子方程式为_______ 。
已知:溶液中 、
、 ,
, 的物质的量分数随pH的分布如图所示。
的物质的量分数随pH的分布如图所示。
 、
、 是解决光化学烟雾、减少酸雨的有效途径,对构建生态文明有着极为重要的意义。回答下列问题:
是解决光化学烟雾、减少酸雨的有效途径,对构建生态文明有着极为重要的意义。回答下列问题:(1)
 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为(2)NO和
 的处理。已除去
的处理。已除去 的硝酸尾气可用NaOH溶液吸收,主要反应如下:
的硝酸尾气可用NaOH溶液吸收,主要反应如下: 、
、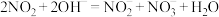
①吸收后的溶液经浓缩、结晶、过滤,得到
 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是 ;吸收后排放的尾气中含量较高的氮氧化物是
;吸收后排放的尾气中含量较高的氮氧化物是②Cu与适量浓硝酸反应生成0.9mol氮的氧化物(NO、
 、
、 ),这些氧化物恰好能被500mL2mol⋅L-1NaOH溶液完全吸收,得到
),这些氧化物恰好能被500mL2mol⋅L-1NaOH溶液完全吸收,得到 和
和 的混合溶液,若参加反应的铜为51.2g,则生成
的混合溶液,若参加反应的铜为51.2g,则生成 。
。③在100mL稀
 和稀
和稀 组成的混合溶液中,两种酸的物质的量浓度之和为0.4mol·L-1.向该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中
组成的混合溶液中,两种酸的物质的量浓度之和为0.4mol·L-1.向该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中 的物质的量浓度最大值为
的物质的量浓度最大值为(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。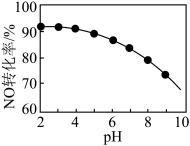
 和
和 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高。其原因是
(4)吸收工厂烟气中的
 ,能有效减少
,能有效减少 对空气的污染。
对空气的污染。①富氧煅烧燃煤产生的低浓度的
 可以在炉内添加
可以在炉内添加 通过以下方式脱除:
通过以下方式脱除: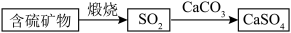
②氨水吸收
 。当通入
。当通入 至溶液
至溶液 左右时,主要反应的离子方程式为
左右时,主要反应的离子方程式为已知:溶液中
 、
、 ,
, 的物质的量分数随pH的分布如图所示。
的物质的量分数随pH的分布如图所示。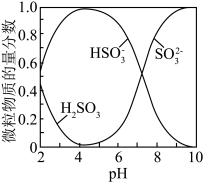
您最近一年使用:0次
【推荐3】磷酸锌[Zn3(PO4)2]在水中几乎不溶,其在水中的溶解度随温度的升高而降低,常用作氯化橡胶合成高分子材料的阻燃剂。工业上利用烧渣灰(主要含ZnO,还含少量FeO、Al2O3、CuO及SiO2等)为原料制取磷酸锌的工艺流程如图所示:
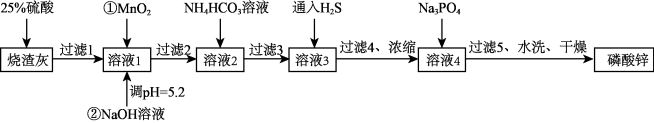
已知:Ⅰ.加入NH4HCO3溶液的目的是沉锰。
Ⅱ.几种金属离子开始沉淀与沉淀完全的pH如下表所示:
(1)用硫酸酸浸烧渣灰,为提高酸浸时锌的浸出率,可以采取的措施是_______ (填一条)。
(2)加入MnO2发生反应的离子方程式是_______ ;经过滤2得到的滤渣的主要成分是_______ (填化学式)。
(3)沉锰反应的离子方程式是_______ 。
(4)水洗时,用热水洗涤磷酸锌沉淀比用冷水洗涤损耗更少,说明原因:_______ 。
(5)通入H2S是为了除铜离子,25℃时,当通入H2S达到饱和时测得溶液的pH = 1,c(H2S)=0.1 mol·L-1,此时溶液中c(Cu2+) =6×10-17 mol·L-1,则CuS的溶度积Ksp=_______ [已知:25℃时,H2S的电离平衡常数Ka1=1×10-7,Ka2=1×10-15]。
(6)利用膜技术电解经净化的含磷酸钠的废液,可以得到所需的工业产品磷酸和氢氧化钠等,电解装置如图所示:

则M为电源的_______ (填“正极”或“负极”),d为_______ (填“阴”或“阳”)离子交换膜,电解总反应式为_______ 。

已知:Ⅰ.加入NH4HCO3溶液的目的是沉锰。
Ⅱ.几种金属离子开始沉淀与沉淀完全的pH如下表所示:
| 金属离子 | Al3+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀的pH | 3.0 | 2.2 | 5.4 | 6.5 |
| 沉淀完全的pH | 5.0 | 3.6 | 6.7 | 8.5 |
(2)加入MnO2发生反应的离子方程式是
(3)沉锰反应的离子方程式是
(4)水洗时,用热水洗涤磷酸锌沉淀比用冷水洗涤损耗更少,说明原因:
(5)通入H2S是为了除铜离子,25℃时,当通入H2S达到饱和时测得溶液的pH = 1,c(H2S)=0.1 mol·L-1,此时溶液中c(Cu2+) =6×10-17 mol·L-1,则CuS的溶度积Ksp=
(6)利用膜技术电解经净化的含磷酸钠的废液,可以得到所需的工业产品磷酸和氢氧化钠等,电解装置如图所示:

则M为电源的
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】实验室以工业废渣(主要含 ,还含少量
,还含少量 、
、 、
、 )为原料制取轻
)为原料制取轻 和
和 晶体,其实验流程如下:
晶体,其实验流程如下:

(1)室温下,反应 达到平衡,则溶液中
达到平衡,则溶液中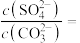
_______ [ ,
,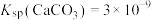 ]。
]。
(2)将氨水和 溶液混合,可制得
溶液混合,可制得 溶液,其离子方程式为
溶液,其离子方程式为_______ 。浸取废渣时,向 溶液中加入适量浓氨水的目的是
溶液中加入适量浓氨水的目的是_______ 。
(3)废渣浸取在如图所示的装置中进行。控制反应温度在60-70℃,搅拌,反应3小时。温度过高将会导致 的转化率下降,其原因是
的转化率下降,其原因是_______ 。保持温度、反应时间、反应物和溶剂的量不变,实验中提高 转化率的操作有
转化率的操作有_______ 。

(4)滤渣水洗后,经多步处理得到制备轻质 所需的
所需的 溶液。设计以水洗后的滤渣为原料,制取
溶液。设计以水洗后的滤渣为原料,制取 溶液的实验方案:
溶液的实验方案:_______ 。[已知 时
时 和
和 沉淀完全;
沉淀完全; 时
时 开始溶解。实验中必须使用的试剂:盐酸和
开始溶解。实验中必须使用的试剂:盐酸和 ]。
]。
(5)将工业废渣中的铁元素提取,经过一系列步骤,可制备聚合硫酸铁。测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品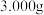 ,置于
,置于 锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的
锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的 溶液(
溶液( 将
将 还原为
还原为 ),充分反应后,除去过量的
),充分反应后,除去过量的 。用
。用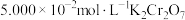 溶液滴定至终点(滴定过程中
溶液滴定至终点(滴定过程中 与
与 反应生成
反应生成 和
和 ),消耗
),消耗 溶液
溶液 。计算该样品中铁的质量分数
。计算该样品中铁的质量分数_______ (保留2位小数,写出计算过程)。
 ,还含少量
,还含少量 、
、 、
、 )为原料制取轻
)为原料制取轻 和
和 晶体,其实验流程如下:
晶体,其实验流程如下:
(1)室温下,反应
 达到平衡,则溶液中
达到平衡,则溶液中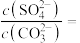
 ,
,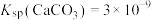 ]。
]。(2)将氨水和
 溶液混合,可制得
溶液混合,可制得 溶液,其离子方程式为
溶液,其离子方程式为 溶液中加入适量浓氨水的目的是
溶液中加入适量浓氨水的目的是(3)废渣浸取在如图所示的装置中进行。控制反应温度在60-70℃,搅拌,反应3小时。温度过高将会导致
 的转化率下降,其原因是
的转化率下降,其原因是 转化率的操作有
转化率的操作有
(4)滤渣水洗后,经多步处理得到制备轻质
 所需的
所需的 溶液。设计以水洗后的滤渣为原料,制取
溶液。设计以水洗后的滤渣为原料,制取 溶液的实验方案:
溶液的实验方案: 时
时 和
和 沉淀完全;
沉淀完全; 时
时 开始溶解。实验中必须使用的试剂:盐酸和
开始溶解。实验中必须使用的试剂:盐酸和 ]。
]。(5)将工业废渣中的铁元素提取,经过一系列步骤,可制备聚合硫酸铁。测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品
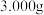 ,置于
,置于 锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的
锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的 溶液(
溶液( 将
将 还原为
还原为 ),充分反应后,除去过量的
),充分反应后,除去过量的 。用
。用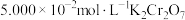 溶液滴定至终点(滴定过程中
溶液滴定至终点(滴定过程中 与
与 反应生成
反应生成 和
和 ),消耗
),消耗 溶液
溶液 。计算该样品中铁的质量分数
。计算该样品中铁的质量分数
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】氟碳铈矿(主要成分为CeFCO3)是提取稀土化合物、冶炼铈的重要矿物原料,根据如图以氟碳铈矿为原料提取铈的工艺流程图,回答问题:

(1)CeFCO3中Ce的化合价为___ ;氧化焙烧时不能使用陶瓷容器,原因是___ 。
(2)氧化焙烧后的产物之一为CeO2,则酸浸时发生反应的离子方程式为___ 。
(3)HT是一种难溶于水的有机溶剂,则操作Ⅰ的名称为___ 。
(4)为了提高酸浸率,可以适当提高反应温度,但发现温度偏高浸出率反而会减小,其原因是___ 。
(5)写出向Ce(OH)3悬浊液中通入氧气得到产品Ce(OH)4的化学方程式:___ 。
(6)298K时,向c(Ce3+)=0.02mol/L的溶液中加入氢氧化钠来调节溶液的pH,若反应后溶液pH=10,此时Ce3+是否沉淀完全?___ (答“是”或“否”)判断的理由是___ 。(要求列式计算,已知:Ksp[Ce(OH)3]=1.0×10-20,c(Ce3+)<1.0×10-5mol/L视为沉淀完全。)

(1)CeFCO3中Ce的化合价为
(2)氧化焙烧后的产物之一为CeO2,则酸浸时发生反应的离子方程式为
(3)HT是一种难溶于水的有机溶剂,则操作Ⅰ的名称为
(4)为了提高酸浸率,可以适当提高反应温度,但发现温度偏高浸出率反而会减小,其原因是
(5)写出向Ce(OH)3悬浊液中通入氧气得到产品Ce(OH)4的化学方程式:
(6)298K时,向c(Ce3+)=0.02mol/L的溶液中加入氢氧化钠来调节溶液的pH,若反应后溶液pH=10,此时Ce3+是否沉淀完全?
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:

(1)气体A中的大气污染物可选用下列试剂中的_______ 吸收。
a.浓H2SO4 b.稀HNO3c.NaOH溶液d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在_______ (填离子符号),检验溶液中还存在Fe2+的方法是_______ (注明试剂、现象)。
(3)已知:Ksp[Fe(OH)3]=1.0×10-38,若所得溶液中只含Fe3+,在溶液中加入一定量的石灰水,调节溶液的pH使Fe3+沉淀完全,此时溶液pH为_______ 。(保留一位小数)
(4)由泡铜冶炼粗铜的化学反应方程式_______ 。
(5)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是_______ 。
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
e.阳极减少的质量与阴极增加的质量相等
(6)利用下列原电池装置可制备CuSO4,其正极电极反应式为_______ 。


(1)气体A中的大气污染物可选用下列试剂中的
a.浓H2SO4 b.稀HNO3c.NaOH溶液d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在
(3)已知:Ksp[Fe(OH)3]=1.0×10-38,若所得溶液中只含Fe3+,在溶液中加入一定量的石灰水,调节溶液的pH使Fe3+沉淀完全,此时溶液pH为
(4)由泡铜冶炼粗铜的化学反应方程式
(5)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
e.阳极减少的质量与阴极增加的质量相等
(6)利用下列原电池装置可制备CuSO4,其正极电极反应式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】实验室用卤块(主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质)制备少量Mg(ClO3)2·6H2O的流程如图:

已知:①四种化合物的溶解度(S)随温度(T)变化曲线如图所示:

②室温时一些物质的Ksp如表所示:
③Mg(ClO3)2有较强的氧化性,其还原产物是Cl-。
回答下列问题:
(1)H2O2的电子式为_______ 。
(2)滤渣的成分是______ (填化学式)。
(3)经测定,D中铁离子的浓度为1×10-5 mol·L-1,则x为________ (已知:lg 5≈0.7)。
(4)D中所发生的化学反应方程式为_______ ,框图中由D→……→制Mg(ClO3)2·6H2O晶体的实验步骤依次为①加热蒸发;②____________ (请补充);③冷却结晶;④过滤洗涤。

已知:①四种化合物的溶解度(S)随温度(T)变化曲线如图所示:

②室温时一些物质的Ksp如表所示:
| 化学式 | Fe(OH)2 | Fe(OH)3 | Mg(OH)2 |
| Ksp | 8.0×10-18 | 8.0×10-38 | 1.8×10-11 |
回答下列问题:
(1)H2O2的电子式为
(2)滤渣的成分是
(3)经测定,D中铁离子的浓度为1×10-5 mol·L-1,则x为
(4)D中所发生的化学反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】兰尼镍是一种带有多孔结构的细小晶粒组成的镍铝合金,被广泛用作有机物的氢化反应的催化剂。以红土镍矿(主要成分为NiS、FeS和SiO2等)为原料制备兰尼镍的工艺流程如下图所示:
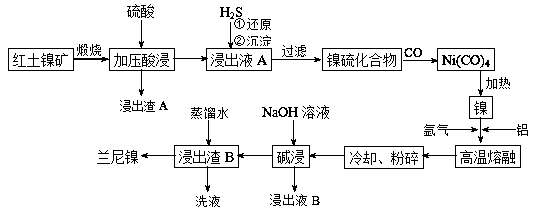
(1)在形成Ni(CO)4的过程中,碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为___________ ;
(2)已知红土镍矿煅烧后生成Ni2O3,而加压酸浸后浸出液A中含有Ni2+,写出有关镍元素的加压酸浸的化学反应方程式______________________ ;
(3)向浸出液A中通入H2S气体,反应的离子方程式是____________________ ;
(4)“高温熔融”时能否将通入氩气换为CO并说明原因_____________________ ;
(5)“碱浸”的目的是使镍铝合金产生多孔结构,从而增强对氢气的强吸附性,此过程
中发生反应的离子方程式为___________________ 。浸出反应所用的NaOH溶液的浓度要大,若NaOH溶液较稀时,则会产生少量的Al(OH)3沉淀而阻止浸出反应的持续进行,请用化学反应原理加以解释:________________________ 。
(6)浸出液B可以回收,重新生成铝以便循环利用。请设计简单的回收流程:
浸出液B→________________________ 。(示例:CuOCu2+Cu)

(1)在形成Ni(CO)4的过程中,碳元素的化合价没有变化,则Ni(CO)4中的Ni的化合价为
(2)已知红土镍矿煅烧后生成Ni2O3,而加压酸浸后浸出液A中含有Ni2+,写出有关镍元素的加压酸浸的化学反应方程式
(3)向浸出液A中通入H2S气体,反应的离子方程式是
(4)“高温熔融”时能否将通入氩气换为CO并说明原因
(5)“碱浸”的目的是使镍铝合金产生多孔结构,从而增强对氢气的强吸附性,此过程
中发生反应的离子方程式为
(6)浸出液B可以回收,重新生成铝以便循环利用。请设计简单的回收流程:
浸出液B→
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】以铬铁矿(主要成分为FeO和Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产化工原料红矾钠(主要成分为Na2Cr2O7·2H2O),其主要工艺流程如图:

查阅资料得知:
ⅰ.Cr2O3可溶于硫酸得到Cr3+;常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO 。
。
ⅱ.
回答下列问题:
(1)反应之前先将矿石粉碎的目的是_______ 。
(2)步骤③加的试剂为_______ ,此时溶液pH要调到4.9~5的目的_______ 。
(3)已知:Ksp[Fe(OH)3]=4.0×10-38。则当调节溶液的pH=3时,溶液中的c(Fe3+)=_______ mol/L 。
(4)配平并补充完成反应④的离子反应方程式:______ 。
_______NaBiO3 + _______Cr3+ + 7OH- + H2O=_______Bi(OH)3+_______CrO +_______Na+
+_______Na+
(5)⑤中酸化是使CrO 转化为Cr2O
转化为Cr2O ,写出该反应的离子方程式:
,写出该反应的离子方程式:_______ 。
(6)将溶液H经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥即得红矾钠粗晶体,精制红矾钠粗晶体需要采用的操作是_______ (填操作名称)。

查阅资料得知:
ⅰ.Cr2O3可溶于硫酸得到Cr3+;常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO
 。
。ⅱ.
| 金属离子 | Fe3+ | Al3+ | Cr3+ | Fe2+ | Bi3+ |
| 开始沉淀的pH | 2.7 | 3.4 | 5.0 | 7.5 | 0.7 |
| 沉淀完全的pH | 3.7 | 4.9 | 5.9 | 9.7 | 4.5 |
回答下列问题:
(1)反应之前先将矿石粉碎的目的是
(2)步骤③加的试剂为
(3)已知:Ksp[Fe(OH)3]=4.0×10-38。则当调节溶液的pH=3时,溶液中的c(Fe3+)=
(4)配平并补充完成反应④的离子反应方程式:
_______NaBiO3 + _______Cr3+ + 7OH- + H2O=_______Bi(OH)3+_______CrO
 +_______Na+
+_______Na+(5)⑤中酸化是使CrO
 转化为Cr2O
转化为Cr2O ,写出该反应的离子方程式:
,写出该反应的离子方程式:(6)将溶液H经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥即得红矾钠粗晶体,精制红矾钠粗晶体需要采用的操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】工业制得的氮化铝(AlN)产品中常含有少量Al4C3、Al2O3、C等杂质。某同学设计如下实验分别测定氮化铝(AlN)样品中AlN和Al4C3的质量分数(忽略NH3在强碱性溶液中的溶解)。
(1)实验原理:
①Al4C3与硫酸反应可生成CH4
②AlN溶于强酸产生铵盐,溶于强碱生成氨气,请写出AlN与过量NaOH溶液反应的化学方程式____ 。
(2)实验装置(如图所示,量气管为碱式滴定管改装)

连好装置后,首先应进行的操作是__________ 。
(3)实验过程:称得装置D的初始质量为yg;称取xgAlN样品置于装置B锥形瓶中,各装置中加入相应药品,重新连好装置;读取量气管的初始读数为amL(量气装置左右液面相平)。
①欲首先测量Al4C3质量分数的有关数据,对三个活塞的操作是: 关闭活塞___ ,打开活塞___
②若无恒压管,对所测气体体积的影响是____ (填“偏大”“偏小”或“无影响”)
③量气管中液面不再发生变化,说明反应已经结束。读取读数之前,应对量气管进行的操作为,首先恢复至室温,然后____ ;若量气管中的液面高于A右侧干燥管中的液面,所测气体的体积___ (填“偏大”“偏小”或“无影响”)。
④记录滴定管的读数为bmL(已知:该实验条件下的气体摩尔体积为VmL·mol-1),则Al4C3的质量分数为____ (用含a、b、x、Vm的代数式表示)。
⑤测量AlN质量分数的数据:首先关闭活塞K1,打开活塞K3,通过分液漏斗加入____ ,与装置B瓶内物质充分反应;反应完成后,____ (填入该步应进行的操作),最后称得装置D的质量为zg。则样品中AlN的质量分数为____ (用含x、y、z、的代数式表示)。
(1)实验原理:
①Al4C3与硫酸反应可生成CH4
②AlN溶于强酸产生铵盐,溶于强碱生成氨气,请写出AlN与过量NaOH溶液反应的化学方程式
(2)实验装置(如图所示,量气管为碱式滴定管改装)

连好装置后,首先应进行的操作是
(3)实验过程:称得装置D的初始质量为yg;称取xgAlN样品置于装置B锥形瓶中,各装置中加入相应药品,重新连好装置;读取量气管的初始读数为amL(量气装置左右液面相平)。
①欲首先测量Al4C3质量分数的有关数据,对三个活塞的操作是: 关闭活塞
②若无恒压管,对所测气体体积的影响是
③量气管中液面不再发生变化,说明反应已经结束。读取读数之前,应对量气管进行的操作为,首先恢复至室温,然后
④记录滴定管的读数为bmL(已知:该实验条件下的气体摩尔体积为VmL·mol-1),则Al4C3的质量分数为
⑤测量AlN质量分数的数据:首先关闭活塞K1,打开活塞K3,通过分液漏斗加入
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】铜转炉烟灰主要含有Zn[还有少量的Fe(+2价)、Pb、Cu、As等元素]的硫酸盐和氧化物,少量为砷酸盐。制备重要化工原料活性氧化锌的工艺流程如图所示。请回答以下问题:
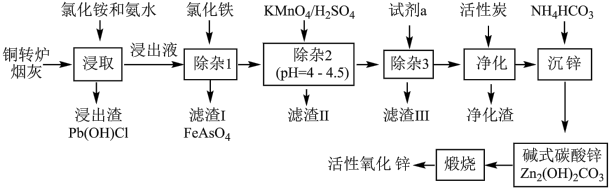
已知:活性炭净化主要是除去有机杂质。
(1)写出氯化铵的电子式___ ,“净化”过程属于___ (填“物理”、“化学”)变化。
(2)在反应温度为50℃,反应时间为1h时,测定各元素的浸出率与氯化铵溶液浓度的关系如图,则氯化铵适宜的浓度为___ mol·L-1。若浸出液中锌元素以[Zn(NH3)4]2+形式存在,则浸取时ZnO发生反应的离子方程式为___ 。

(3)滴加KMnO4溶液有MnO2生成,目的是除___ 元素,除杂3是置换除杂过程,则试剂a是___ ,“滤渣Ⅲ”的主要成分为___ (填化学式)。
(4)写出“沉锌”时发生反应的离子方程式___ ,此过程中可以循环利用的副产品是___ 。
(5)取mg活性氧化锌样品配成待测液,加入指示剂3、4滴,再加入适量六亚甲基四胺,用amol•L-1EDTA标准液进行滴定,消耗标准液VmL。已知:与1.0mLEDTA标准液[c(EDTA)=1.000mol•L-1]相当的以克表示的氧化锌质量为0.08139,则样品中氧化锌的质量分数为___ (用代数式表示)。

已知:活性炭净化主要是除去有机杂质。
(1)写出氯化铵的电子式
(2)在反应温度为50℃,反应时间为1h时,测定各元素的浸出率与氯化铵溶液浓度的关系如图,则氯化铵适宜的浓度为

(3)滴加KMnO4溶液有MnO2生成,目的是除
(4)写出“沉锌”时发生反应的离子方程式
(5)取mg活性氧化锌样品配成待测液,加入指示剂3、4滴,再加入适量六亚甲基四胺,用amol•L-1EDTA标准液进行滴定,消耗标准液VmL。已知:与1.0mLEDTA标准液[c(EDTA)=1.000mol•L-1]相当的以克表示的氧化锌质量为0.08139,则样品中氧化锌的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】亚硝酰氯(ClNO)是有机物合成中的重要试剂,为红褐色液体或黄色气体,具有刺鼻恶臭味、遇水反应生成一种氯化物和两种氮化物。某学习小组在实验空用Cl2和NO制备ClNO并测定其纯度,相关实验装置(夹持装置略去)如下图所示。请回答:

(1)制备C12发生装置可以选用____ (填写字母代号),请写出发生反应的离子方程式:____________ 。
(2)欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a→_______ (按气流方向,用小写字母表示)。
(3)实验室可用下图装置制备亚硝酰氯(C1NO):

①实验室也可用B装置制备NO,X装置的优点为__________ 。
②检验装置气密性并装入药品,打开K2,然后再打开K1,通入一段时间气体,其目的为_______ ,然后进行其他操作,当Z有一定量液体生成时,停止实验。
③若无装置Y,则Z中C1NO可能发生反应的化学方程式为________ 。
(4)取Z中所得液体mg溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用cmol•L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL。则亚硝酰氯(C1NO)的质量分数为______ (用代数式表示)。[已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(K2CrO4)=1×10-12]

(1)制备C12发生装置可以选用
(2)欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a→
(3)实验室可用下图装置制备亚硝酰氯(C1NO):

①实验室也可用B装置制备NO,X装置的优点为
②检验装置气密性并装入药品,打开K2,然后再打开K1,通入一段时间气体,其目的为
③若无装置Y,则Z中C1NO可能发生反应的化学方程式为
(4)取Z中所得液体mg溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用cmol•L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL。则亚硝酰氯(C1NO)的质量分数为
您最近一年使用:0次



