硅是重要的半导体材料,构成了现代电子工业的基础。回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号________________ ,该能层具有的原子轨道数为________________ 、电子数为________________ 。
(2)硅主要以硅酸盐、________________ 等化合物的形式存在于地壳中。
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以________________ 相结合,其晶胞中共有8个原子,其中在面心位置贡献________________ 个原子。
(4)单质硅可通过甲硅烷(SiH4) 分解反应来制备。工业上采用Mg2Si和NH4CI在液氨介质中反应制得SiH4,该反应的化学方程式为________________ 。
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是___________ SiH4的稳定性小于CH4,更易生成氧化物,原因是 ________________ 。
(6)在硅酸盐中,SiO44+四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根;其中Si原子的杂化形式为________________ 。Si与O的原子数之比为 ________________ 化学式为________ .

(1)基态Si原子中,电子占据的最高能层符号
(2)硅主要以硅酸盐、
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以
(4)单质硅可通过甲硅烷(SiH4) 分解反应来制备。工业上采用Mg2Si和NH4CI在液氨介质中反应制得SiH4,该反应的化学方程式为
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
| 化学键 | C-C | C-H | C-O | Si-Si | Si-H | Si-O |
| 键能/(kJ/mol) | 356 | 413 | 336 | 226 | 318 | 452 |
(6)在硅酸盐中,SiO44+四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根;其中Si原子的杂化形式为

更新时间:2020-02-24 21:26:28
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】请回答下列问题。
(1)①写出 的俗名:
的俗名:________ ;②写出熟石膏的化学式:_________ 。
(2)写出铜和稀硝酸反应的离子方程式__________ 。
(3)检验 溶液中
溶液中 的实验方法
的实验方法___________ 。
(1)①写出
 的俗名:
的俗名:(2)写出铜和稀硝酸反应的离子方程式
(3)检验
 溶液中
溶液中 的实验方法
的实验方法
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Si是现代社会半导体工业发展的基石。回答下列问题:
(1)硅元素在自然界中的存在形式有___________ (填字母)。
A.游离态 B.化合态 C.游离态和化合态都有
(2) 可通过
可通过 与纯碱混合高温熔融反应制得,高温熔融纯碱时,下列坩埚可选用的是___________(填字母)。
与纯碱混合高温熔融反应制得,高温熔融纯碱时,下列坩埚可选用的是___________(填字母)。
(3)制备硅半导体材料必须先得到高纯硅,三氯甲硅烷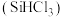 还原法是当前制备高纯硅的主要方法,生产过程示意图如图:
还原法是当前制备高纯硅的主要方法,生产过程示意图如图:
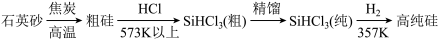
①写出由石英砂制备粗硅的化学反应方程式:___________ 。
②写出由纯 制备高纯硅的化学反应方程式:
制备高纯硅的化学反应方程式:___________ 。
(1)硅元素在自然界中的存在形式有
A.游离态 B.化合态 C.游离态和化合态都有
(2)
 可通过
可通过 与纯碱混合高温熔融反应制得,高温熔融纯碱时,下列坩埚可选用的是___________(填字母)。
与纯碱混合高温熔融反应制得,高温熔融纯碱时,下列坩埚可选用的是___________(填字母)。| A.普通玻璃坩埚 | B.石英玻璃坩埚 | C.氧化铝坩埚 | D.铁坩埚 |
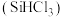 还原法是当前制备高纯硅的主要方法,生产过程示意图如图:
还原法是当前制备高纯硅的主要方法,生产过程示意图如图: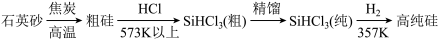
①写出由石英砂制备粗硅的化学反应方程式:
②写出由纯
 制备高纯硅的化学反应方程式:
制备高纯硅的化学反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化合物A是制玻璃的主要原料之一。常温下,化合物B、H、I为气体,B不溶于水,H、I易溶于水,H的水溶液呈碱性,I的水溶液呈酸性。D元素是地壳中含量仅次于氧的非金属元素。化合物J是一种可用于制造发动机的新型无机非金属材料,其相对分子质量为140,其中D元素的质量分数为60%。上述物质间的转化关系如下图所示。
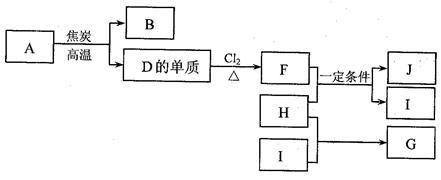
(1)除A外,制玻璃的主要原料还有物质(填化学式)_______ 、_______ 。
盛放NaOH溶液的试剂瓶不能用玻璃塞,原因是(用化学方程式表示)_______ 。
(2)D元素在元素周期表中的位置是___________ 。
(3)H的电子式是_________ 。
(4)F和H反应生成J和I反应的化学方程式是___________ 。
(5)下列说法正确的是(填选项序号)______ 。
a.上述由A生成D的单质的反应属于置换反应
b. D元素在自然界中主要以单质形式存在
c. G是含有极性共价键的离子化合物
d. I是强电解质,G是弱电解质,二者的水溶液都显酸性

(1)除A外,制玻璃的主要原料还有物质(填化学式)
盛放NaOH溶液的试剂瓶不能用玻璃塞,原因是(用化学方程式表示)
(2)D元素在元素周期表中的位置是
(3)H的电子式是
(4)F和H反应生成J和I反应的化学方程式是
(5)下列说法正确的是(填选项序号)
a.上述由A生成D的单质的反应属于置换反应
b. D元素在自然界中主要以单质形式存在
c. G是含有极性共价键的离子化合物
d. I是强电解质,G是弱电解质,二者的水溶液都显酸性
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】量子化学计算预测未知化合物是现代化学发展的途径之一。2016 年2月有人通过计算预言铁也存在四氧化物,其分子构型是四面体,但该分子中铁的氧化态是+6而不是+8。
(1)写出该分子中铁的价电子组态____ 。
(2)画出该分子结构的示意图(用元素符号表示原子,用短线表示原子间的化学键)____ 。
(1)写出该分子中铁的价电子组态
(2)画出该分子结构的示意图(用元素符号表示原子,用短线表示原子间的化学键)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】有机物种类繁多,应用广泛。
(1)邻氨基吡啶(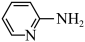 )的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为
)的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为______ (填元素符号)。1mol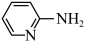 中含有σ键的数目为
中含有σ键的数目为______ mol。
(2)一种鸟嘌呤和吡咯的结构如图。
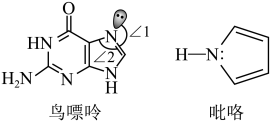
①鸟嘌呤中轨道之间的夹角∠1______ ∠2(填“>”或“<”)。
②分子中的大π键可以用符号π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为______ 。
(3)超分子化学已逐渐扩展到化学的各个领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。
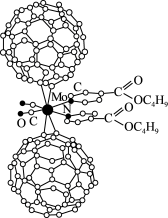
①Mo处于第五周期第VIB族,价电子排布与Cr相似,它的基态价电子排布式是______ ,该超分子中存在的化学键类型有______ (填选项字母)。
A.离子键 B.氢键 C.σ键 D.π键
②该超分子中,配体CO提供孤电子对的原子是______ (填元素符号),p-甲酸丁酯吡啶配体中C原子的杂化方式有_______ 。
(1)邻氨基吡啶(
 )的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为
)的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为 中含有σ键的数目为
中含有σ键的数目为(2)一种鸟嘌呤和吡咯的结构如图。

①鸟嘌呤中轨道之间的夹角∠1
②分子中的大π键可以用符号π
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为(3)超分子化学已逐渐扩展到化学的各个领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。

①Mo处于第五周期第VIB族,价电子排布与Cr相似,它的基态价电子排布式是
A.离子键 B.氢键 C.σ键 D.π键
②该超分子中,配体CO提供孤电子对的原子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如表是元素周期表的一部分。表中所列的字母分别代表一种化学元素:
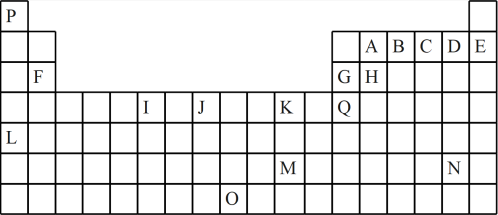
(1)I的最高化合价为____ ;K的元素名称为____ 。
(2)基态时G元素原子的电子排布式___ ,J元素原子的外围电子排布式___ 。
(3)下列对比正确的是___ 。
a.原子半径H>G>B>A b.第一电离能E>D>C>B
c.电负性A>H>G>Q d.最高价氧化物的水化物酸性B>A>H>G
(4)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述不正确的是____ 。
a.L位于元素周期表中第5周期ⅠA族,属于s区元素
b. O位于元素周期表中第7周期ⅧB族,属于d区元素
c.M的外围电子排布式为6s1,属于ds区元素
d.H所在族的外围电子排布式为ns2np2,属于p区元素
(5)元素B和C的气态氢化物热稳定性较强的是____ (填化学式)。

(1)I的最高化合价为
(2)基态时G元素原子的电子排布式
(3)下列对比正确的是
a.原子半径H>G>B>A b.第一电离能E>D>C>B
c.电负性A>H>G>Q d.最高价氧化物的水化物酸性B>A>H>G
(4)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述不正确的是
a.L位于元素周期表中第5周期ⅠA族,属于s区元素
b. O位于元素周期表中第7周期ⅧB族,属于d区元素
c.M的外围电子排布式为6s1,属于ds区元素
d.H所在族的外围电子排布式为ns2np2,属于p区元素
(5)元素B和C的气态氢化物热稳定性较强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求填空:
(1)在下列物质中:①NH3、②HC≡CH、③NaOH、④O2、⑤溴化铵(用序号填空)
其中只含有非极性键的是___________ ;只含有极性键的是___________ ;含有离子键、共价键、配位键的是___________ ;
(2)A的原子的2p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子价电子的轨道表示式:___________ 。
(3)N≡N的键能为942 kJ•mol﹣1,N﹣N单键的键能为247 kJ•mol﹣1,通过计算说明N2中的______ 键更稳定(填“σ”或“π”)。
(4)在①苯;②CH3OH;③HCHO;④CS2;⑤CCl4五种溶剂中,碳原子采取sp2杂化的分子有___________ (填序号),CS2分子的空间结构是___________ ,CO2与CS2相比,___________ (填化学式)的熔点较高。
(5)苯胺(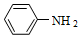 )与甲苯的相对分子质量相近,但苯胺的熔点(﹣5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(﹣950℃)沸点(110.6℃),原因是
)与甲苯的相对分子质量相近,但苯胺的熔点(﹣5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(﹣950℃)沸点(110.6℃),原因是___________ 。
(1)在下列物质中:①NH3、②HC≡CH、③NaOH、④O2、⑤溴化铵(用序号填空)
其中只含有非极性键的是
(2)A的原子的2p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子价电子的轨道表示式:
(3)N≡N的键能为942 kJ•mol﹣1,N﹣N单键的键能为247 kJ•mol﹣1,通过计算说明N2中的
(4)在①苯;②CH3OH;③HCHO;④CS2;⑤CCl4五种溶剂中,碳原子采取sp2杂化的分子有
(5)苯胺(
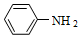 )与甲苯的相对分子质量相近,但苯胺的熔点(﹣5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(﹣950℃)沸点(110.6℃),原因是
)与甲苯的相对分子质量相近,但苯胺的熔点(﹣5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(﹣950℃)沸点(110.6℃),原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮、氟及其化合物在生产及生活中有着广泛的用途。请回答下列问题:
(1)氟磷灰石可用于制取磷肥,基态P原子有___________ 个未成对电子, 的中心P原子的杂化方式为
的中心P原子的杂化方式为___________ 。
(2)氟气可以用于制取惰性强于 的保护气
的保护气 ,也可以用于制取聚合反应的催化剂
,也可以用于制取聚合反应的催化剂 ,
, 可以作为工业制取硅单质的中间物质(
可以作为工业制取硅单质的中间物质( )的原料。
)的原料。
① 分子的空间结构为
分子的空间结构为___________ 。
②S、P、Si的第一电离能由大到小的顺序为___________ 。
(3)Na与N形成的 可用于汽车的安全气囊中,其中阴离子的空间结构为
可用于汽车的安全气囊中,其中阴离子的空间结构为___________ 。
(4)键角比较:
___________  (填“>”或“<”),其原因为
(填“>”或“<”),其原因为___________ 。
(1)氟磷灰石可用于制取磷肥,基态P原子有
 的中心P原子的杂化方式为
的中心P原子的杂化方式为(2)氟气可以用于制取惰性强于
 的保护气
的保护气 ,也可以用于制取聚合反应的催化剂
,也可以用于制取聚合反应的催化剂 ,
, 可以作为工业制取硅单质的中间物质(
可以作为工业制取硅单质的中间物质( )的原料。
)的原料。①
 分子的空间结构为
分子的空间结构为②S、P、Si的第一电离能由大到小的顺序为
(3)Na与N形成的
 可用于汽车的安全气囊中,其中阴离子的空间结构为
可用于汽车的安全气囊中,其中阴离子的空间结构为(4)键角比较:

 (填“>”或“<”),其原因为
(填“>”或“<”),其原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
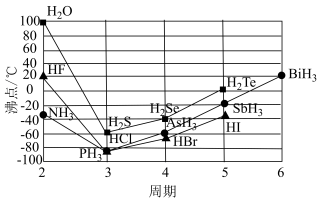
【推荐3】下图为第ⅤA族、ⅥA、ⅦA族元素简单氢化物沸点随周期数的递变趋势图。
(1)解释第ⅤA族元素氢化物沸点变化的趋势:___________ ,推测ⅣA族 与
与 的沸点大小为
的沸点大小为
___________  (填“>”或“<”)。
(填“>”或“<”)。
(2)接近水的沸点的水蒸气的相对分子质量测定值比按化学式 计算出的相对分子质量大一些,原因为
计算出的相对分子质量大一些,原因为___________ 。
(3) 常用于制备半导体材料,
常用于制备半导体材料, 与足量的
与足量的 加热可反应得到
加热可反应得到 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。通过___________ 的实验分析方法可测出 的键长键角信息,下列关于
的键长键角信息,下列关于 分子的说法正确的是
分子的说法正确的是___________ 。
A.中心原子价层电子对数为5对
B.分子的空间构型为正四面体
C.中心原子的杂化方式为 杂化
杂化
(1)解释第ⅤA族元素氢化物沸点变化的趋势:
 与
与 的沸点大小为
的沸点大小为
 (填“>”或“<”)。
(填“>”或“<”)。(2)接近水的沸点的水蒸气的相对分子质量测定值比按化学式
 计算出的相对分子质量大一些,原因为
计算出的相对分子质量大一些,原因为(3)
 常用于制备半导体材料,
常用于制备半导体材料, 与足量的
与足量的 加热可反应得到
加热可反应得到 ,写出该反应的化学方程式
,写出该反应的化学方程式 的键长键角信息,下列关于
的键长键角信息,下列关于 分子的说法正确的是
分子的说法正确的是A.中心原子价层电子对数为5对
B.分子的空间构型为正四面体
C.中心原子的杂化方式为
 杂化
杂化
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】X、Y、Z、W是元素周期表前四周期中原子序数依次增大的四种常见元素,基态X原子核外有2个未成对电子,基态Z原子最外层电子排布式为nsnnpn+2,W的核电荷数等于X与Y的核电荷数之和的2倍。
(1)Z在元素周期表中的位置为________ ,W的元素基态原子的电子排布式是________ 。
(2)X、Y、Z三种元素的第一电离能的大小顺序为________ (用元素符号表示,下同);H-X、 H-Y、H-Z三种共价键中,键长最长的是_________ 。
(3)Y的最简单氢化物的空间构型是_________ 。
(4)CH3+、—CH3(甲基)、CH3-都是重要的有机反应中间体,有关它们的说法正确的是________ 。
A.它们均由甲烷去掉一个氢原子所得
B.它们互为等电子体,碳原子均采取sp2杂化
C.CH3-与NH3、H3O+互为等电子体,几何构型均为三角锥形
D.CH3+中的碳原子采取sp2杂化,所有原子均共面
E.两个—CH3(甲基)或一个CH3+和一个CH3-结合均可得到CH3CH3
(1)Z在元素周期表中的位置为
(2)X、Y、Z三种元素的第一电离能的大小顺序为
(3)Y的最简单氢化物的空间构型是
(4)CH3+、—CH3(甲基)、CH3-都是重要的有机反应中间体,有关它们的说法正确的是
A.它们均由甲烷去掉一个氢原子所得
B.它们互为等电子体,碳原子均采取sp2杂化
C.CH3-与NH3、H3O+互为等电子体,几何构型均为三角锥形
D.CH3+中的碳原子采取sp2杂化,所有原子均共面
E.两个—CH3(甲基)或一个CH3+和一个CH3-结合均可得到CH3CH3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=___ 。与CO互为等电子体的离子是_____ (至少写两种)
(2)甲醛(H2C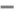 O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醇分子内O原子的杂化方式为
O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醇分子内O原子的杂化方式为___ ,甲醇分子内的O—C—H键角___ (填“大于”“等于”或“小于”)甲醛分子内的O—C—H键角。
(3)已知高碘酸有两种形式,化学式分别为H5IO6和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6________ (填“>”“<”或“=”)HIO4。
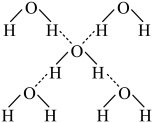
(4)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图),已知冰的升华热是+51 kJ·mol-1,除氢键外,水分子间还存在范德华力(11 kJ·mol-1),则冰晶体中氢键的键能是________ kJ·mol-1。
(2)甲醛(H2C
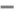 O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醇分子内O原子的杂化方式为
O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醇分子内O原子的杂化方式为(3)已知高碘酸有两种形式,化学式分别为H5IO6和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6

(4)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图),已知冰的升华热是+51 kJ·mol-1,除氢键外,水分子间还存在范德华力(11 kJ·mol-1),则冰晶体中氢键的键能是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】毒奶粉中发现的化工原料三聚氰胺可以由下列反应合成:CaO+3C CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2 CaCN2+C,CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CaCN2+C,CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)基态钙原子电子占据的最高能层符号是_________ ,其核外共有______ 种不同能量的电子。
(2)CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O,由此可以推知CN22-的空间构型为________ 。
(3)1mol 尿素分子[CO(NH2)2]中含有的π键与σ键的数目之比为_________ ;所含元素的电负性由大到小的顺序为_____________ 。
(4)三聚氰胺俗称“蛋白精”,其结构为:

其中氮原子的杂化方式为________ 。
 CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2 CaCN2+C,CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CaCN2+C,CaCN2+2H2O=NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。(1)基态钙原子电子占据的最高能层符号是
(2)CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O,由此可以推知CN22-的空间构型为
(3)1mol 尿素分子[CO(NH2)2]中含有的π键与σ键的数目之比为
(4)三聚氰胺俗称“蛋白精”,其结构为:

其中氮原子的杂化方式为
您最近一年使用:0次



