氢、氮、氯、铜是元素周期表中前四周期元素。回答下列问题:
(1)铜在元素周期表中的位置__ ,写出NH3的电子式__ 。
(2)氯与硫相比,非金属性较强的是__ (用元素符号表示),下列事实能证明这一结论的是__ 。(填序号)。
a.常温下氯的单质呈气态,硫的单质呈固态
b.稳定性:HCl>H2S
c.酸性:HClO4>H2SO4
d.氯的电负性大于硫的电负性
(3)含氮化合物(CH3)3N与盐酸反应,离子方程式为:(CH3)3N+H+=[(CH3)3NH]+,该反应过程中新生成的化学键为___ (填序号)。
a.离子键 b.配位键 c.氢键 d.非极性共价键
若化合物(CH3)3N能溶于水,其可能的原因是___ 。
(4)Cu与H元素形成某种晶体的结构如图所示,则该晶体的化学式为__ ,若该晶体的密度为ρ g•cm-3,阿伏加 德罗常数的值为NA,则该晶胞的棱长为__ nm(用含ρ和NA的式子表示,已知1nm=10-7cm)。

(1)铜在元素周期表中的位置
(2)氯与硫相比,非金属性较强的是
a.常温下氯的单质呈气态,硫的单质呈固态
b.稳定性:HCl>H2S
c.酸性:HClO4>H2SO4
d.氯的电负性大于硫的电负性
(3)含氮化合物(CH3)3N与盐酸反应,离子方程式为:(CH3)3N+H+=[(CH3)3NH]+,该反应过程中新生成的化学键为
a.离子键 b.配位键 c.氢键 d.非极性共价键
若化合物(CH3)3N能溶于水,其可能的原因是
(4)Cu与H元素形成某种晶体的结构如图所示,则该晶体的化学式为

更新时间:2020-02-26 22:07:29
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,表中序号分别代表某一元素。请回答下列问题:
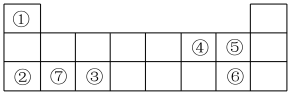
(1)⑥在元素周期表中的位置是___________ 。
(2)④的离子结构示意图为___________ 。
(3)②③④⑥四种元素的简单离子半径由小到大的顺序为___________ (用离子符号表示)。
(4)①④形成的既含极性键又含非极性键的共价化合物的电子式为___________ 。
(5)用电子式表示②④只含有离子键的化合物的形成过程___________ 。
(6)②③⑦最高价氧化物对应的水化物的碱性由强到弱的顺序为___________ (写化学式),⑤和⑥形成的气态氢化物,稳定性较弱的是___________ (写化学式)。
(7)单质②与元素④的简单氢化物反应的离子方程式为___________ 。

(1)⑥在元素周期表中的位置是
(2)④的离子结构示意图为
(3)②③④⑥四种元素的简单离子半径由小到大的顺序为
(4)①④形成的既含极性键又含非极性键的共价化合物的电子式为
(5)用电子式表示②④只含有离子键的化合物的形成过程
(6)②③⑦最高价氧化物对应的水化物的碱性由强到弱的顺序为
(7)单质②与元素④的简单氢化物反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下图是元素周期表的一部分。根据图中标注的9种元素,用化学符号填写下列空格:
以上9种元素中,
(1)单质的化学性质最不活泼的元素是_______ ;常温下,会在浓硫酸中发生钝化的金属是_______ 。
(2)金属性最强的元素是_______ 非金属性最强的元素是_______ 。
(3)最高价氧化物对应的水化物,碱性最强的是_______ ,酸性最强的是_______ 。
(4)②的原子结构示意图是_______ 。
(5)①的最高价氧化物的电子式是_______ ,其所含化学键类型为_______ (填“极性键”或“非极性键”)。
(6)⑧和⑨分别形成的最简单氢化物更稳定的是_______ 。
(7)⑤的最高价氧化物形成的水化物与⑦的最高价氧化物反应的离子方程式为_______ 。
(8)用电子式表示⑥的氯化物的形成过程_______ 。
| 族 周期 | IA | 0 | |||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | ④ | ||
| 2 | ① | ② | ③ | ||||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)单质的化学性质最不活泼的元素是
(2)金属性最强的元素是
(3)最高价氧化物对应的水化物,碱性最强的是
(4)②的原子结构示意图是
(5)①的最高价氧化物的电子式是
(6)⑧和⑨分别形成的最简单氢化物更稳定的是
(7)⑤的最高价氧化物形成的水化物与⑦的最高价氧化物反应的离子方程式为
(8)用电子式表示⑥的氯化物的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】如表是元素周期表主族元素的一部分,请参照元素①~⑥在表中的位置,回答下列问题:

(1)②在周期表中的位置______ 。
(2)①的简单氢化物的电子式______ 。
(3)③④⑤形成的简单离子半径由大到小的排序是______ (用离子符号表示)。
(4)用电子式表示③和⑥形成的化合物的过程______ 。
(5)写出⑤单质与③的最高价氧化物对应水化物反应的离子方程式______ 。
(6)③和④中金属性强的是______ (填“元素符号”),以下说法能证明该结论的是______ 。
a.③容易失去1个e-,而④容易失去2个e-
b.③与冷水剧烈反应,而④与冷水反应缓慢
c.③和④的最高价氧化物对应水化物的碱性:③>④
(7)硒(Se)位于第四周期,与②同主族。下列推断不正确 的是______ 。
a.Se最低价为-2价
b.Se单质常温下也呈气态,只有氧化性
c.沸点:H2Se<H2O

(1)②在周期表中的位置
(2)①的简单氢化物的电子式
(3)③④⑤形成的简单离子半径由大到小的排序是
(4)用电子式表示③和⑥形成的化合物的过程
(5)写出⑤单质与③的最高价氧化物对应水化物反应的离子方程式
(6)③和④中金属性强的是
a.③容易失去1个e-,而④容易失去2个e-
b.③与冷水剧烈反应,而④与冷水反应缓慢
c.③和④的最高价氧化物对应水化物的碱性:③>④
(7)硒(Se)位于第四周期,与②同主族。下列推断
a.Se最低价为-2价
b.Se单质常温下也呈气态,只有氧化性
c.沸点:H2Se<H2O
您最近一年使用:0次
【推荐1】已知A、B、C、D、E、F、G、H为原子序数依次增大的前36号元素,A的一种同位素原子无中子;B元素基态原子的核外电子数是其能级数的2倍,且含有未成对的电子;D的基态原子2p轨道中含有两种不同自旋方向的电子,且电子数之比为3∶1;E为周期表中电负性最强的元素;F、H与D元素同主族;G位于第四周期第IB族。回答下列问题(用元素符号或化学式表示):
(1)G+的价层电子排布式为_______
(2)B、C、F的原子半径由大到小的顺序为_______ (填元素符号)。
(3)C、D、E的第一电离能由大到小排序是_______ (填元素符号)。
(4)从分子结构与性质角度分析CA3气体易溶于水的原因是_______ ,_______ 。
(5)由A、B、D三种元素形成的餐桌上常见的化合物B2A4D2,一个该分子中含_______ 个键,该分子中所含的化学键的类型为_______ (填序号)。
A.离子键 B.极性共价键 C.非极性共价键
(1)G+的价层电子排布式为
(2)B、C、F的原子半径由大到小的顺序为
(3)C、D、E的第一电离能由大到小排序是
(4)从分子结构与性质角度分析CA3气体易溶于水的原因是
(5)由A、B、D三种元素形成的餐桌上常见的化合物B2A4D2,一个该分子中含
A.离子键 B.极性共价键 C.非极性共价键
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表为长式周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)表中⑨号属于______ 区元素。
(2)③和⑧形成的一种常见溶剂,其分子立体空间构型为________ 。
(3)元素①和⑥形成的最简单分子X属于________ 分子(填“极性”或“非极性”)
(4)元素⑥的第一电离能________ 元素⑦的第一电离能;元素②的电负性________ 元素④的电负性(选填“>”、“=”或“<”)。
(5)元素⑨的基态原子核外价电子排布式是________ 。
(6)元素⑧和④形成的化合物的电子式为________ 。
(7)某些不同族元素的性质也有一定的相似性,如表中元素⑩与元素⑤的氢氧化物有相似的性质。请写出元素⑩的氢氧化物与NaOH溶液反应的化学方程式:____________________ 。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||||||||||||
| ⑨ | ⑩ |
请回答下列问题:
(1)表中⑨号属于
(2)③和⑧形成的一种常见溶剂,其分子立体空间构型为
(3)元素①和⑥形成的最简单分子X属于
(4)元素⑥的第一电离能
(5)元素⑨的基态原子核外价电子排布式是
(6)元素⑧和④形成的化合物的电子式为
(7)某些不同族元素的性质也有一定的相似性,如表中元素⑩与元素⑤的氢氧化物有相似的性质。请写出元素⑩的氢氧化物与NaOH溶液反应的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】元素周期表是元素周期律的具体表现,是学习和研究化学的一种重要工具。下图是元素周期表的一部分,回答下列问题:
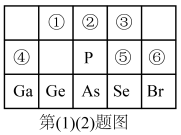

(1)元素①最简单的气态氢化物分子的空间构型是___________ 。请用一个方程式比较元素①和元素②的非金属性强弱:___________ 。
(2)元素⑤、⑥非金属性更强的是:___________ (用元素符号表示),请从原子结构的角度解释:___________ 。
电离能是指由气态原子失去电子形成阳离子需要的能量。从中性原子中失去第一个电子所需要的能量为第一电离能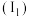 ,失去第二个电子所需要的能量为第二电离能
,失去第二个电子所需要的能量为第二电离能 ,依次类推。上图为1-19号元素第一电离能
,依次类推。上图为1-19号元素第一电离能 。回答下列问题:
。回答下列问题:
(3)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常,预测下列关系式中正确的是___________(填编号)。
(4)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
锰元素位于第四周期第VIIB族。请写出基态 的价层电子排布式:
的价层电子排布式:___________ ,比较两元素的 、
、 ,可知,气态
,可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是___________ 。
(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:___________ 。


(1)元素①最简单的气态氢化物分子的空间构型是
(2)元素⑤、⑥非金属性更强的是:
电离能是指由气态原子失去电子形成阳离子需要的能量。从中性原子中失去第一个电子所需要的能量为第一电离能
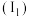 ,失去第二个电子所需要的能量为第二电离能
,失去第二个电子所需要的能量为第二电离能 ,依次类推。上图为1-19号元素第一电离能
,依次类推。上图为1-19号元素第一电离能 。回答下列问题:
。回答下列问题:(3)同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常,预测下列关系式中正确的是___________(填编号)。
A.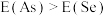 | B. |
C. | D.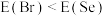 |
| 元素 | Mn | Fe | |
电离能 |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
 的价层电子排布式:
的价层电子排布式: 、
、 ,可知,气态
,可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出
 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】中国古代文献中记载了大量古代化学的研究成果,《本草纲目》中记载:“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者”,反应原理为:S+2KNO3+3C=K2S+N2↑+3CO2↑。
(1)硫原子的价层电子排布图为_____ ,烟花燃放过程中,钾元素中的电子跃迁的方式是____ ,K、S、N、O四种元素第一电离能由大到小的顺序为____ 。上述反应涉及的元素中电负性最大的是_____ (填元素符号)。
(2)碳元素除可形成常见的氧化物CO、CO2外,还可形成C2O3(结构式为 )。C2O3与水反应可生成草酸(HOOC—COOH)。
)。C2O3与水反应可生成草酸(HOOC—COOH)。
①C2O3中碳原子的杂化轨道类型为______ ,CO2分子的立体构型为_____ 。
②草酸与正丁酸(CH3CH2CH2COOH)的相对分子质量相差2,二者的熔点分别为101℃、-7.9℃,导致这种差异的最主要原因可能是______ 。
③CO分子中π键与σ键个数比为______ 。
(3)超氧化钾的晶胞结构图如下,则与K+等距离且最近的O2 - 个数为_____ ,若晶胞参数为dpm,则该超氧化物的密度为___ g·cm-3(用含d、NA的代数式表示,设NA表示阿伏加 德罗常数的值)。
(1)硫原子的价层电子排布图为
(2)碳元素除可形成常见的氧化物CO、CO2外,还可形成C2O3(结构式为
 )。C2O3与水反应可生成草酸(HOOC—COOH)。
)。C2O3与水反应可生成草酸(HOOC—COOH)。①C2O3中碳原子的杂化轨道类型为
②草酸与正丁酸(CH3CH2CH2COOH)的相对分子质量相差2,二者的熔点分别为101℃、-7.9℃,导致这种差异的最主要原因可能是
③CO分子中π键与σ键个数比为
(3)超氧化钾的晶胞结构图如下,则与K+等距离且最近的O2 - 个数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】下图是元素周期表的一部分

(1)元素⑩的次外层电子数为__________ 个。
(2)如果在温度接近373K时,根据M=m/n测定⑤的气态氢化物的相对分子质量,结果发现测定结果比理论值高,其原因是___________________ ;
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质。写出元素②的氢氧化物与NaOH溶液反应的离子方程式____________________ ;
(4)根据下列五种元素的第一至第四电离能数据(单位:kJ•mol-1),回答下面各题:
①在周期表中,最可能处于同一主族的是_________ .(填元素代号)
②T元素最可能是________ (填“s”、“p”、“d”、“ds”等)区元素;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物分子键角为____________ 。

(1)元素⑩的次外层电子数为
(2)如果在温度接近373K时,根据M=m/n测定⑤的气态氢化物的相对分子质量,结果发现测定结果比理论值高,其原因是
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质。写出元素②的氢氧化物与NaOH溶液反应的离子方程式
(4)根据下列五种元素的第一至第四电离能数据(单位:kJ•mol-1),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
②T元素最可能是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】硼及其化合物是用途广泛的化工原料,硼可以与多种元素形成化合物。
回答下列问题:
(1)硼酸的化学式为B(OH)3,是一元弱酸。
①硼酸具有弱酸性是由于B与水中的OH-形成配位键,在该键中由____ 原子提供空轨道。
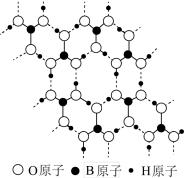
②硼酸晶体是片层结构,其中一层的结构如图所示。硼酸晶体在冷水中的溶解度很小,但在热水中较大,可能的原因是____ 。
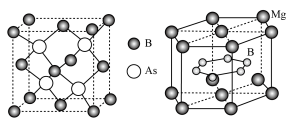
(2)砷化硼和硼化镁均可做高温超导材料,其晶胞结构分别如图所示。
①砷化硼属于____ 晶体,B原子的杂化轨道类型是____ 。
②硼化镁的化学式是____ 。
回答下列问题:
(1)硼酸的化学式为B(OH)3,是一元弱酸。
①硼酸具有弱酸性是由于B与水中的OH-形成配位键,在该键中由
②硼酸晶体是片层结构,其中一层的结构如图所示。硼酸晶体在冷水中的溶解度很小,但在热水中较大,可能的原因是

(2)砷化硼和硼化镁均可做高温超导材料,其晶胞结构分别如图所示。

①砷化硼属于
②硼化镁的化学式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】丁二烯(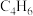 )是生产合成橡胶的重要原料,其用量占全部合成橡胶原料消耗的60%以上,工业上可通过多种催化方法生产丁二烯。回答下列问题:
)是生产合成橡胶的重要原料,其用量占全部合成橡胶原料消耗的60%以上,工业上可通过多种催化方法生产丁二烯。回答下列问题:
(1)已知如下热化学方程式:
丁烷( )脱氢:
)脱氢: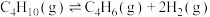
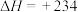 kJ/mol
kJ/mol
丁烯( )脱氢:
)脱氢: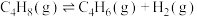
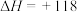 kJ/mol
kJ/mol
则下图中符号X表示的是_______ 。_______ 。
(3)丁烯氧化脱氢制丁二烯的化学反应为: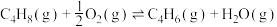 。一定条件下该反应的平衡常数K与热力学温度T的关系近似为:
。一定条件下该反应的平衡常数K与热力学温度T的关系近似为: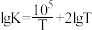 ,则该反应
,则该反应
_______ O(填“>”或“<”)。
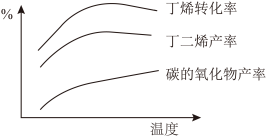
(4)丁烯氧化脱氢反应常伴随碳的氧化物的生成。研究在一定气体流速下,丁烯氧化脱氢反应随温度变化的关系如图所示。丁烯转化率随温度升高先增大后减小的原因是_______ ,反应不宜在较高的温度下进行的原因是_______ 。 氧化丁烯脱氢制备丁二烯近来得到广泛关注。研究表明该反应可能为一步或两步进行(如图所示)。已知某温度下,反应①的平衡常数
氧化丁烯脱氢制备丁二烯近来得到广泛关注。研究表明该反应可能为一步或两步进行(如图所示)。已知某温度下,反应①的平衡常数 kPa,反应②的平衡常数
kPa,反应②的平衡常数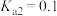 kPa,则当平衡体系中
kPa,则当平衡体系中 与
与 的分压相等时,
的分压相等时, 与CO的分压之比为
与CO的分压之比为_______ 。_______ 个,已知该晶体结构示意图的底边长为a nm,高为c nm,则其晶体密度为_______ g⋅cm (用含a、c和
(用含a、c和 的计算式表示,无需化简)。
的计算式表示,无需化简)。
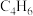 )是生产合成橡胶的重要原料,其用量占全部合成橡胶原料消耗的60%以上,工业上可通过多种催化方法生产丁二烯。回答下列问题:
)是生产合成橡胶的重要原料,其用量占全部合成橡胶原料消耗的60%以上,工业上可通过多种催化方法生产丁二烯。回答下列问题:(1)已知如下热化学方程式:
丁烷(
 )脱氢:
)脱氢: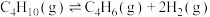
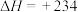 kJ/mol
kJ/mol丁烯(
 )脱氢:
)脱氢: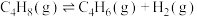
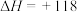 kJ/mol
kJ/mol则下图中符号X表示的是

(3)丁烯氧化脱氢制丁二烯的化学反应为:
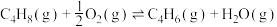 。一定条件下该反应的平衡常数K与热力学温度T的关系近似为:
。一定条件下该反应的平衡常数K与热力学温度T的关系近似为: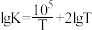 ,则该反应
,则该反应
(4)丁烯氧化脱氢反应常伴随碳的氧化物的生成。研究在一定气体流速下,丁烯氧化脱氢反应随温度变化的关系如图所示。丁烯转化率随温度升高先增大后减小的原因是
 氧化丁烯脱氢制备丁二烯近来得到广泛关注。研究表明该反应可能为一步或两步进行(如图所示)。已知某温度下,反应①的平衡常数
氧化丁烯脱氢制备丁二烯近来得到广泛关注。研究表明该反应可能为一步或两步进行(如图所示)。已知某温度下,反应①的平衡常数 kPa,反应②的平衡常数
kPa,反应②的平衡常数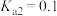 kPa,则当平衡体系中
kPa,则当平衡体系中 与
与 的分压相等时,
的分压相等时, 与CO的分压之比为
与CO的分压之比为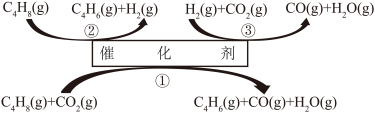
 (用含a、c和
(用含a、c和 的计算式表示,无需化简)。
的计算式表示,无需化简)。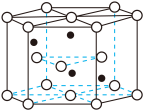
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】科学家预测21 世纪中叶将进入“氢能经济”时代,许多化合物或合金都是具有广阔应用前景的储氢材料。回答下列问题:
(1)基态Li原子核外电子有___ 种不同的运动状态,占据最高能层电子的电子云轮廓图形状为____________ 。
(2)Li的焰色反应为紫红色,很多金属元素能产生焰色反应的原因为___________________ 。
(3)亚氨基锂(Li2NH) 中所含的元素,电负性由大到小排列的顺序是_________ 。
(4)咔唑(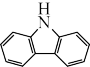 )的沸点比芴(
)的沸点比芴(  )高的主要原因是
)高的主要原因是___________________ 。
(5)NH3BH3(氨硼烷,熔点104℃)与______ (写出一种分子)互为等电子体。可通过红外光谱测定该分子的立体构型,NH3BH3中B的杂化轨道类型为____________ 。
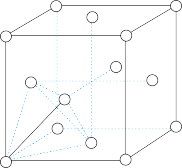
(6)一种储氢合金的晶胞结构如图所示。在晶胞中Cu 原子处于面心,Au 原子处于顶点位置。该晶体中,原子之间的作用力是___________ 。实现储氢功能时,氢原子可进入到由Cu 原子与Au 原子构成的四面体空隙中心(如图),若所有四面体空隙都填满,该晶体储氢后的化学式为__________ 。已知该晶胞的晶胞参数为a nm,阿伏加 德罗常数值为NA,则密度ρ为__________ g/cm3(用NA和a的代数式表示)
(1)基态Li原子核外电子有
(2)Li的焰色反应为紫红色,很多金属元素能产生焰色反应的原因为
(3)亚氨基锂(Li2NH) 中所含的元素,电负性由大到小排列的顺序是
(4)咔唑(
 )的沸点比芴(
)的沸点比芴(  )高的主要原因是
)高的主要原因是(5)NH3BH3(氨硼烷,熔点104℃)与
(6)一种储氢合金的晶胞结构如图所示。在晶胞中Cu 原子处于面心,Au 原子处于顶点位置。该晶体中,原子之间的作用力是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】金属材料对于促进生产发展、改善人类生活发挥了巨大作用。
I.钢是人类使用最早的金属之一,至今仍被广泛应用于电气、电子等领域。
(1)写出基态Cu原子的核外电子排布式___________ 。涩法冶炼是以赤铜矿( )精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。
)精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。
(2)赤铜矿在稀硫酸中浸出,得到硫酸铜溶液,该反应的离子方程式为___ 。
(3)已知: 晶胞为立方体形,边长为
晶胞为立方体形,边长为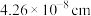 。根据图示,每个
。根据图示,每个 晶胞中含O原子的数目为
晶胞中含O原子的数目为___________ 个。计算 晶体的密度
晶体的密度
___________  (结果保留两位小数)。
(结果保留两位小数)。
(4)基态Na原子的价层电子轨道表示式为___________ 。
(5)NaCl熔点为:800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式为:
 ,加入
,加入 的目的是
的目的是___________ 。
(6)除去 粉末中混有的少量
粉末中混有的少量 的方法是
的方法是___________ 。
Ⅲ.钛被誉为太空金属和亲生物金属,拥有卓越的金属特性。它在特定温度下能与多种物质发生反应,在生产和日常生活中都能找到它的踪影。
(7) 原子的价电子排布式为
原子的价电子排布式为 ,它在元素周期表中的位置是
,它在元素周期表中的位置是___________ 。
(8) 易与
易与 形成
形成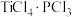 。下列关于
。下列关于 分子说法错误的是___________。
分子说法错误的是___________。
(9)钛溶于盐酸制得的三氯化钛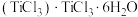 晶体有两种异构体:
晶体有两种异构体: (绿色)、
(绿色)、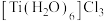 (紫色),两者配位数
(紫色),两者配位数___________ (选填“相同”或“不同”),绿色晶体中配体是___________ 。
I.钢是人类使用最早的金属之一,至今仍被广泛应用于电气、电子等领域。
(1)写出基态Cu原子的核外电子排布式
 )精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。
)精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。(2)赤铜矿在稀硫酸中浸出,得到硫酸铜溶液,该反应的离子方程式为
(3)已知:
 晶胞为立方体形,边长为
晶胞为立方体形,边长为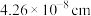 。根据图示,每个
。根据图示,每个 晶胞中含O原子的数目为
晶胞中含O原子的数目为 晶体的密度
晶体的密度
 (结果保留两位小数)。
(结果保留两位小数)。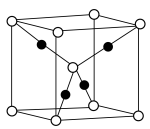
(4)基态Na原子的价层电子轨道表示式为
(5)NaCl熔点为:800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式为:

 ,加入
,加入 的目的是
的目的是(6)除去
 粉末中混有的少量
粉末中混有的少量 的方法是
的方法是Ⅲ.钛被誉为太空金属和亲生物金属,拥有卓越的金属特性。它在特定温度下能与多种物质发生反应,在生产和日常生活中都能找到它的踪影。
(7)
 原子的价电子排布式为
原子的价电子排布式为 ,它在元素周期表中的位置是
,它在元素周期表中的位置是(8)
 易与
易与 形成
形成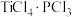 。下列关于
。下列关于 分子说法错误的是___________。
分子说法错误的是___________。| A.键角为120° | B.是极性分子 |
C.含有 键 键 | D.中心原子采取 杂化 杂化 |
(9)钛溶于盐酸制得的三氯化钛
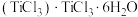 晶体有两种异构体:
晶体有两种异构体: (绿色)、
(绿色)、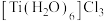 (紫色),两者配位数
(紫色),两者配位数
您最近一年使用:0次



