填表:
| 原子序数 | 核外电子排布式 | 外围电子排布式 | 周期表中的位置 |
| 16 | |||
| 23 | |||
| 34 |
更新时间:2020-03-06 20:14:44
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】如图是元素周期表的一部分。表中所列的字母分别代表某一元素。

(1) mol A与
mol A与 的简单氢化物完全反应时可产生标准状况下气体的体积为
的简单氢化物完全反应时可产生标准状况下气体的体积为___________ 。
(2)写出 的最高价氧化物对应的水化物的化学式
的最高价氧化物对应的水化物的化学式___________ 。
(3)其中含元素E化合物是一种白色胶状沉淀,可用于净水,则该物质的化学式为___________ ; 与
与 的氢氧化物水溶液反应的化学方程式为
的氢氧化物水溶液反应的化学方程式为___________ 。C的简单氢化物的电子式___________ 。
(4) 、E、F、
、E、F、 形成的简单离子半径由大到小顺序(用离子符合表示)
形成的简单离子半径由大到小顺序(用离子符合表示)___________ 。

(1)
 mol A与
mol A与 的简单氢化物完全反应时可产生标准状况下气体的体积为
的简单氢化物完全反应时可产生标准状况下气体的体积为(2)写出
 的最高价氧化物对应的水化物的化学式
的最高价氧化物对应的水化物的化学式(3)其中含元素E化合物是一种白色胶状沉淀,可用于净水,则该物质的化学式为
 与
与 的氢氧化物水溶液反应的化学方程式为
的氢氧化物水溶液反应的化学方程式为(4)
 、E、F、
、E、F、 形成的简单离子半径由大到小顺序(用离子符合表示)
形成的简单离子半径由大到小顺序(用离子符合表示)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表显示了元素周期表中短周期的一部分,①~⑥代表6种短周期元素。
已知③与氢元素能组成生活中最常见的化合物X。请填写下列空白。
(1)与⑤同族的下一周期元素的原子结构示意图为___________ 。
(2)④的单质与X反应的离子方程式为___________ 。
(3)⑥的单质与X反应的化学方程式为___________ 。
(4)①、②、③分别与氢元素组成含10个电子的分子的化学式分别为___________ 、___________ 、___________ 。
| ① | ② | ③ | ||||
| ④ | ⑤ | ⑥ |
(1)与⑤同族的下一周期元素的原子结构示意图为
(2)④的单质与X反应的离子方程式为
(3)⑥的单质与X反应的化学方程式为
(4)①、②、③分别与氢元素组成含10个电子的分子的化学式分别为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是周期表的一部分,根据A~I在周期表中的位置,回答以下问题:
(1)表中元素,化学性质最不活泼的是___________ (用元素符号表示,本小题下同);除稀有气体外,原子半径最大的是___________ ,可用于制半导体材料的元素是_______ ;形成化合物中种类最多的元素是___________ 。
(2)最高价氧化物的水化物酸性最强的是___________ (填化学式),A分别与D、E、F、G、H形成的化合物中,最稳定的是___________ (填化学式)
(3)元素E和元素H的氢化物均极易溶于水,用两根玻璃棒分别醮取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式___________
(4)B、C两元素的最高价氧化物对应水化物之间反应的离子方程式是___________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | J | F | H | I |
(1)表中元素,化学性质最不活泼的是
(2)最高价氧化物的水化物酸性最强的是
(3)元素E和元素H的氢化物均极易溶于水,用两根玻璃棒分别醮取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式
(4)B、C两元素的最高价氧化物对应水化物之间反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】柠檬酸亚铁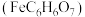 是一种高效补铁剂,实验室可通过铁粉制备,反应原理简示如下:
是一种高效补铁剂,实验室可通过铁粉制备,反应原理简示如下:
实验步骤:
①取15g铁粉,用 ,边搅拌边加热,至反应完全,过滤,以滤液制备
,边搅拌边加热,至反应完全,过滤,以滤液制备 (
(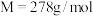 )晶体。
)晶体。
②取9g精制的 ,缓慢加入
,缓慢加入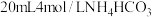 溶液,静置40min后有大量
溶液,静置40min后有大量
沉淀析出,过滤洗涤,得 晶体。
晶体。
③在烧杯中加入6g柠檬酸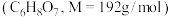 、80mL水、
、80mL水、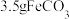 边加热边搅拌至晶体析出,过滤洗涤干燥得
边加热边搅拌至晶体析出,过滤洗涤干燥得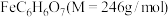 晶体。
晶体。
回答下列问题:
(1)请利用原子结构的相关知识解释三价铁比二价铁稳定原因_______ 。
(2) 溶液制备
溶液制备 晶体常用两种方法:
晶体常用两种方法:
方法ⅰ:先将滤液进行蒸发浓缩至稀糊状,可选用仪器有酒精灯、玻璃棒、_______ (从下列仪器中选择并填写名称,后一问相同要求)等,再将浓缩液冷却至室温,用_______ (仪器名称)过滤,其优点是_______ 。
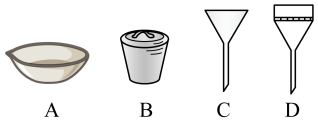
方法ⅱ:将滤液冷却静置后,用玻璃棒摩擦烧杯壁,先有少量规则晶体出现,后有大量晶体 晶体出现。试回答,用玻璃棒摩擦烧杯壁的作用
晶体出现。试回答,用玻璃棒摩擦烧杯壁的作用_______ 。
(3)写出制备碳酸亚铁的离子方程式_______ 。
(4)利用邻二氮菲 与
与 生成稳定橙红色配合物
生成稳定橙红色配合物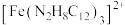 ,最大吸收波长为510nm这一特征可用来检测
,最大吸收波长为510nm这一特征可用来检测 含量,某同学将上述所制
含量,某同学将上述所制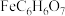 晶体全部溶解于试管中后,添加25mL3mol/L邻二氮菲溶液后,可获得最大吸收波长,则
晶体全部溶解于试管中后,添加25mL3mol/L邻二氮菲溶液后,可获得最大吸收波长,则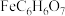 晶体质量为
晶体质量为_______ g。
(5)不用酸性高锰酸钾溶液滴定 最可能的原因是
最可能的原因是_______ 。
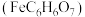 是一种高效补铁剂,实验室可通过铁粉制备,反应原理简示如下:
是一种高效补铁剂,实验室可通过铁粉制备,反应原理简示如下:
实验步骤:
①取15g铁粉,用
 ,边搅拌边加热,至反应完全,过滤,以滤液制备
,边搅拌边加热,至反应完全,过滤,以滤液制备 (
(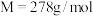 )晶体。
)晶体。②取9g精制的
 ,缓慢加入
,缓慢加入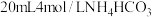 溶液,静置40min后有大量
溶液,静置40min后有大量
沉淀析出,过滤洗涤,得
 晶体。
晶体。③在烧杯中加入6g柠檬酸
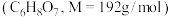 、80mL水、
、80mL水、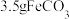 边加热边搅拌至晶体析出,过滤洗涤干燥得
边加热边搅拌至晶体析出,过滤洗涤干燥得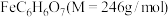 晶体。
晶体。回答下列问题:
(1)请利用原子结构的相关知识解释三价铁比二价铁稳定原因
(2)
 溶液制备
溶液制备 晶体常用两种方法:
晶体常用两种方法:方法ⅰ:先将滤液进行蒸发浓缩至稀糊状,可选用仪器有酒精灯、玻璃棒、

方法ⅱ:将滤液冷却静置后,用玻璃棒摩擦烧杯壁,先有少量规则晶体出现,后有大量晶体
 晶体出现。试回答,用玻璃棒摩擦烧杯壁的作用
晶体出现。试回答,用玻璃棒摩擦烧杯壁的作用(3)写出制备碳酸亚铁的离子方程式
(4)利用邻二氮菲
 与
与 生成稳定橙红色配合物
生成稳定橙红色配合物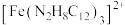 ,最大吸收波长为510nm这一特征可用来检测
,最大吸收波长为510nm这一特征可用来检测 含量,某同学将上述所制
含量,某同学将上述所制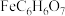 晶体全部溶解于试管中后,添加25mL3mol/L邻二氮菲溶液后,可获得最大吸收波长,则
晶体全部溶解于试管中后,添加25mL3mol/L邻二氮菲溶液后,可获得最大吸收波长,则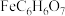 晶体质量为
晶体质量为(5)不用酸性高锰酸钾溶液滴定
 最可能的原因是
最可能的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】碳、硅、溴及其化合物在生产、生活中应用广泛。回答下列问题:
(1)基态Si原子核外电子的空间运动状态有_______ 种,核外电子占据的最高能层符号为_______ ,能量最高的电子占据的原子轨道电子云轮廓为_______ 形。
(2)C、O、Si电负性由小到大的顺序为_______ ;元素C和元素O形成的最简单氢化物的键角:_______ >_______ (填氢化物的化学式)。
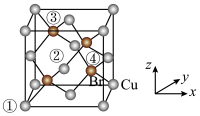
(3)CuBr是点击化学常用的催化剂,其晶胞结构如图所示,晶胞参数为apm。已知①号铜原子坐标分数为(0,0,0),则②号铜原子的坐标分数为_______ ;③号溴原子与最近的铜原子之间的距离为_______ ;CuBr晶体的密度为dg•cm﹣3,则阿伏加德罗常数NA=_______ (列出计算式)。
(1)基态Si原子核外电子的空间运动状态有
(2)C、O、Si电负性由小到大的顺序为
(3)CuBr是点击化学常用的催化剂,其晶胞结构如图所示,晶胞参数为apm。已知①号铜原子坐标分数为(0,0,0),则②号铜原子的坐标分数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】硫自远古时代就被人们所知晓并使用,请回答:
(1)低浓度的 溶液中存在2种结构A(
溶液中存在2种结构A( )和B(
)和B( ),A结构中硫原子的杂化轨道类型是
),A结构中硫原子的杂化轨道类型是_______ 。B结构的空间构型(以S为中心)名称为_______ 。A与B通过氢键形成C,请画出C的结构_______ 。
(2)下列关于由S元素形成的微粒说法正确的是_______。
(3)CuS的晶胞如图所示,该图中缺失了部分硫原子,请在如图上用白球或黑球将缺失的原子补齐_______ ,该晶胞内含有Cu原子为_______ 个,其中配位4个硫原子的Cu原子有_______ 个。

(1)低浓度的
 溶液中存在2种结构A(
溶液中存在2种结构A( )和B(
)和B( ),A结构中硫原子的杂化轨道类型是
),A结构中硫原子的杂化轨道类型是(2)下列关于由S元素形成的微粒说法正确的是_______。
A. 的价电子排布图为 的价电子排布图为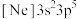 |
B.[Ne]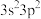 电离1个电子所需最低能量大于[Ne] 电离1个电子所需最低能量大于[Ne]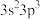 |
C. 的氧化性强于 的氧化性强于 |
D. 的发射光谱不止1条谱线 的发射光谱不止1条谱线 |

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】二氧化钛是钛的重要化合物,钛白(纯净的二氧化钛)是一种折射率高、着色力和遮盖力强、化学性质稳定的白色颜料。钛精矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有Fe2O3、SiO2等杂质,由钛精矿制取一氧化钛,常用硫酸法,其流程如下:

(1)基态22Ti原子的价电子排布式为___________ 。
(2)钛精矿主要成分与硫酸反应的主要产物是TiOSO4和FeSO4,该反应的化学方程式为___________ 。
(3)矿渣主要成分___________ ,试剂X为___________ (填化学式)。
(4)为了从溶液I中获取纯净的FeSO4·7H2O,应采取的操作是___________ 、___________ 、过滤、洗涤、干燥。
(5)用氧化还原滴定法测定制备得到的中间产品中TiO2的质量分数:在一定条件下,将一定量的产品溶解并将TiO2还原为Ti3+,再以KSCN溶液作为指示剂,用硫酸铁铵 [NH4Fe(SO4)2]标准溶液滴定Ti3+至全部生成Ti4+。
①滴定终点的现象是:加入最后半滴标准液时,___________ 。
②滴定分析时,称取TiO2试样0.2g,消耗0.1mol/L[NH4Fe(SO4)2]标准溶液24.00mL,则TiO2的质量分数为(计算结果保留小数点后一位)___________ 。

(1)基态22Ti原子的价电子排布式为
(2)钛精矿主要成分与硫酸反应的主要产物是TiOSO4和FeSO4,该反应的化学方程式为
(3)矿渣主要成分
(4)为了从溶液I中获取纯净的FeSO4·7H2O,应采取的操作是
(5)用氧化还原滴定法测定制备得到的中间产品中TiO2的质量分数:在一定条件下,将一定量的产品溶解并将TiO2还原为Ti3+,再以KSCN溶液作为指示剂,用硫酸铁铵 [NH4Fe(SO4)2]标准溶液滴定Ti3+至全部生成Ti4+。
①滴定终点的现象是:加入最后半滴标准液时,
②滴定分析时,称取TiO2试样0.2g,消耗0.1mol/L[NH4Fe(SO4)2]标准溶液24.00mL,则TiO2的质量分数为(计算结果保留小数点后一位)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】2020年12月17 日凌晨1时59分,“嫦娥五号”首次实现了我国地外天体采样返回,标志着我国航天事业迈出了一大步。带回的月壤中包含了H、O、N、Al、S、Ti、Cu、Au等多种元素。回答下列问题:
(1)Ti被称为第三金属,写出Ti的原子结构示意图:_______
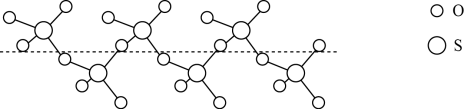
(2)S 与O可形成多种微粒,其中SO2能杀菌,它的VSEPR模型为_______ ;;液态SO3冷却到289.8K 时,能得到一种螺旋状单链结构的固体,其结构如图所示,此固态SO3中S原子的杂化轨道类型是_______ 。
(3)含氧有机物CH3CH2OH不能用无水CaCl2干燥的原因是Ca2+和CH3CH2OH可形成[Ca(CH3CH2OH)4]2+,该离子中提供孤电子对的原子是_______ 。
(4)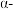 Al2O3 是“嫦娥五号”中用到的一种耐火材料,具有熔点高(2054°C)、硬度大且熔融态能导电的特点主要原因为
Al2O3 是“嫦娥五号”中用到的一种耐火材料,具有熔点高(2054°C)、硬度大且熔融态能导电的特点主要原因为_______ 。
(5)一种铜金合金具有储氢功能,其晶体为面心立方最密堆积结构,晶胞中Cu原子处于面心,Au原子处于顶点,则Au原子紧邻的Cu原子的数目为_______ 。该储氢材料储氢时,H2可进入到中Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与ZnS的结构相似(如图),该晶体储氢后的化学式为_______ 中;若最近的铜原子 与金原子之间的距离为apm,NA表示阿伏加德罗常数,则储氢之前的晶体密度为_______ g·cm 2 (列出计算式,不必化简)。
(1)Ti被称为第三金属,写出Ti的原子结构示意图:
(2)S 与O可形成多种微粒,其中SO2能杀菌,它的VSEPR模型为

(3)含氧有机物CH3CH2OH不能用无水CaCl2干燥的原因是Ca2+和CH3CH2OH可形成[Ca(CH3CH2OH)4]2+,该离子中提供孤电子对的原子是
(4)
 Al2O3 是“嫦娥五号”中用到的一种耐火材料,具有熔点高(2054°C)、硬度大且熔融态能导电的特点主要原因为
Al2O3 是“嫦娥五号”中用到的一种耐火材料,具有熔点高(2054°C)、硬度大且熔融态能导电的特点主要原因为(5)一种铜金合金具有储氢功能,其晶体为面心立方最密堆积结构,晶胞中Cu原子处于面心,Au原子处于顶点,则Au原子紧邻的Cu原子的数目为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
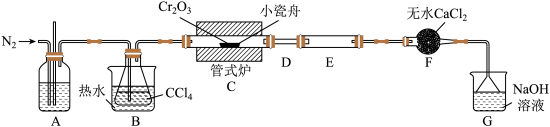
【推荐3】三氯化铬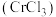 是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取
是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取 的反应为,其实验装置如图所示:
的反应为,其实验装置如图所示:
已知:① (俗称光气)有毒,遇水发生水解;
(俗称光气)有毒,遇水发生水解;
②碱性条件下, 可将
可将 氧化为
氧化为 ;酸性条件下,
;酸性条件下, 将
将 还原为
还原为 。
。
回答下列问题:
(1)基态 原子的简化核外电子排布式为
原子的简化核外电子排布式为___________ 。
(2)无水 的作用是
的作用是___________ 。
(3)装置E用来收集产物。实验过程中若D处出现堵塞,可通过___________ (填操作方法)使实验继续进行。
(4)装置G中发生生成两种盐的反应的化学方程式为___________ 。
(5)测定产品中 质量分数的实验步骤如下:
质量分数的实验步骤如下:
I.取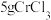 产品,在强碱性条件下,加入过量的
产品,在强碱性条件下,加入过量的 溶液,小火加热使
溶液,小火加热使 完全转化为
完全转化为 ,继续加热一段时间;
,继续加热一段时间;
II.冷却后,滴入适量的稀硫酸和浓磷酸(浓磷酸的作用是防止指示剂提前变色),使 转化为
转化为 ,再加适量的蒸馏水将溶液稀释至
,再加适量的蒸馏水将溶液稀释至 ;
;
III.取 溶液,加入适量浓硫酸混合均匀,滴入3滴试亚铁灵作指示剂,用新配制的
溶液,加入适量浓硫酸混合均匀,滴入3滴试亚铁灵作指示剂,用新配制的 的
的 标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗
标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗 标准溶液
标准溶液 (已知
(已知 被
被 还原为
还原为 )。
)。
①该样品中 的质量分数为
的质量分数为___________  (保留小数点后两位,
(保留小数点后两位,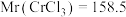 )
)
②下列操作将导致产品中 质量分数测定值偏低的是
质量分数测定值偏低的是___________ (填标号)。
A.步骤I中未继续加热一段时间
B.步骤III中所用 溶液已变质
溶液已变质
C.步骤II中未加浓磷酸
D.步骤III中读数时,滴定前俯视,滴定后平视
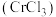 是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取
是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取 的反应为,其实验装置如图所示:
的反应为,其实验装置如图所示:
已知:①
 (俗称光气)有毒,遇水发生水解;
(俗称光气)有毒,遇水发生水解;②碱性条件下,
 可将
可将 氧化为
氧化为 ;酸性条件下,
;酸性条件下, 将
将 还原为
还原为 。
。回答下列问题:
(1)基态
 原子的简化核外电子排布式为
原子的简化核外电子排布式为(2)无水
 的作用是
的作用是(3)装置E用来收集产物。实验过程中若D处出现堵塞,可通过
(4)装置G中发生生成两种盐的反应的化学方程式为
(5)测定产品中
 质量分数的实验步骤如下:
质量分数的实验步骤如下:I.取
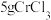 产品,在强碱性条件下,加入过量的
产品,在强碱性条件下,加入过量的 溶液,小火加热使
溶液,小火加热使 完全转化为
完全转化为 ,继续加热一段时间;
,继续加热一段时间;II.冷却后,滴入适量的稀硫酸和浓磷酸(浓磷酸的作用是防止指示剂提前变色),使
 转化为
转化为 ,再加适量的蒸馏水将溶液稀释至
,再加适量的蒸馏水将溶液稀释至 ;
;III.取
 溶液,加入适量浓硫酸混合均匀,滴入3滴试亚铁灵作指示剂,用新配制的
溶液,加入适量浓硫酸混合均匀,滴入3滴试亚铁灵作指示剂,用新配制的 的
的 标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗
标准溶液滴定,溶液由黄色经蓝绿色变为红褐色即为终点,重复2~3次,平均消耗 标准溶液
标准溶液 (已知
(已知 被
被 还原为
还原为 )。
)。①该样品中
 的质量分数为
的质量分数为 (保留小数点后两位,
(保留小数点后两位,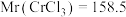 )
)②下列操作将导致产品中
 质量分数测定值偏低的是
质量分数测定值偏低的是A.步骤I中未继续加热一段时间
B.步骤III中所用
 溶液已变质
溶液已变质C.步骤II中未加浓磷酸
D.步骤III中读数时,滴定前俯视,滴定后平视
您最近一年使用:0次



