工业上常用水合肼(N2H4∙H2O)还原法制取碘化钠,工艺流程如图:
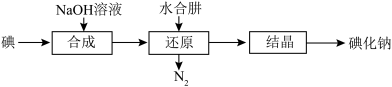
已知:I2与NaOH溶液反应,其氧化产物与还原产物的物质的量之比为1:5
(1)写出水合肼还原过程的化学反应方程式_____ 。
(2)若加入的水合肼已过量,请设计实验方案检验_____ 。

已知:I2与NaOH溶液反应,其氧化产物与还原产物的物质的量之比为1:5
(1)写出水合肼还原过程的化学反应方程式
(2)若加入的水合肼已过量,请设计实验方案检验
更新时间:2020-03-11 19:49:38
|
相似题推荐
【推荐1】溴是一种重的化工原料,从淡化海水中提取溴的工艺流程如下:

⑴操作Ⅱ中,用饱和Na2CO3碱性溶液吸收Br2,过程中有CO2产生,反应的粒子方程式为______ ,当0.6 mol Br2被吸收时,转移电子的数目为______
 步骤Ⅳ包含萃取,分液和蒸馏,该过程中不必用到的仪器有
步骤Ⅳ包含萃取,分液和蒸馏,该过程中不必用到的仪器有______  填序号
填序号
a.烧杯 b.分液漏斗c.普通漏斗 d.玻璃棒 e.蒸发皿 f.冷凝管
 某化学兴趣小组利用高锰酸钾和浓盐酸反应制取氯气,并探究氯水的性质
某化学兴趣小组利用高锰酸钾和浓盐酸反应制取氯气,并探究氯水的性质

①将A,B,C相连,制得Cl2后加入适量水,即可制得氯水,将所得氯水分为两份,进行甲,乙两个实验,实验操作如下,将现象填入下表:
②由实验乙不能推出氯气与水反应的产物具有酸性,原因是______ ,若要制备纯净干燥的Cl2,按气流方向连接各仪器接口,顺序为a→_____ →_____ →_____ →_____ →_____ →_____ →d
 实验完毕后,假设装置C中氢氧化钠和
实验完毕后,假设装置C中氢氧化钠和 恰好完全反应,其反应方程式为
恰好完全反应,其反应方程式为______ ,反应后溶液中离子浓度由大到小的顺序为______ ,常温下HClO的电离平衡常数为K,则常温下NaClO水解反应的平衡常数为______ (用含Ka和Kw的表达式表示)

⑴操作Ⅱ中,用饱和Na2CO3碱性溶液吸收Br2,过程中有CO2产生,反应的粒子方程式为
 步骤Ⅳ包含萃取,分液和蒸馏,该过程中不必用到的仪器有
步骤Ⅳ包含萃取,分液和蒸馏,该过程中不必用到的仪器有 填序号
填序号
a.烧杯 b.分液漏斗c.普通漏斗 d.玻璃棒 e.蒸发皿 f.冷凝管
 某化学兴趣小组利用高锰酸钾和浓盐酸反应制取氯气,并探究氯水的性质
某化学兴趣小组利用高锰酸钾和浓盐酸反应制取氯气,并探究氯水的性质
①将A,B,C相连,制得Cl2后加入适量水,即可制得氯水,将所得氯水分为两份,进行甲,乙两个实验,实验操作如下,将现象填入下表:
| 实验序号 | 实验操作 | 现象 |
| 甲 | 将氯水滴入品红溶液 | |
| 乙 | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 |
②由实验乙不能推出氯气与水反应的产物具有酸性,原因是
 实验完毕后,假设装置C中氢氧化钠和
实验完毕后,假设装置C中氢氧化钠和 恰好完全反应,其反应方程式为
恰好完全反应,其反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】2-氯丙酸(CH3CHClCOOH)主要用生产农药除草剂,还用于生产乳酸及有工业价值的低级醇酯。如图为实验室制备2-氯丙酸的装置。

已知:相关物质的物理性质如下表所示:
制备方法:在三颈烧瓶中放置148g(2mol)丙酸和1.5g三氯化磷(作催化剂),加热至100~110℃,缓慢通入氯气,保持温度在105~110℃之间大约反应5h。回答下列问题:
(1)A装置中反应的离子方程式为_______ ,当生成6.72LCl2(标准状况)时,转移电子的数目为_______ 。
(2)某同学分析发现D装置有两处缺陷,请指出其中一处_______ 。

已知:相关物质的物理性质如下表所示:
| 物质 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 2-氯丙酸 | 14 | 190 | 能与水、乙醇互溶 |
| 丙酸 | -21.5 | 141 | 能与水、乙醇互溶 |
| PCl3 | -93.6 | 76.1 | 与水剧烈反应,能溶于乙醇 |
(1)A装置中反应的离子方程式为
(2)某同学分析发现D装置有两处缺陷,请指出其中一处
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】硝酸铜晶体[Cu(NO3)2·6H2O],是一种重要的化工原料,常用于农药、镀铜、搪瓷等工业。以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备硝酸铜晶体的某工艺如图所示:

回答下列问题:
(1)“浸取”时,为了提高浸取率可采取的措施有______ (任写一点),浸取时在生成S的反应中还原剂与氧化剂的物质的量之比为______ 。
(2)薄层层析法是利用溶液各成分对同一吸附剂吸附能力不同,在溶液流过吸附剂时,使各成分互相分离的方法。某实验小组利用薄层层析法监控滤液1加入铁粉过程中溶液的组成,实验结果如下,则还需继续加入Fe粉的是______ (选填编号)。

(3)滤渣2的主要成分是______ ,滤渣2与稀硝酸反应时,需向装置内通入适量空气,这样做的目的是______ 。
(4)调节溶液pH时选用的物质a可以是______ ,几种金属离子沉淀的pH范围如图所示,“调pH”时应将溶液pH调至______ ~______ 。

(5)操作X主要包括______ 、______ 、过滤、洗涤、干燥。

回答下列问题:
(1)“浸取”时,为了提高浸取率可采取的措施有
(2)薄层层析法是利用溶液各成分对同一吸附剂吸附能力不同,在溶液流过吸附剂时,使各成分互相分离的方法。某实验小组利用薄层层析法监控滤液1加入铁粉过程中溶液的组成,实验结果如下,则还需继续加入Fe粉的是

(3)滤渣2的主要成分是
(4)调节溶液pH时选用的物质a可以是

(5)操作X主要包括
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某小组利用如图甲所示装置制备并收集 (夹持装置略去)。
(夹持装置略去)。

已知:Ⅰ.高温时能与 反应,极易水解,能溶于
反应,极易水解,能溶于 ;
;
Ⅱ.物质的熔沸点如表:
(1)加热管式炉前需先通入 的目的是
的目的是___________ ,管式炉加热至900℃时,瓷舟中会生成 、
、 和一种有毒的气态氧化物,并发生副反应生成少量
和一种有毒的气态氧化物,并发生副反应生成少量 ,写出主反应生成
,写出主反应生成 的化学方程式
的化学方程式___________ 。
(2)为除去 中的
中的 应调节控温箱的温度范围为
应调节控温箱的温度范围为___________ ℃。
(3)碱石灰的作用是___________ ,该装置的缺陷是___________ 。
(4)已知 在碳化物中硬度最大,工业上一般在真空和高温(>1800℃)条件下用C还原
在碳化物中硬度最大,工业上一般在真空和高温(>1800℃)条件下用C还原 制取
制取 :
: 。
。
①基态Ti原子的电子排布式为___________ 。
②反应中涉及的元素第一电离能最大的是___________ , 中化学键类型为
中化学键类型为___________ 。
③ 是一种优良的颜料,其晶胞结构如图。
是一种优良的颜料,其晶胞结构如图。

则黑球代表___________ (填“Ti”或“O”)。该晶体的密度为___________  (用含a、b、
(用含a、b、 的代数式表示,
的代数式表示, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 (夹持装置略去)。
(夹持装置略去)。
已知:Ⅰ.高温时能与
 反应,极易水解,能溶于
反应,极易水解,能溶于 ;
;Ⅱ.物质的熔沸点如表:
| 物质 |  |  |  |
| 熔点℃ | -23.2 | 306 | -23 |
| 沸点℃ | 136.4 | 315 | 76.8 |
(1)加热管式炉前需先通入
 的目的是
的目的是 、
、 和一种有毒的气态氧化物,并发生副反应生成少量
和一种有毒的气态氧化物,并发生副反应生成少量 ,写出主反应生成
,写出主反应生成 的化学方程式
的化学方程式(2)为除去
 中的
中的 应调节控温箱的温度范围为
应调节控温箱的温度范围为(3)碱石灰的作用是
(4)已知
 在碳化物中硬度最大,工业上一般在真空和高温(>1800℃)条件下用C还原
在碳化物中硬度最大,工业上一般在真空和高温(>1800℃)条件下用C还原 制取
制取 :
: 。
。①基态Ti原子的电子排布式为
②反应中涉及的元素第一电离能最大的是
 中化学键类型为
中化学键类型为③
 是一种优良的颜料,其晶胞结构如图。
是一种优良的颜料,其晶胞结构如图。
则黑球代表
 (用含a、b、
(用含a、b、 的代数式表示,
的代数式表示, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
【推荐2】锗是重要的半导体材料,应用于航空航天测控、光纤通讯等领域.一种提纯二氧化锗粗品(主要含GeO2、As2O3)的工艺如下:

已知:①“碱浸”过程中的反应为:
GeO2+2NaOH=Na2GeO3+H2O
As2O3+2NaOH=2NaAsO2+H2O
②“蒸馏”过程中的反应为:Na2GeO3+6HCl=2NaCl+GeCl4+3H2O
③GeCl4的熔点为-49.5℃,AsCl3与GeCl4的沸点分别为130.2℃、84℃.
(1)锗的原子序数为32,锗在元素周期表中的位置为第______ 周期 ______ 族.
(2)“氧化除砷”的过程是将NaAsO2氧化为Na3AsO4,其反应方程式为:______ .
(3)传统的提纯方法是将粗品直接加入盐酸中蒸馏,其缺点是______ .
(4)工业上与蒸馏操作相关的设备有______
A.蒸馏釜 B.离心萃取机 C.冷凝塔 D.加压过滤机
(5)“水解”操作时发生的化学反应方程式为______ ,“水解”操作时保持较低温度有利于提高产率,其最可能的原因是 ______ (答一条即可).
(6)若1吨二氧化锗粗品(含杂质30%)经提纯得0.745吨的高纯二氧化锗产品,则杂质脱除率为______ .

已知:①“碱浸”过程中的反应为:
GeO2+2NaOH=Na2GeO3+H2O
As2O3+2NaOH=2NaAsO2+H2O
②“蒸馏”过程中的反应为:Na2GeO3+6HCl=2NaCl+GeCl4+3H2O
③GeCl4的熔点为-49.5℃,AsCl3与GeCl4的沸点分别为130.2℃、84℃.
(1)锗的原子序数为32,锗在元素周期表中的位置为第
(2)“氧化除砷”的过程是将NaAsO2氧化为Na3AsO4,其反应方程式为:
(3)传统的提纯方法是将粗品直接加入盐酸中蒸馏,其缺点是
(4)工业上与蒸馏操作相关的设备有
A.蒸馏釜 B.离心萃取机 C.冷凝塔 D.加压过滤机
(5)“水解”操作时发生的化学反应方程式为
(6)若1吨二氧化锗粗品(含杂质30%)经提纯得0.745吨的高纯二氧化锗产品,则杂质脱除率为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】多晶硅生产工艺流程如图:
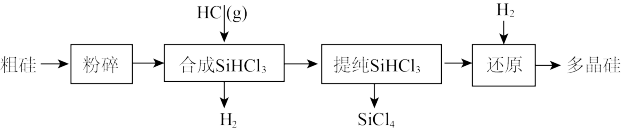
(1)粗硅粉碎的目的是_______ 。分离SiHCl3 (l)和SiCl4(l)的方法为_______ 。
(2)900℃以上, H2与SiHCl3发生如下反应:SiHCl3 (g)+ H2 (g)⇌Si (s) + 3HCl (g) ΔH >0,其平衡常数表达式为K =_______ 。为提高还原时SiHCl3的转化率,可采取的措施有_______ 。
(3)该流程中可以循环使用的物质是_______ 。
(4)SiCl4与上述流程中的单质发生化合反应,可以制得SiHCl3,其化学方程式为_______ 。

(1)粗硅粉碎的目的是
(2)900℃以上, H2与SiHCl3发生如下反应:SiHCl3 (g)+ H2 (g)⇌Si (s) + 3HCl (g) ΔH >0,其平衡常数表达式为K =
(3)该流程中可以循环使用的物质是
(4)SiCl4与上述流程中的单质发生化合反应,可以制得SiHCl3,其化学方程式为
您最近一年使用:0次
【推荐1】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是___________ ;(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯B.坩埚C.表面皿D.泥三角E.酒精灯F.干燥器
(2)步骤③的实验操作名称是___________ ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是___________ 。
(3)步骤⑤中,某学生选择用苯来提取碘的理由是___________
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:___________

请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是
A.烧杯B.坩埚C.表面皿D.泥三角E.酒精灯F.干燥器
(2)步骤③的实验操作名称是
(3)步骤⑤中,某学生选择用苯来提取碘的理由是
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】海带中含有碘元素,从海带中提取碘的实验过程如下图所示。

(1)步骤①会用到下列仪器中的_______(填字母)。
(2)海带灰悬浊液含有I-。步骤④的试剂选用 、稀硫酸,离子方程式是
、稀硫酸,离子方程式是_______ 。
(3)步骤⑤“提取”包含以下四个过程。

①过程I使用的 体积明显小于含I2溶液,即可使I2几乎完全地转移至
体积明显小于含I2溶液,即可使I2几乎完全地转移至 中,推测I2在
中,推测I2在_______ (填“ ”或“
”或“ ”)中的溶解度更大。
”)中的溶解度更大。
②I2与 浓溶液反应的离子方程式是
浓溶液反应的离子方程式是_______ 。
③过程I→过程III的目的是_______ 。

(1)步骤①会用到下列仪器中的_______(填字母)。
| A.酒精灯 | B.漏斗 | C.坩埚 | D.泥三角 |
 、稀硫酸,离子方程式是
、稀硫酸,离子方程式是(3)步骤⑤“提取”包含以下四个过程。

①过程I使用的
 体积明显小于含I2溶液,即可使I2几乎完全地转移至
体积明显小于含I2溶液,即可使I2几乎完全地转移至 中,推测I2在
中,推测I2在 ”或“
”或“ ”)中的溶解度更大。
”)中的溶解度更大。②I2与
 浓溶液反应的离子方程式是
浓溶液反应的离子方程式是③过程I→过程III的目的是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐3】碘是人体必须的微量元素之一,海洋植物如海带、海藻中含有丰富的碘元素。在实验室中,从海藻里提取碘的流程如图:

(1)上述过程中步骤i实验操作的名称:___ 。
(2)①步骤ii中,氧化剂可使用Cl2,从原子结构角度说明理由___ 。
②当Cl2过量时,会有IO 产生,用离子方程式表示这一变化
产生,用离子方程式表示这一变化___ 。
(3)步骤ii中,当使用H2O2做氧化剂时,I-的转化率受外界因素的影响如图所示。

①图1中,pH=7时I-转化率几乎为0,结合离子方程式解释原因:___ 。
②图2中,T2后I-的转化率明显减小,可能的原因是___ 。

(1)上述过程中步骤i实验操作的名称:
(2)①步骤ii中,氧化剂可使用Cl2,从原子结构角度说明理由
②当Cl2过量时,会有IO
 产生,用离子方程式表示这一变化
产生,用离子方程式表示这一变化(3)步骤ii中,当使用H2O2做氧化剂时,I-的转化率受外界因素的影响如图所示。

①图1中,pH=7时I-转化率几乎为0,结合离子方程式解释原因:
②图2中,T2后I-的转化率明显减小,可能的原因是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验(一) 碘含量的测定

取100.00 mL 海带浸取原液于锥形瓶中,用 0.0100 mol•L-1的AgNO3标准溶液测定其中的碘,消耗标准溶液体积的平均值为20.00 mL。
(1)仪器A 的名称为___________ ;所用仪器B为___________ 。
(2)计算海带中碘的百分含量为___________ %(保留3位有效数字)。
实验(二) 碘的制取
另取海带浸取原液,甲、乙两种实验方案如下:
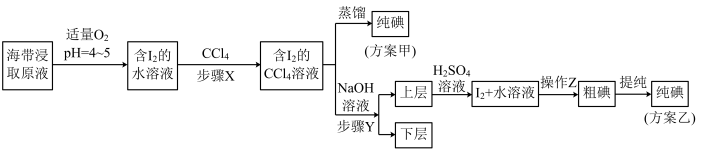
已知:3I2+6NaOH=5NaI+NaIO3+3H2O,酸性条件下I2在水中的溶解度很小。
(3)“适量O2”中能代替O2的最佳物质的电子式为___________ 。
(4)下列有关步骤Y 的说法中正确的是___________ (填选项字母),步骤Y 中的方法称为___________ 。
A.应控制 NaOH 溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除浸取原液中的有机杂质
D.NaOH 溶液可由乙醇代替
(5)方案乙中液体中加入 H2SO4溶液,反应的离子方程式为__________________ ,其中操作Z的名称是___________ 。
实验(一) 碘含量的测定

取100.00 mL 海带浸取原液于锥形瓶中,用 0.0100 mol•L-1的AgNO3标准溶液测定其中的碘,消耗标准溶液体积的平均值为20.00 mL。
(1)仪器A 的名称为
(2)计算海带中碘的百分含量为
实验(二) 碘的制取
另取海带浸取原液,甲、乙两种实验方案如下:

已知:3I2+6NaOH=5NaI+NaIO3+3H2O,酸性条件下I2在水中的溶解度很小。
(3)“适量O2”中能代替O2的最佳物质的电子式为
(4)下列有关步骤Y 的说法中正确的是
A.应控制 NaOH 溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除浸取原液中的有机杂质
D.NaOH 溶液可由乙醇代替
(5)方案乙中液体中加入 H2SO4溶液,反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某化学兴趣小组利用二氧化锰、浓盐酸、石灰乳等试剂制取少量漂白粉,设计了如下实验装置。

请回答下列问题:
(1)根据提供的试剂,写出实验室制 的离子方程式:
的离子方程式:___________ 。
(2)为提高漂白粉有效成分的含量,A中盛放的溶液是___________ ,作用是___________ 。
(3)B中制取漂白粉的化学方程式为___________ ,若反应中每转移 的
的 ,消耗标准状况下氯气的体积为
,消耗标准状况下氯气的体积为___________ L。
(4)C中 溶液的作用为
溶液的作用为___________ 。
(5)制取漂白粉的反应为放热反应,当温度较高时,氯气与石灰乳反应生成 ,为避免此副反应的发生,可采取的措施为
,为避免此副反应的发生,可采取的措施为___________ 。

请回答下列问题:
(1)根据提供的试剂,写出实验室制
 的离子方程式:
的离子方程式:(2)为提高漂白粉有效成分的含量,A中盛放的溶液是
(3)B中制取漂白粉的化学方程式为
 的
的 ,消耗标准状况下氯气的体积为
,消耗标准状况下氯气的体积为(4)C中
 溶液的作用为
溶液的作用为(5)制取漂白粉的反应为放热反应,当温度较高时,氯气与石灰乳反应生成
 ,为避免此副反应的发生,可采取的措施为
,为避免此副反应的发生,可采取的措施为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】某同学设计用如图所示装置制备少量的 .已知:①无水氯化铝在
.已知:①无水氯化铝在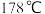 升华.②氯化铝极易吸收水分形成酸雾.请回答下列问题:
升华.②氯化铝极易吸收水分形成酸雾.请回答下列问题:

(1)写出装置A中发生反应的化学方程式:______________ .
(2)实验开始时,正确的操作步骤是______________ (填序号).
Ⅰ.先打开旋塞 和
和 ,再点燃
,再点燃 处酒精灯,最后点燃
处酒精灯,最后点燃 处酒精灯
处酒精灯
Ⅱ.先打开旋塞 和
和 ,再点燃
,再点燃 处酒精灯,最后点燃
处酒精灯,最后点燃 处酒精灯
处酒精灯
(3)装置 和装置
和装置 中所加试剂依次是
中所加试剂依次是______________ 、______________ .
(4)装置 的作用是
的作用是____________________________ .
(5)H处可以选择的装置是______________ (仅选一种,填字母,下同),可以用装置______________ 替换掉装置G和H.

(6)装置中存在的一处安全隐患是 升华后遇冷凝华,在装置
升华后遇冷凝华,在装置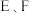 连接的细导管处容易发生堵塞,引起危险,因此装置B的用途是
连接的细导管处容易发生堵塞,引起危险,因此装置B的用途是______________ ,除此以外装置 的用途还有
的用途还有______________ .
 .已知:①无水氯化铝在
.已知:①无水氯化铝在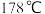 升华.②氯化铝极易吸收水分形成酸雾.请回答下列问题:
升华.②氯化铝极易吸收水分形成酸雾.请回答下列问题:
(1)写出装置A中发生反应的化学方程式:
(2)实验开始时,正确的操作步骤是
Ⅰ.先打开旋塞
 和
和 ,再点燃
,再点燃 处酒精灯,最后点燃
处酒精灯,最后点燃 处酒精灯
处酒精灯Ⅱ.先打开旋塞
 和
和 ,再点燃
,再点燃 处酒精灯,最后点燃
处酒精灯,最后点燃 处酒精灯
处酒精灯(3)装置
 和装置
和装置 中所加试剂依次是
中所加试剂依次是(4)装置
 的作用是
的作用是(5)H处可以选择的装置是

(6)装置中存在的一处安全隐患是
 升华后遇冷凝华,在装置
升华后遇冷凝华,在装置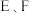 连接的细导管处容易发生堵塞,引起危险,因此装置B的用途是
连接的细导管处容易发生堵塞,引起危险,因此装置B的用途是 的用途还有
的用途还有
您最近一年使用:0次



