X、Y、Z、W、T是原子序数依次增大的五种短周期元素,且X、Y、Z、W的原子序数之和为32。其中X是元素周期表中原子半径最小的元素,Y、Z左右相邻,Z、W位于同一主族。T的单质常用于自来水的杀菌消毒。请回答下列问题:
(1)W元素在周期表中的位置为_____ 。
(2)由X、Y、Z、W四种元素中的三种组成一种强酸,该强酸的稀溶液能与金属铜反应,该反应的离子方程式为_____ 。
(3)Y元素的气态氢化物与其最高价氧化物的水化物可以相互反应,写出其离子方程式:_____ 。
(4)Y和T两元素的非金属性强弱为Y_____ T(填“>”“<”或者“=”),可以验证该结论的方法是_____ 。
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素所形成含氧酸的酸性
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素与氢气化合的难易程度
E.比较这两种元素气态氢化物的还原性
(1)W元素在周期表中的位置为
(2)由X、Y、Z、W四种元素中的三种组成一种强酸,该强酸的稀溶液能与金属铜反应,该反应的离子方程式为
(3)Y元素的气态氢化物与其最高价氧化物的水化物可以相互反应,写出其离子方程式:
(4)Y和T两元素的非金属性强弱为Y
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素所形成含氧酸的酸性
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素与氢气化合的难易程度
E.比较这两种元素气态氢化物的还原性
更新时间:2020-03-14 13:50:17
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子。Y元素原子的最外层2p轨道上有2个未成对电子,X跟Y可形成化合物X2Y3。Z元素可以形成负一价离子。请回答下列问题:
(1)X元素基态原子的电子排布式为_________ ,该元素的符号是____ 。
(2)Y元素原子的价层电子排布图为_________ ,该元素的名称是____ 。
(3)已知化合物X2Y3在稀硫酸中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是___________ 。
(1)X元素基态原子的电子排布式为
(2)Y元素原子的价层电子排布图为
(3)已知化合物X2Y3在稀硫酸中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】利用元素周期律和元素周期表可以系统研究元素的性质。几种主族元素在周期表中的位置如下,回答下列问题:
(1)元素⑥形成的单质的电子式是___________ 。
(2)⑥、⑦、⑨三种元素的简单气态氢化物中,稳定性最弱的是___________ (填化学式)。
(3)④、⑦、⑧三种元素的简单离子半径由大到小的顺序是___________ (用离子符号表示)。
(4)①和⑦可分别形成10电子和18电子分子,其中18电子分子是___________ (填化学式)。
(5)比较元素⑧和⑩的非金属性强弱:在⑧的氢化物的水溶液中通入少量⑩的单质,写出发生反应的化学方程式:___________ 。
(6)元素①和③形成的化合物能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,该反应的氧化产物为___________ (填化学式)。
(7)工业上利用⑩的单质制取漂白粉,反应的化学方程式为___________ 。
(8)结合元素周期律,根据下列事实所得推测不合理的是___________ (填字母)。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ⑥ | ⑦ | ⑨ | |||||
| 3 | ② | ④ | ⑤ | ⑧ | ⑩ | |||
| 4 | ③ | |||||||
(2)⑥、⑦、⑨三种元素的简单气态氢化物中,稳定性最弱的是
(3)④、⑦、⑧三种元素的简单离子半径由大到小的顺序是
(4)①和⑦可分别形成10电子和18电子分子,其中18电子分子是
(5)比较元素⑧和⑩的非金属性强弱:在⑧的氢化物的水溶液中通入少量⑩的单质,写出发生反应的化学方程式:
(6)元素①和③形成的化合物能与水反应生成氢气,在反应后的溶液中滴入酚酞,溶液变红,该反应的氧化产物为
(7)工业上利用⑩的单质制取漂白粉,反应的化学方程式为
(8)结合元素周期律,根据下列事实所得推测不合理的是
| 选项 | 事实 | 推测 |
| A | 随核电荷数递增,第ⅠA族的碱金属元素单质的沸点逐渐降低 | 随核电荷数递增,第ⅦA族元素单质的沸点也逐渐降低 |
| B |  、 、 均为强碱 均为强碱 |  (氢氧化锶)是强碱 (氢氧化锶)是强碱 |
| C |  与 与 在暗处剧烈化合, 在暗处剧烈化合, 与 与 光照或点燃时反应 光照或点燃时反应 |  与 与 在常温下即可反应 在常温下即可反应 |
| D | 第ⅣA族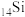 和 和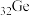 的单质是半导体材料 的单质是半导体材料 | 同族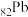 的单质是半导体材料 的单质是半导体材料 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分:
请填写下列空白:
(1)表中元素,原子半径最大的是___ (填元素符号);①的核外电子排布式___ ,④的M层上有___ 种不同能级的电子。③和⑥两元素形成化合物的电子式为___ 。
(2)②③④三种元素最高价氧化物对应的水化物中,碱性最强的是___ (填化学式)。
(3)比较④、⑤两种元素的简单离子半径:___ (填离子符号);元素④最高价氧化物对应的水化物与硝酸反应的离子方程式为___ 。
(4)列举一个事实来证明元素①比元素⑤的非金属性强___ 。
(5)若8g甲烷气体完全燃烧生成液态水时放出445.15kJ的热量,请写出其热化学方程式___ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | ||
| 二 | C | N | ① | |||||
| 三 | ② | ③ | ④ | P | ⑤ | ⑥ |
请填写下列空白:
(1)表中元素,原子半径最大的是
(2)②③④三种元素最高价氧化物对应的水化物中,碱性最强的是
(3)比较④、⑤两种元素的简单离子半径:
(4)列举一个事实来证明元素①比元素⑤的非金属性强
(5)若8g甲烷气体完全燃烧生成液态水时放出445.15kJ的热量,请写出其热化学方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置。
Ⅰ.第一代电池的光电转换材料是单晶硅。某单晶硅制备工艺中涉及的主要物质转化如下:________ (填字母)。
a.ⅰ中,C做还原剂 b.碳酸的酸性强于硅酸
c.碳酸的热稳定性弱于硅酸 d.元素的电负性C>Si
(2)ⅱ中,1molSi与3molHCl反应转移4mole-。
①SiHCl3中,H的化合价为________ ,电负性Si________ H(填“>”或“<”)。
②该反应的化学方程式为________ 。
(3)ⅲ中,利用物质沸点差异,可直接实现高纯硅与SiHCl3的分离,从晶体类型角度解释其原因:________ 。
Ⅱ.第二代电池的光电转换材料是一种无机物薄膜,其光电转化率高于单晶硅。
科学家在元素周期表中Si的附近寻找到元素Ga和As(它们在周期表中的位置如图),并制成它们的化合物薄膜,其晶体结构类似单晶硅。
(4)写出基态Ga原子价层电子排布式________ 。
(5)As的第一电离能比Se大的主要原因是:________________ 。
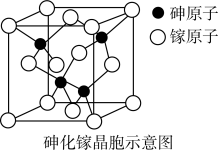
(6)下图为砷化镓晶胞示意图,写出其化学式________ 。
Ⅰ.第一代电池的光电转换材料是单晶硅。某单晶硅制备工艺中涉及的主要物质转化如下:
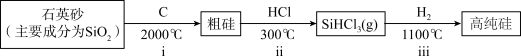
a.ⅰ中,C做还原剂 b.碳酸的酸性强于硅酸
c.碳酸的热稳定性弱于硅酸 d.元素的电负性C>Si
(2)ⅱ中,1molSi与3molHCl反应转移4mole-。
①SiHCl3中,H的化合价为
②该反应的化学方程式为
(3)ⅲ中,利用物质沸点差异,可直接实现高纯硅与SiHCl3的分离,从晶体类型角度解释其原因:
Ⅱ.第二代电池的光电转换材料是一种无机物薄膜,其光电转化率高于单晶硅。
科学家在元素周期表中Si的附近寻找到元素Ga和As(它们在周期表中的位置如图),并制成它们的化合物薄膜,其晶体结构类似单晶硅。
| Si | |||
| Ga | As | Se |
(4)写出基态Ga原子价层电子排布式
(5)As的第一电离能比Se大的主要原因是:
(6)下图为砷化镓晶胞示意图,写出其化学式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是部分元素周期表的结构图,表中每一个序号代表一种元素。请根据要求回答下列问题。
(1)①在周期表中的位置是___________ 。
(2)②、③、④、⑤四种元素的离子半径最小的是___________ (写离子符号)。
(3)①和②可形成两种化合物,用电子式分别为___________ 、___________ 。
(4)②的最高价氧化物的水化物与④的单质发生反应的离子方程式为___________ 。
(5)下列事实能判断②和③的金属性强弱的是___________ (填字母)。
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(6)硒(Se)位于第四周期,与①同主族。下列推断正确的是___________ (填字母)。
a.SeO2只具有还原性
b.Se的最低负化合价是-2价
c.Se的气态氢化物的稳定性比①的强
室温下向SeO2固体表面吹入NH3,得到两种单质和H2O,该反应的化学方程式为___________ 。
| ① | ||||||||
| ② | ③ | ④ | ⑤ | |||||
(2)②、③、④、⑤四种元素的离子半径最小的是
(3)①和②可形成两种化合物,用电子式分别为
(4)②的最高价氧化物的水化物与④的单质发生反应的离子方程式为
(5)下列事实能判断②和③的金属性强弱的是
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(6)硒(Se)位于第四周期,与①同主族。下列推断正确的是
a.SeO2只具有还原性
b.Se的最低负化合价是-2价
c.Se的气态氢化物的稳定性比①的强
室温下向SeO2固体表面吹入NH3,得到两种单质和H2O,该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下表列出了①~⑨十种元素在周期表中的位置:
请按要求回答下列问题:
(1)⑧的名称是___________ ,1molD2O含有的中子个数为___________ 。
(2)上述元素中,最高价氧化物对应水化物酸性最强的是___________ (写出酸的化学式)。
(3)由④、⑤、⑦四种元素形成的简单离子半径由大到小的顺序是:___________ 。(用离子符号表示)
(4)元素①,④以原子个数比为1∶1形成的化合物中含有化学键的类型为___________ 。(填“极性共价键”或“非极性共价键”或“离子键”)
(5)元素①、④、⑨以原子个数比为1∶1∶1形成的化合物的电子式为___________ 。
(6)19.2g金属铜与③的最高价氧化物的水化物反应生成还原产物 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。
(7)可以比较⑤、⑥两元素金属性强弱的实验是___________。
| 族周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)⑧的名称是
(2)上述元素中,最高价氧化物对应水化物酸性最强的是
(3)由④、⑤、⑦四种元素形成的简单离子半径由大到小的顺序是:
(4)元素①,④以原子个数比为1∶1形成的化合物中含有化学键的类型为
(5)元素①、④、⑨以原子个数比为1∶1∶1形成的化合物的电子式为
(6)19.2g金属铜与③的最高价氧化物的水化物反应生成还原产物
 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(7)可以比较⑤、⑥两元素金属性强弱的实验是___________。
| A.比较这两种元素最高价氧化物对应的水化物的碱性 |
| B.将⑤的单质投入到⑥的盐溶液中 |
| C.将这两种元素的单质分别放入冷水中 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知1-20号元素中A、B、C、D、E、F、G元素原子质子数依次增大,A的某种同位素可用于考古测定文物年代;C最外层电子数是次外层的3倍;D的阳离子是同周期元素形成的阳离子中半径最大的,E的阳离子为同周期中最小的;F最高正价与最低负价代数和为6;G的原子核外K、M层电子数之和等于L、N层电子数之和,试推断:
(1)元素的名称:B_______ D______ G在周期表中的位置_____
(2)写出含有10个中子的C元素的原子符号________
(3)B、E、F、G形成的简单离子的半径由大到小排序__________ (用元素符号表示)
(4)在A、B元素各自形成的氢化物中,稳定性较差的氢化物的化学式为____ ,原因为是_____ ;其氢化物中沸点较高的化学式为________ ,原因是______ 。
(5)C可与氢元素形成四核18电子的物质,其电子式为______ ,含有的化学键类型_____ 。
(6)E的最高价氧化物对应的水化物可与G的最高价氧化物对应的水化物发生反应的离子方程式为____ 。
(7)D与周期表中非金属性最强的元素可形成化合物X,用电子式表示X的形成过程_______ 。
(1)元素的名称:B
(2)写出含有10个中子的C元素的原子符号
(3)B、E、F、G形成的简单离子的半径由大到小排序
(4)在A、B元素各自形成的氢化物中,稳定性较差的氢化物的化学式为
(5)C可与氢元素形成四核18电子的物质,其电子式为
(6)E的最高价氧化物对应的水化物可与G的最高价氧化物对应的水化物发生反应的离子方程式为
(7)D与周期表中非金属性最强的元素可形成化合物X,用电子式表示X的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】现有五种元素A、B、C、D、E,其中A、B、C为三个不同周期的短周期元素,E为第四周期元素。请根据下列相关信息,回答下列问题:
(1)C基态原子中能量最高的电子,其电子云在空间有___________ 个伸展方向,C简单离子核外有___________ 种运动状态不同的电子。
(2)A2B2难溶于CS2,简要说明理由:______________ 。
(3)ED3分子的VSEPR模型名称为____________ ,空间构型为____________ 。
(4)下列气态分子BCl3、CCl4、H2O和BeCl2中,其键角由大到小的顺序为_____________ 。
(5)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度:RCO﹣>﹣F>﹣Cl>﹣Br>﹣I>﹣C≡CH>﹣C6H5>﹣H,则下列物质酸性由强到弱的顺序是___________ (填序号)。
A.CH3COOH B.ClCH2COOH C.HC≡CCH2COOH D.C6H5CH2COOH
元素 | 相关信息 |
A | 核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
B | 原子核外p电子数与s电子数相等 |
C | 基态原子的价电子排布为nsn-1npn+1 |
D | 能层数与C相同,且电负性比C大 |
E | 元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
(2)A2B2难溶于CS2,简要说明理由:
(3)ED3分子的VSEPR模型名称为
(4)下列气态分子BCl3、CCl4、H2O和BeCl2中,其键角由大到小的顺序为
(5)键的极性对物质的化学性质有重要影响。已知一些常见电子基团的吸电子效应的强度:RCO﹣>﹣F>﹣Cl>﹣Br>﹣I>﹣C≡CH>﹣C6H5>﹣H,则下列物质酸性由强到弱的顺序是
A.CH3COOH B.ClCH2COOH C.HC≡CCH2COOH D.C6H5CH2COOH
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】某玉石由短周期主族元素W、X、Y、Z组成,且W、X、Y、Z的原子序数依次增大。W与Y同主族,W与X同周期。W、Y、Z的最外层电子数之和与X的最外层电子数相等,Z的最外层电子数是X电子总数的一半。回答下列问题:
(1)Z在元素周期表中的位置是___________ 。
(2)该玉石的成分是 ,若
,若 的化学式可以写成
的化学式可以写成 二元化合物组合的形式,则该玉石的成分用二元化合物组合的形式可以写成
二元化合物组合的形式,则该玉石的成分用二元化合物组合的形式可以写成___________ 。
(3)已知Z的单质可以溶于Y的氧化物对应的水化物溶液中,该过程发生反应的离子方程式是___________ 。
(4)四种元素的单质及其化合物广泛应用于电池、通信等领域。
①Z的单质常用作___________ 材料(填一种,下同);X和Z组成的化合物常用作___________ 材料。
②W离子电池比Y离子电池有更好的储能优势,其原因是___________ 。在W离子电池中,W离子嵌入石墨形成复合材料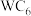 ,该材料是电池的负极材料,当电池部分放电释放出x个W离子时,该电极反应式是
,该材料是电池的负极材料,当电池部分放电释放出x个W离子时,该电极反应式是___________ 。
(1)Z在元素周期表中的位置是
(2)该玉石的成分是
 ,若
,若 的化学式可以写成
的化学式可以写成 二元化合物组合的形式,则该玉石的成分用二元化合物组合的形式可以写成
二元化合物组合的形式,则该玉石的成分用二元化合物组合的形式可以写成(3)已知Z的单质可以溶于Y的氧化物对应的水化物溶液中,该过程发生反应的离子方程式是
(4)四种元素的单质及其化合物广泛应用于电池、通信等领域。
①Z的单质常用作
②W离子电池比Y离子电池有更好的储能优势,其原因是
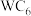 ,该材料是电池的负极材料,当电池部分放电释放出x个W离子时,该电极反应式是
,该材料是电池的负极材料,当电池部分放电释放出x个W离子时,该电极反应式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、W是元素周期表中的短周期元素,它们的相对位置如下表所示,其中X、Y 元素均能形成10电子的氢化物,Z的原子序数是Y的2倍。请回答下列问题:
(1)W的简单离子的结构示意图为______ ,Y元素在周期表中的位置是____ 。
(2)写出实验室制W元素单质的离子方程式:___________
(3)关于W同主族元素,下列说法正确的是:__________
A.从上到下密度逐渐增大
B.从上到下熔点和沸点都逐渐升高
C.从上到下元素的非金属性越来越强
D.同主族元素对应的单质中,只有W元素对应的单质在常态下为气态
(4)W与Z形成的液体化合物Z2W2,该物质可与水反应生成ZO2气体,1 mol Z2W2参加反应时转移1.5 mol电子,其中只有一种元素化合价发生改变,Z2W2与水反应的化学方程式为_____ 。
| X | Y | |
| Z | W |
(1)W的简单离子的结构示意图为
(2)写出实验室制W元素单质的离子方程式:
(3)关于W同主族元素,下列说法正确的是:
A.从上到下密度逐渐增大
B.从上到下熔点和沸点都逐渐升高
C.从上到下元素的非金属性越来越强
D.同主族元素对应的单质中,只有W元素对应的单质在常态下为气态
(4)W与Z形成的液体化合物Z2W2,该物质可与水反应生成ZO2气体,1 mol Z2W2参加反应时转移1.5 mol电子,其中只有一种元素化合价发生改变,Z2W2与水反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E为五中短周期元素,且原子序数依次增大,五种元素原子序数之和为39,B、C同周期,A、D同主族,A、C能形成两种液态化合物A2C和A2C2,E元素的周期序数与主族序数相等。
(1)A2C的结构式为___________ 。
(2)B中质子数和中子数相等的核素符号为___________ ,E元素在周期表中的位置为___________ 。
(3)C、D、E三种元素的简单离子半径由小到大的顺序为___________ (填离子符号)。
(4)在一定条件下,D元素的单质能与A元素的单质化合生成DA,DA能与水反应放氢气,则其化学方程式为___________ ,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是___________ L(标准状况下)。
(5)若要比较D和E的金属性强弱,下列实验方法可行的是___________ 。
a. 将D单质置于E的盐溶液中,若单质D不能置换出单质E,说明D的金属性弱。
b. 将少量D、E的单质分别投入到水中,若D反应而E不反应,说明D的金属性强。
c.比较相同条件下D和E的最高价氧化物对应水化物的溶解性若前者比后者溶解度大,说明D的金属性强。
(1)A2C的结构式为
(2)B中质子数和中子数相等的核素符号为
(3)C、D、E三种元素的简单离子半径由小到大的顺序为
(4)在一定条件下,D元素的单质能与A元素的单质化合生成DA,DA能与水反应放氢气,则其化学方程式为
(5)若要比较D和E的金属性强弱,下列实验方法可行的是
a. 将D单质置于E的盐溶液中,若单质D不能置换出单质E,说明D的金属性弱。
b. 将少量D、E的单质分别投入到水中,若D反应而E不反应,说明D的金属性强。
c.比较相同条件下D和E的最高价氧化物对应水化物的溶解性若前者比后者溶解度大,说明D的金属性强。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、X、W、D、E为短周期元素,且原子序数依次增大。A、D同主族,X、W同周期, X形成的气态氢化物可使湿润的红色石蕊试纸变蓝, A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为______________________ 。W的原子结构示意图为________ 。
(2)A、X 两种元素能形成含18电子的分子,请写出该分子的电子式:_______________ 。
用电子式表示化合物D2W的形成过程______________________________________ 。
(3)下列事实能说明W元素的非金属性比S元素的非金属性强的是________ (填字母)。
a.W单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1 mol W单质比1 mol S得电子多
c.W和S两元素的简单氢化物受热分解,前者的分解温度高
(4)实验室制备A和X形成的气态化合物的化学方程式为____________________________ 。
(5)经测定A2W2为二元弱酸,其酸性比碳酸的还要弱,请写出其第一步电离的电离方程式_________________________________________________________________________ 。
(6)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现在改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式________________________________________________________________ 。
(1)E元素在周期表中的位置为
(2)A、X 两种元素能形成含18电子的分子,请写出该分子的电子式:
用电子式表示化合物D2W的形成过程
(3)下列事实能说明W元素的非金属性比S元素的非金属性强的是
a.W单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1 mol W单质比1 mol S得电子多
c.W和S两元素的简单氢化物受热分解,前者的分解温度高
(4)实验室制备A和X形成的气态化合物的化学方程式为
(5)经测定A2W2为二元弱酸,其酸性比碳酸的还要弱,请写出其第一步电离的电离方程式
(6)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现在改用A2W2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出反应的离子方程式
您最近一年使用:0次



