氯及其化合物在工农业生产和人类生活中有着重要的作用。回答下列问题:
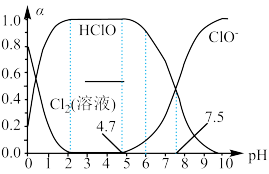
(1)25℃时将氯气溶于水形成“氯气-氯水”体系,该体系存在多个含氯元素的平衡关系,其中之一为:Cl2(溶液)+H2O HClO+H++Cl-,体系中Cl2(溶液)、HClO和ClO-三者的物质的量分数(α)随pH(酸碱度)变化的关系如图所示。已知HClO的杀菌能力比ClO-强,用氯气处理饮用水时,杀菌效果最强的pH范围为
HClO+H++Cl-,体系中Cl2(溶液)、HClO和ClO-三者的物质的量分数(α)随pH(酸碱度)变化的关系如图所示。已知HClO的杀菌能力比ClO-强,用氯气处理饮用水时,杀菌效果最强的pH范围为__ (填字母)。
A.0~2 B.2~4.7 C.4.7~7.5 D.7.5~10
(2)写出次氯酸光照分解的化学方程式___ ,如果在家中直接使用自来水养金鱼,除去其中残留的次氯酸可采取的简易措施为__ 。
(3)NaClO、NaClO2、ClO2等含氯化合物都是常见的消毒剂,这是因为它们都具有强氧化性。
①写出工业上用氯气和NaOH溶液生产消毒剂NaClO的化学方程式___ ;
②84消毒液(主要成分是NaClO)与洁厕灵(主要成分是盐酸)混在一起使用会产生有毒气体Cl2,其反应的离子方程式为__ ;
③NaClO2中Cl元素化合价为__ ;
④ClO2的杀菌效果比Cl2好,等物质的量的ClO2杀菌效果是Cl2的__ 倍(杀菌效果与单位物质的量的氧化剂得电子的物质的量有关,ClO2与Cl2消毒杀菌后均被还原为Cl-)。
(1)25℃时将氯气溶于水形成“氯气-氯水”体系,该体系存在多个含氯元素的平衡关系,其中之一为:Cl2(溶液)+H2O
 HClO+H++Cl-,体系中Cl2(溶液)、HClO和ClO-三者的物质的量分数(α)随pH(酸碱度)变化的关系如图所示。已知HClO的杀菌能力比ClO-强,用氯气处理饮用水时,杀菌效果最强的pH范围为
HClO+H++Cl-,体系中Cl2(溶液)、HClO和ClO-三者的物质的量分数(α)随pH(酸碱度)变化的关系如图所示。已知HClO的杀菌能力比ClO-强,用氯气处理饮用水时,杀菌效果最强的pH范围为A.0~2 B.2~4.7 C.4.7~7.5 D.7.5~10

(2)写出次氯酸光照分解的化学方程式
(3)NaClO、NaClO2、ClO2等含氯化合物都是常见的消毒剂,这是因为它们都具有强氧化性。
①写出工业上用氯气和NaOH溶液生产消毒剂NaClO的化学方程式
②84消毒液(主要成分是NaClO)与洁厕灵(主要成分是盐酸)混在一起使用会产生有毒气体Cl2,其反应的离子方程式为
③NaClO2中Cl元素化合价为
④ClO2的杀菌效果比Cl2好,等物质的量的ClO2杀菌效果是Cl2的
更新时间:2020-03-14 11:29:14
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氨催化氧化法是工业生产中制取硝酸的主要途径。
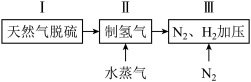
(1)合成氨原料气可由以下方法得到,步骤II在催化剂作用下反应的化学方程式为:_______ 。
(2)以氨气、氧气为原料,在催化剂存在下生成NO和副产物 的化学方程式如下:
的化学方程式如下:
I:
II:
催化氧化时,有关物质的产率与温度的关系如图
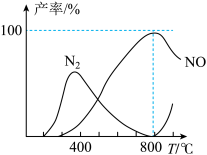
①该催化剂在低温时对反应_______ (填“I”或“II”)的选择性更好。
②温度高于800℃后,副产物 的产率增大的原因可能是
的产率增大的原因可能是_______ 。
(3)氧气与氨气的物质的量之比是影响催化氧化和后续反应的重要因素,催化氧化时加入氧气与氨气的物质的量之比应_______ (填“大于”或“等于”或“小于”)5:4,原因是_______ 。
(4)某合成氨工业废水中含有一定量的氨氮(以 、
、 形式存在),pH约为6时,用NaClO可将废水中的氨氮转化为
形式存在),pH约为6时,用NaClO可将废水中的氨氮转化为 。
。
①NaClO将废水中的 转化为
转化为 的离子方程式为
的离子方程式为_______ 。
②研究发现,当温度高于30℃时,废水中氨氮去除率随着温度升高而降低,其原因是_______ 。
(5)铁触媒(+2价铁和+3价铁组成的氧化物)是工业合成氨的催化剂。某学习小组用下列流程测定铁触媒的含铁量(25.00mL稀释后的溶液不含有 )。根据题意回答相关问题:
)。根据题意回答相关问题:
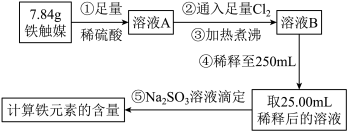
步骤⑤消耗 的
的 溶液25.00mL,则铁触媒中铁元素的质量分数为
溶液25.00mL,则铁触媒中铁元素的质量分数为_______ 。
(1)合成氨原料气可由以下方法得到,步骤II在催化剂作用下反应的化学方程式为:

(2)以氨气、氧气为原料,在催化剂存在下生成NO和副产物
 的化学方程式如下:
的化学方程式如下:I:

II:

催化氧化时,有关物质的产率与温度的关系如图

①该催化剂在低温时对反应
②温度高于800℃后,副产物
 的产率增大的原因可能是
的产率增大的原因可能是(3)氧气与氨气的物质的量之比是影响催化氧化和后续反应的重要因素,催化氧化时加入氧气与氨气的物质的量之比应
(4)某合成氨工业废水中含有一定量的氨氮(以
 、
、 形式存在),pH约为6时,用NaClO可将废水中的氨氮转化为
形式存在),pH约为6时,用NaClO可将废水中的氨氮转化为 。
。①NaClO将废水中的
 转化为
转化为 的离子方程式为
的离子方程式为②研究发现,当温度高于30℃时,废水中氨氮去除率随着温度升高而降低,其原因是
(5)铁触媒(+2价铁和+3价铁组成的氧化物)是工业合成氨的催化剂。某学习小组用下列流程测定铁触媒的含铁量(25.00mL稀释后的溶液不含有
 )。根据题意回答相关问题:
)。根据题意回答相关问题:
步骤⑤消耗
 的
的 溶液25.00mL,则铁触媒中铁元素的质量分数为
溶液25.00mL,则铁触媒中铁元素的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)由5.6gCO、4.4gCO2及0.4gH2组成的混合气体的平均摩尔质量是____________ ;该混合气体相对于O2的密度为_________ ;该混合气体中CO的物质的量分数是__________ 。
(2)焦亚硫酸钠(Na2S2O5)是常用食品抗氧化剂,常用于葡萄酒、果脯等食品中。Na2S2O5中硫元素的化合价是_________ ,焦亚硫酸钠在空气中久置会被氧化生成连二硫酸钠(Na2S2O6),写出该反应的化学方程式__________________________________________ 。
(3)葡萄酒中的 Na2S2O5的使用量是以游离的 SO2 来计算的。我国规定每升葡萄酒中SO2的最高含量是 0.25g,则一瓶 800mL 的葡萄酒中 SO2的物质的量不能超过______ (精确到 0.001 )。
(2)焦亚硫酸钠(Na2S2O5)是常用食品抗氧化剂,常用于葡萄酒、果脯等食品中。Na2S2O5中硫元素的化合价是
(3)葡萄酒中的 Na2S2O5的使用量是以游离的 SO2 来计算的。我国规定每升葡萄酒中SO2的最高含量是 0.25g,则一瓶 800mL 的葡萄酒中 SO2的物质的量不能超过
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)甲、乙两位同学想探究铝电极在原电池中的作用,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸中,乙同学将电极放入NaOH溶液中,实验装置如图所示。
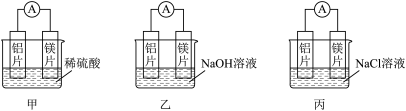
①写出甲中电池总反应的离子方程式:_______ 。
②乙中铝为_______ 极,写出铝电极的电极反应式:_______ 。
③甲同学后来继续按图丙进行实验,该装置_______ 产生电流。(填“会”或“不会”)。
(2)硅太阳能电池中用到硅。三氯甲硅烷( )还原法是当前制备高纯硅的主要方法,生产过程示意图如图:
)还原法是当前制备高纯硅的主要方法,生产过程示意图如图:
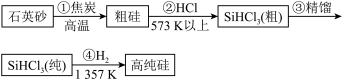
第①步制备粗硅的化学方程式为:_______ 。
 遇水剧烈反应生成
遇水剧烈反应生成 、HCl和另一种物质,写出
、HCl和另一种物质,写出 遇水的化学反应方程式:
遇水的化学反应方程式:_______ 。
(3)铜的电极可以用稀硝酸来用溶解,写出其反应的离子方程式_______ 。
(4)把盛有48mLNO和 混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为24mL,则原混合气中
混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为24mL,则原混合气中 是
是_______ mL。
(1)甲、乙两位同学想探究铝电极在原电池中的作用,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸中,乙同学将电极放入NaOH溶液中,实验装置如图所示。

①写出甲中电池总反应的离子方程式:
②乙中铝为
③甲同学后来继续按图丙进行实验,该装置
(2)硅太阳能电池中用到硅。三氯甲硅烷(
 )还原法是当前制备高纯硅的主要方法,生产过程示意图如图:
)还原法是当前制备高纯硅的主要方法,生产过程示意图如图:
第①步制备粗硅的化学方程式为:
 遇水剧烈反应生成
遇水剧烈反应生成 、HCl和另一种物质,写出
、HCl和另一种物质,写出 遇水的化学反应方程式:
遇水的化学反应方程式:(3)铜的电极可以用稀硝酸来用溶解,写出其反应的离子方程式
(4)把盛有48mLNO和
 混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为24mL,则原混合气中
混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为24mL,则原混合气中 是
是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按写出下列反应的方程式:
(1)钠投入氯化铁溶液中反应的离子方程式:______ 。
(2)过氧化钠与二氧化碳反应的化学方程式:______ 。
(3)氯气与水反应的离子方程式:______ 。
(4)漂白粉应密封避光保存,原因为______ 、______ (用化学方程式解释)。
(5)硫酸氢钠与氢氧化钡反应至溶液呈中性的离子方程式:______ 。
(6)氯酸钾和浓盐酸制氯气的化学方程式:______ 。
(7)“84消毒液”(主要成分是NaClO)与“洁厕灵”(主要成分为HCl)不能混用的原因(离子方程式):______ 。
(1)钠投入氯化铁溶液中反应的离子方程式:
(2)过氧化钠与二氧化碳反应的化学方程式:
(3)氯气与水反应的离子方程式:
(4)漂白粉应密封避光保存,原因为
(5)硫酸氢钠与氢氧化钡反应至溶液呈中性的离子方程式:
(6)氯酸钾和浓盐酸制氯气的化学方程式:
(7)“84消毒液”(主要成分是NaClO)与“洁厕灵”(主要成分为HCl)不能混用的原因(离子方程式):
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】H7N9型禽流感是一种新型禽流感,浙江自2015年入秋以来,已累计报告人感染H7N9禽流感4例。研究表明,该病毒对热敏感,煮沸2分钟以上即可失去活性,许多常用消毒药物如:高锰酸钾、漂白粉、氯气等,也都可以将该病毒杀灭。
(1)新制氯水中含有多种微粒,将紫色石蕊试液滴入氯水中,溶液显红色起作用的微粒是___________ ;过一会儿,溶液颜色逐渐褪去,起作用的微粒是______________ 。
请写出氯气与水反应的离子方程式_____________________ 。
(2)工业上制取漂白粉的反应方程式为:__________________ 。
(3)已知高锰酸钾与浓盐酸混合能产生氯气,化学反应方程式为:2KMnO4 + 16HCl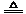 2MnCl2 + 2KCl + 8H2O + 5Cl2↑,该反应中氧化剂为
2MnCl2 + 2KCl + 8H2O + 5Cl2↑,该反应中氧化剂为____________ 。
(4)向漂白粉清液中滴加碳酸钠溶液,有白色沉淀生成,写出发生反应的离子方程式________________ 。
(1)新制氯水中含有多种微粒,将紫色石蕊试液滴入氯水中,溶液显红色起作用的微粒是
请写出氯气与水反应的离子方程式
(2)工业上制取漂白粉的反应方程式为:
(3)已知高锰酸钾与浓盐酸混合能产生氯气,化学反应方程式为:2KMnO4 + 16HCl
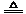 2MnCl2 + 2KCl + 8H2O + 5Cl2↑,该反应中氧化剂为
2MnCl2 + 2KCl + 8H2O + 5Cl2↑,该反应中氧化剂为(4)向漂白粉清液中滴加碳酸钠溶液,有白色沉淀生成,写出发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)。

(1)能证明氯水具有漂白性的是_______ (填“a”、“b”、“c”或“d”);
(2)c过程中的现象是_______ ;d过程中的现象是_______ ;e过程中的现象是_______ ;b过程中的离子方程式为_______ ;e过程的化学方程式_______ ;
(3)久置的氯水变为_______ ,用化学反应方程式表示为_______ ;
(4)实验室保存饱和氯水的方法是_______ 。

(1)能证明氯水具有漂白性的是
(2)c过程中的现象是
(3)久置的氯水变为
(4)实验室保存饱和氯水的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】电石(主要成分为 )是重要的基本化工原料,主要用于生产乙炔。回答下列问题:
)是重要的基本化工原料,主要用于生产乙炔。回答下列问题:
(1)碳元素在元素周期表中的位置为_______ ; 的电子式为
的电子式为_______ 。
(2)①目前工业上合成电石主要采用氧热法。
已知: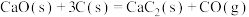
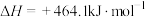 ;
;

 。
。
若不考虑热量耗散,物料转化率均为 ,最终炉中出来的气体只有
,最终炉中出来的气体只有 。则为了维持热平衡,每生产
。则为了维持热平衡,每生产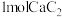 ,投料的量为
,投料的量为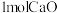 、
、_______ 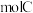 及
及_______ 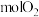 。
。
②制乙炔后的固体废渣主要成分为 ,可用于制取漂白粉,制取漂白粉的化学方程式为
,可用于制取漂白粉,制取漂白粉的化学方程式为_______ 。
(3)乙炔是二种重要的有机化工原料,乙炔在不同的反应条件下可以转化成下列化合物:
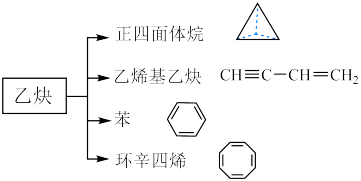
下列说法正确的是_______(填标号)。
(4)以乙炔为原料可制备维尼纶(PVAC),其合成路线如下:
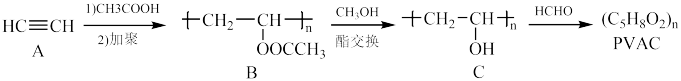
① 中官能团名称为
中官能团名称为_______ 。
② 经过两步反应,第二步为加聚反应,第一步反应类型为
经过两步反应,第二步为加聚反应,第一步反应类型为_______ 。
③ 的反应过程中另一种生成物的结构简式为
的反应过程中另一种生成物的结构简式为_______ 。
 )是重要的基本化工原料,主要用于生产乙炔。回答下列问题:
)是重要的基本化工原料,主要用于生产乙炔。回答下列问题:(1)碳元素在元素周期表中的位置为
 的电子式为
的电子式为(2)①目前工业上合成电石主要采用氧热法。
已知:
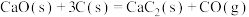
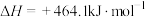 ;
;
 。
。若不考虑热量耗散,物料转化率均为
 ,最终炉中出来的气体只有
,最终炉中出来的气体只有 。则为了维持热平衡,每生产
。则为了维持热平衡,每生产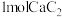 ,投料的量为
,投料的量为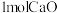 、
、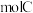 及
及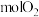 。
。②制乙炔后的固体废渣主要成分为
 ,可用于制取漂白粉,制取漂白粉的化学方程式为
,可用于制取漂白粉,制取漂白粉的化学方程式为(3)乙炔是二种重要的有机化工原料,乙炔在不同的反应条件下可以转化成下列化合物:

下列说法正确的是_______(填标号)。
| A.乙烯基乙炔分子中所有原子可以处于同一直线上 |
B.常温下, 苯中含碳碳双键数目约为 苯中含碳碳双键数目约为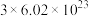 |
| C.环辛四烯与苯均能使酸性高锰酸钾溶液褪色 |
| D.正四面体烷与环辛四烯的一取代物均只有一种 |
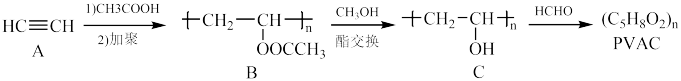
①
 中官能团名称为
中官能团名称为②
 经过两步反应,第二步为加聚反应,第一步反应类型为
经过两步反应,第二步为加聚反应,第一步反应类型为③
 的反应过程中另一种生成物的结构简式为
的反应过程中另一种生成物的结构简式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下图是氯的“价类二维图”,请根据所学回答下列问题:

(1)已知A、H均为一元酸,写出A、H的化学式:___________ 、___________ 。
(2)写出B物质的一种用途:___________ 。
(3)洁厕灵溶于水会有A物质生成,物质F为84消毒液的有效成分,当洗洁过程中两者混合使用,可能会发生中毒事件,试用离子方程式说明原因:___________ 。
(4)物质D是一种比氯气更优的消毒剂,它的消毒能力(每摩尔消毒剂得电子数的多少)是氯气的___________ 倍(已知两种消毒剂均被还原为 )。
)。

(1)已知A、H均为一元酸,写出A、H的化学式:
(2)写出B物质的一种用途:
(3)洁厕灵溶于水会有A物质生成,物质F为84消毒液的有效成分,当洗洁过程中两者混合使用,可能会发生中毒事件,试用离子方程式说明原因:
(4)物质D是一种比氯气更优的消毒剂,它的消毒能力(每摩尔消毒剂得电子数的多少)是氯气的
 )。
)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉都是生活中常用的含氯消毒剂。家庭中常常使用的消毒剂主要是“84”消毒液,可以说化学让生活更美好。图为“84”消毒液说明书。请回答下列问题。
(1)“84”消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该“84”消毒液商品的有效氯按53.25g/L计算,该消毒液的NaClO的物质的量浓度是_______ 。
(2)常温下用烧碱溶液吸收Cl2制备“84”消毒液。写出该反应的离子方程式_______ ,若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为_______ ,从氧化还原角度分析Cl2表现了______ 性。
(3)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是______ (用离子方程式表达)。(已知:酸性:H2CO3>HClO>HCO ),家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是
),家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是_______ 。
(4)游泳池水的消毒多用漂粉精,但酸碱性对漂粉精的消毒效果影响明显。池水碱性过强,杀毒作用会_______ (填“增强”或“减弱”)。
(5)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、“84”消毒液,主要目的_____ 。
A.增强漂白能力和消毒作用
B.使它转化为较稳定物质,便于保存和运输
C.使它转化为较易溶于水的物质
D.提高氯的质量分数,有利于漂白、消毒
 说明书 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00g/L~60.00g/L | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
| 用法用量 | 稀释后浸泡或洗刷白色衣物,浴缸等1:200水溶液餐饮具,瓜果等1:100水溶液 |
(1)“84”消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该“84”消毒液商品的有效氯按53.25g/L计算,该消毒液的NaClO的物质的量浓度是
(2)常温下用烧碱溶液吸收Cl2制备“84”消毒液。写出该反应的离子方程式
 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为(3)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是
 ),家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是
),家庭消毒马桶时,不可在用洁厕灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应的离子方程式是(4)游泳池水的消毒多用漂粉精,但酸碱性对漂粉精的消毒效果影响明显。池水碱性过强,杀毒作用会
(5)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、“84”消毒液,主要目的
A.增强漂白能力和消毒作用
B.使它转化为较稳定物质,便于保存和运输
C.使它转化为较易溶于水的物质
D.提高氯的质量分数,有利于漂白、消毒
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。其中含氯消毒剂在生产生活中有着广泛的用途。
(1)工业上将氯气溶于一定浓度的氢氧化钠溶液可制得“84消毒液”,用电子式表示“84消毒液”的有效成分是__________ 。
(2)二氧化氯(ClO2)是一种黄绿色易溶于水的气体,也可用于自来水的杀菌消毒。工业上常用NaClO3和Na2SO3溶液混合并加入稀H2SO4酸化后反应制得,反应中NaClO3和Na2SO3的物质的量之比为______________ 。
(1)工业上将氯气溶于一定浓度的氢氧化钠溶液可制得“84消毒液”,用电子式表示“84消毒液”的有效成分是
(2)二氧化氯(ClO2)是一种黄绿色易溶于水的气体,也可用于自来水的杀菌消毒。工业上常用NaClO3和Na2SO3溶液混合并加入稀H2SO4酸化后反应制得,反应中NaClO3和Na2SO3的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氯气是一种重要的化工原料,在生产生活中具有广泛的应用。
(1)实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
①写出实验室制取氯气的化学方程式_______ 。若产生标准状况下4.48 LCl2,则反应过程中被氧化的HCl的物质的量是_______ mol。
②为了防止氯气污染环境,需将剩余氯气通入_______ ,发生的化学反应方程式_______ 。
③实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下: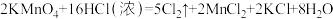 。在此反应中浓盐酸中显示出来的性质是
。在此反应中浓盐酸中显示出来的性质是_______ (填写字母)
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)电解饱和食盐水生产氢气、氯气、氢氧化钠,氯气与石灰乳反应可制取漂白粉。干燥的漂白粉不能发挥漂白效果,请写出漂白粉能发挥漂白效果的化学反应方程式_______ 。
(1)实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
①写出实验室制取氯气的化学方程式
②为了防止氯气污染环境,需将剩余氯气通入
③实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
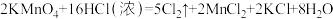 。在此反应中浓盐酸中显示出来的性质是
。在此反应中浓盐酸中显示出来的性质是A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)电解饱和食盐水生产氢气、氯气、氢氧化钠,氯气与石灰乳反应可制取漂白粉。干燥的漂白粉不能发挥漂白效果,请写出漂白粉能发挥漂白效果的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某工厂在山坡坑道的仓库里贮有氯气钢瓶。某天,有一只贮有氯气的钢瓶损坏,造成氯气泄漏,在场工人采取以下措施,请选择。
(1)①处理该钢瓶的方法正确的是_______ 。
A.钢瓶推到坡下的小河里 B.把钢瓶丢到深坑里,用石灰填埋 C.把钢瓶扔到农田中
②若在场工人没有防毒面具,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是_______ 。
A.NaOH B.NaCl C.Na2CO3
(2)为了探究HClO的漂白性,某同学设计了如图的实验:

①将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_______ ;氯水可作为漂白剂,起主要作用的是氯水中含有的_______ (用化学式表示)。
②为防止氯气尾气污染空气,可用NaOH溶液吸收多余的氯气,原理是_______ (化学方程式);根据这一原理,工业上常用廉价的石灰乳吸收制得漂白粉,漂白粉的有效成分是_______ (填化学式)。
(1)①处理该钢瓶的方法正确的是
A.钢瓶推到坡下的小河里 B.把钢瓶丢到深坑里,用石灰填埋 C.把钢瓶扔到农田中
②若在场工人没有防毒面具,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是
A.NaOH B.NaCl C.Na2CO3
(2)为了探究HClO的漂白性,某同学设计了如图的实验:

①将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
②为防止氯气尾气污染空气,可用NaOH溶液吸收多余的氯气,原理是
您最近一年使用:0次



