2019年1月3日上午,嫦娥四号探测器翩然落月,首次实现人类飞行器在月球背面的软着陆。所搭载的“玉兔二号”月球车,通过砷化镓(GaAs)太阳能电池提供能量进行工作。回答下列问题:
(1)基态Ga原子价电子排布式__________________ ,核外电子占据最高能级的电子云形状为_________ ;基态As原子最高能层上有_______ 个电子。
(2)镓失去电子的逐级电离能(单位:kJ•mol−1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为____ 和+3,砷的第一电离能比镓_____ (填“大”或“小”)。
(3)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为__________ 。
(4)砷化镓可由(CH3)3Ga和AsH3在700℃制得,(CH3)3Ga中Ga原子的杂化方式为______ ,AsH3分子的空间构型为____________ 。
(5)相同压强下,AsH3的沸点______ NH3(填“大于”或“小于”),原因为__________________
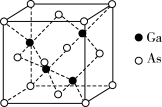
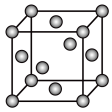
(6)GaAs为原子晶体,其晶胞结构如图所示,Ga与As以___________ (填“共价键”或“离子键”)键合。设阿伏加 德罗常数的值为NA,该晶胞边长为a pm,则GaAs晶体的密度为_____ g•cm−3(列出计算式即可)。

(1)基态Ga原子价电子排布式
(2)镓失去电子的逐级电离能(单位:kJ•mol−1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为
(3)第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为
(4)砷化镓可由(CH3)3Ga和AsH3在700℃制得,(CH3)3Ga中Ga原子的杂化方式为
(5)相同压强下,AsH3的沸点
(6)GaAs为原子晶体,其晶胞结构如图所示,Ga与As以
更新时间:2020-03-17 12:44:20
|
相似题推荐
【推荐1】结合物质结构与性质相关知识,回答下列问题。
(1)基态Se原子的核外电子排布式为________________ 。
(2) 分子的空间构型为
分子的空间构型为________________ ,属于________________ (填“极性”或“非极性”)分子。 分子易作为配体与
分子易作为配体与 形成
形成 ,在
,在 结构中若用两个
结构中若用两个 分子代替两个
分子代替两个 分子可以得到两种不同结构的化合物,由此推测
分子可以得到两种不同结构的化合物,由此推测 的空间构型为
的空间构型为________________ 。
(3)吡啶( )在水中的溶解度远大于苯,可能原因是①吡啶和
)在水中的溶解度远大于苯,可能原因是①吡啶和 均为极性分子相似相溶而苯为非极性分子;②
均为极性分子相似相溶而苯为非极性分子;②___ 。
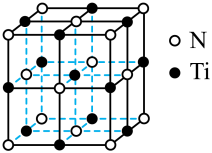
(4)氮化钛晶体的晶胞结构如图所示,该晶体结构中所含N、Ti原子个数比为________________ ;N原子周围与其原子距离相等且最近的N原子个数是________________ 个。
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图所示,S原子的配位数是____________ ,已知晶胞边长为540.0pm, 代表阿伏加德罗常数,则其密度为
代表阿伏加德罗常数,则其密度为_______________ (列式并计算)。(S:32;Zn:65)

(1)基态Se原子的核外电子排布式为
(2)
 分子的空间构型为
分子的空间构型为 分子易作为配体与
分子易作为配体与 形成
形成 ,在
,在 结构中若用两个
结构中若用两个 分子代替两个
分子代替两个 分子可以得到两种不同结构的化合物,由此推测
分子可以得到两种不同结构的化合物,由此推测 的空间构型为
的空间构型为(3)吡啶(
 )在水中的溶解度远大于苯,可能原因是①吡啶和
)在水中的溶解度远大于苯,可能原因是①吡啶和 均为极性分子相似相溶而苯为非极性分子;②
均为极性分子相似相溶而苯为非极性分子;②(4)氮化钛晶体的晶胞结构如图所示,该晶体结构中所含N、Ti原子个数比为

(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图所示,S原子的配位数是
 代表阿伏加德罗常数,则其密度为
代表阿伏加德罗常数,则其密度为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】碳和硅均为元素周期表中第ⅣA族的元素,其单质和化合物有着重要应用。
(1)石墨烯是只有一个碳原子直径厚度的单层石墨,最早是由科学家用机械剥离的方法从石墨中分离出来,其部分性能优于传统的硅材料,具有广泛的应用前景。
①写出基态碳原子的电子排布式_______ ,石墨烯中C的杂化类型为_______ 。
②下图为单层石墨烯的结构示意图。12 g的石墨烯中由C原子连接成的六元环的物质的量约为_______ mol。

③石墨烯可由加热SiC晶体脱除Si的方法制得。该过程属于_______ 。
a.物理变化 b.分解反应 c.氧化还原反应
(2)SiC的晶体结构与晶体硅类似。SiC的晶体类型为_______ ,晶体中Si原子与Si-C键的数目之比为_______ 。
(3)CHCl3与SiHCl3空间构型相似,但性质不同:前者不易与水反应,但后者与水剧烈反应,生成两种酸和一种气体,写出该反应的化学方程式:______ 。
(1)石墨烯是只有一个碳原子直径厚度的单层石墨,最早是由科学家用机械剥离的方法从石墨中分离出来,其部分性能优于传统的硅材料,具有广泛的应用前景。
①写出基态碳原子的电子排布式
②下图为单层石墨烯的结构示意图。12 g的石墨烯中由C原子连接成的六元环的物质的量约为

③石墨烯可由加热SiC晶体脱除Si的方法制得。该过程属于
a.物理变化 b.分解反应 c.氧化还原反应
(2)SiC的晶体结构与晶体硅类似。SiC的晶体类型为
(3)CHCl3与SiHCl3空间构型相似,但性质不同:前者不易与水反应,但后者与水剧烈反应,生成两种酸和一种气体,写出该反应的化学方程式:
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】Fe、Cu都是重要的材料元素,其单质及化合物在诸多领域中都有广泛的应用。
(1)Fe位于元素周期表的_____ 区,Fe2+的价层电子排布图为_____ 。
(2)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成红色。该反应在有的教材中用方程式FeCl3+3KSCN=Fe(SCN)3+3KCl表示。经研究表明,Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1∶3的个数比配合,还可以其他个数比配合。请按要求填空:
①所得Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1∶1配合所得离子显红色。含该离子的配合物的化学式是____ 。
②铁的另一种配合物铁氰化钾K3[Fe(CN)6]俗称赤血盐,可用于检验Fe2+,两者反应生成带有特征蓝色的沉淀,请用离子方程式说明原理_____ ,该赤血盐其配体的电子式为:_____ 。
(3)Cu的某种化合物的结构如图所示,该化合物中既含有配位键,又含有氢键,其中配位键和氢键均采用虚线表示。
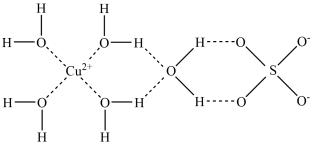
0.5mol该化合物中含有σ键的个数为_____ 。Cu2+与NH3还可形成[Cu(NH3)4]2+配离子,该配离子的立体构型为____ 。
(1)Fe位于元素周期表的
(2)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成红色。该反应在有的教材中用方程式FeCl3+3KSCN=Fe(SCN)3+3KCl表示。经研究表明,Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1∶3的个数比配合,还可以其他个数比配合。请按要求填空:
①所得Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1∶1配合所得离子显红色。含该离子的配合物的化学式是
②铁的另一种配合物铁氰化钾K3[Fe(CN)6]俗称赤血盐,可用于检验Fe2+,两者反应生成带有特征蓝色的沉淀,请用离子方程式说明原理
(3)Cu的某种化合物的结构如图所示,该化合物中既含有配位键,又含有氢键,其中配位键和氢键均采用虚线表示。

0.5mol该化合物中含有σ键的个数为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】图表法、图象法是常用的科学研究方法。
(1)短周期某主族元素M的电离能情况如图1所示。则M元素位于周期表的第________ 族。
(2)图2是研究部分主族元素氢化物的沸点变化规律的图象,折线c可以表达出第________ 族元素气态氢化物的沸点变化规律。两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线(a和b),你认为正确的是折线___________ (填a或b)。
(3)部分短周期主族元素的最高价氧化物对应的水化物(浓度均为0.01mol.L-1)溶液的pH和原子序数的关系如下图所示。元素R在周期表中的位置是______________ ;元素Y的原子结构示意图是____________ 。
(1)短周期某主族元素M的电离能情况如图1所示。则M元素位于周期表的第

(2)图2是研究部分主族元素氢化物的沸点变化规律的图象,折线c可以表达出第
(3)部分短周期主族元素的最高价氧化物对应的水化物(浓度均为0.01mol.L-1)溶液的pH和原子序数的关系如下图所示。元素R在周期表中的位置是

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】新型储氢材料是开发利用氢能的重要研究方向。
(1)元素N的价电子数排布式为3d24s2,其氯化物NCl4和LiBH4反应可制得储氢材料N(BH4)3。
①元素N在周期表中的位置为__ ,该原子具有__ 种运动状态不同的电子。
②化合物LiBH4中含有的化学键有__ ,BH4-的立体构型是_ ,B原子的杂化轨道类型是__ ,B原子轨道表达式为__ 。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+__ H-(填“>”“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:M的最高正价是__ 。
(3)NaH具有NaCl型晶体结构,Na+的配位数为__ ,晶体的堆积方式为__ ,已知NaH晶体的晶胞参数a=488pm,Na+半径为102pm,H-的半径为pm,NaH的理论密度是__ g·cm-3。(仅写表达式,不计算)
(1)元素N的价电子数排布式为3d24s2,其氯化物NCl4和LiBH4反应可制得储氢材料N(BH4)3。
①元素N在周期表中的位置为
②化合物LiBH4中含有的化学键有
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:M的最高正价是
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
(3)NaH具有NaCl型晶体结构,Na+的配位数为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】氮及其化合物广泛存在于自然界中,回答下列问题:
(1)在基态16N中,其s能电子云形状是_____ 形的,其p能级轨道上存在______ 个自旋方向相同的电子;CN-中共价键的类型有______ 。
(2)碱性肥料氰氮化钙(CaCN2)的组成元素第一电离能最小的是_______ (填名称)。
(3)化合物(CH3)3N能溶于水,其原因是_______________ ,(CH3)3N与盐酸反应生成[(CH3)3NH]+,该过程新生成的化学键类型为__________________ .。
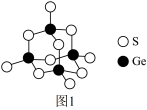
(4)阳离子[(CH3)3NH]+和阴离子A可按个数比4:1组成化合物,阴离子A的结构如图1所示,则S原子的杂化轨道类型是______ ,阴离子A的化学式为______ 。

(5)立方氮化硼的晶胞如图2所示(白球为氮原子,黑球为硼原子),则硼原子的配位数为______ ;若晶胞边长为acm,则立方氮化硼的密度是______ g·cm-3(只要求列算式,阿伏伽德罗常数用NA表示)。
(1)在基态16N中,其s能电子云形状是
(2)碱性肥料氰氮化钙(CaCN2)的组成元素第一电离能最小的是
(3)化合物(CH3)3N能溶于水,其原因是
(4)阳离子[(CH3)3NH]+和阴离子A可按个数比4:1组成化合物,阴离子A的结构如图1所示,则S原子的杂化轨道类型是


(5)立方氮化硼的晶胞如图2所示(白球为氮原子,黑球为硼原子),则硼原子的配位数为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】黑火药是我国古代的四大发明之一。黑火药爆炸时发生的反应为:2KNO3+S+3C=K2S+N2↑+3CO2↑。回答下列问题:
(1)基态钾原子的核外电子排布式为____________ ,第一电离能:K______ (填“>”或“<”)Na。
(2)NO3-的空间构型为_____________ 。
(3)固态硫易溶于CS2,熔点为112℃,沸点为444.8℃。其分子结构为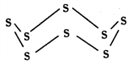 ,S8中硫原子的杂化轨道类型是
,S8中硫原子的杂化轨道类型是____________ ,S8分子中至多有________ 个硫原子处于同一平面。
(4)N2分子中σ键与π键的个数比为________ ,N2的沸点比CO的沸点____ (填“高”或“低”)。
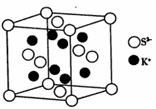
(5)K2S的晶胞结构如图所示。其中K+的配位数为_______ ,S2-的配位数为____ ;若晶胞中距离最近的两个S2-核间距为a cm,则K2S晶体的密度为____ g·cm-3(列出计算式,不必计算出结果)。
(1)基态钾原子的核外电子排布式为
(2)NO3-的空间构型为
(3)固态硫易溶于CS2,熔点为112℃,沸点为444.8℃。其分子结构为
 ,S8中硫原子的杂化轨道类型是
,S8中硫原子的杂化轨道类型是(4)N2分子中σ键与π键的个数比为
(5)K2S的晶胞结构如图所示。其中K+的配位数为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,也是重要的非金属元素。
回答下列问题:
(1)基态磷原子的价电子排布式为________________ 。
(2)N和P同主族且相邻,PF3和NH3都能与许多过渡金属形成配合物,但NF3却不能与过渡金属形成配合物,其原因是____________________________________________ 。
(3)磷酸为三元酸,其结构式为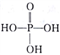 。PO43-的空间构型为
。PO43-的空间构型为____________ ;写出一种与PO43-互为等电子体且属于非极性分子的化学式:____________________ 。
(4)将磷酸加热可发生分子间脱水生成焦磷酸(H4P2O7)、三磷酸以及高聚磷酸,焦磷酸的酸性强于磷酸的原因是______________________________________________________ 。
(5)磷化硼(BP)是受到高度关注的耐磨涂料。BP中B和P原子均形成共价键,其中存在配位键,配位键中提供孤电子对的是____________ (填元素符号)原子;磷化硼的晶体类型是____________ ,其中B原子的杂化方式是____________ 杂化,1mol BP 中含有____________ molB-P键。
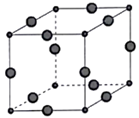
(6)Cu3P的晶胞结构如图所示,P3-的配位数为____________ ,Cu+的半径为a pm,P3- 的半径为bpm,阿伏伽德罗常数的值为NA,则CuP晶体的密度为____________ g·cm-3(用含a、b、NA的代数式表示)。
回答下列问题:
(1)基态磷原子的价电子排布式为
(2)N和P同主族且相邻,PF3和NH3都能与许多过渡金属形成配合物,但NF3却不能与过渡金属形成配合物,其原因是
(3)磷酸为三元酸,其结构式为
 。PO43-的空间构型为
。PO43-的空间构型为(4)将磷酸加热可发生分子间脱水生成焦磷酸(H4P2O7)、三磷酸以及高聚磷酸,焦磷酸的酸性强于磷酸的原因是
(5)磷化硼(BP)是受到高度关注的耐磨涂料。BP中B和P原子均形成共价键,其中存在配位键,配位键中提供孤电子对的是
(6)Cu3P的晶胞结构如图所示,P3-的配位数为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
真题
名校
【推荐3】(1)元素的第一电离能:Al___ Si(填“>”或“<”)。
(2)基态Mn2+的核外电子排布式为___ 。
(3)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是___ 。

(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示

①在Xm-中,硼原子轨道的杂化类型有___ ;配位键存在于___ 原子之间(填原子的数字标号);m=___ (填数字)。
②硼砂晶体由Na+、Xm-和H2O构成,它们之间的作用力有___ (填序号)。
A.离子键 B.共价键 C.金属键 D.范德华力 E.氢键
(2)基态Mn2+的核外电子排布式为
(3)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是

(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示

①在Xm-中,硼原子轨道的杂化类型有
②硼砂晶体由Na+、Xm-和H2O构成,它们之间的作用力有
A.离子键 B.共价键 C.金属键 D.范德华力 E.氢键
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】 和
和 均属于稀有金属,在生产、科技和军事领域均有重要的研究和应用价值。回答下列问题:
均属于稀有金属,在生产、科技和军事领域均有重要的研究和应用价值。回答下列问题:
(1)基态 原子的价电子排布式为
原子的价电子排布式为_______ ;基态 原子占据最高能层的核外电子的电子云轮廓图的形状为
原子占据最高能层的核外电子的电子云轮廓图的形状为_______ 。
(2) 和
和 处于同一周期,且核外最高能层电子构型相同。金属
处于同一周期,且核外最高能层电子构型相同。金属 的熔点
的熔点_______ (填“高于”或“低于”)金属 ,原因为
,原因为_______ 。
(3) 能形成多种重要配合物,如
能形成多种重要配合物,如 能形成
能形成 能形成
能形成 、
、 等。
等。
 ①中所含阴离子的每个原子最外层均满足
①中所含阴离子的每个原子最外层均满足 结构。该阴离子的立体构型为
结构。该阴离子的立体构型为_______ ,其中心原子的杂化形式为_______ 。
② 中含有
中含有 键的数目为
键的数目为_______ 。
(4) 能形成多种化合物,如
能形成多种化合物,如 、
、 。基态
。基态 原子的第一电离能
原子的第一电离能_______  填“大于”或“小于”
填“大于”或“小于” 基态
基态 原子。
原子。
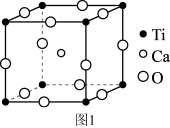
(5)钛酸钙晶胞结构如图1所示。钛酸钙的化学式为_______ ; 个钛离子与
个钛离子与_______ 个氧离子等距离且最近,连接这些氧离子构成正八面体,钛离子位于该正八面体的体心。
(6)铁和氮可组成一种过渡金属氮化物,其晶胞结构如图2所示。六棱柱底边边长为 ,高为
,高为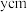 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则它的密度为
,则它的密度为_______  (列算式即可) 。
(列算式即可) 。
 和
和 均属于稀有金属,在生产、科技和军事领域均有重要的研究和应用价值。回答下列问题:
均属于稀有金属,在生产、科技和军事领域均有重要的研究和应用价值。回答下列问题:(1)基态
 原子的价电子排布式为
原子的价电子排布式为 原子占据最高能层的核外电子的电子云轮廓图的形状为
原子占据最高能层的核外电子的电子云轮廓图的形状为(2)
 和
和 处于同一周期,且核外最高能层电子构型相同。金属
处于同一周期,且核外最高能层电子构型相同。金属 的熔点
的熔点 ,原因为
,原因为(3)
 能形成多种重要配合物,如
能形成多种重要配合物,如 能形成
能形成 能形成
能形成 、
、 等。
等。 ①中所含阴离子的每个原子最外层均满足
①中所含阴离子的每个原子最外层均满足 结构。该阴离子的立体构型为
结构。该阴离子的立体构型为②
 中含有
中含有 键的数目为
键的数目为(4)
 能形成多种化合物,如
能形成多种化合物,如 、
、 。基态
。基态 原子的第一电离能
原子的第一电离能 填“大于”或“小于”
填“大于”或“小于” 基态
基态 原子。
原子。(5)钛酸钙晶胞结构如图1所示。钛酸钙的化学式为
 个钛离子与
个钛离子与
(6)铁和氮可组成一种过渡金属氮化物,其晶胞结构如图2所示。六棱柱底边边长为
 ,高为
,高为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则它的密度为
,则它的密度为 (列算式即可) 。
(列算式即可) 。
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】钇是稀土元素之一。我国蕴藏着丰富的钇矿石(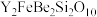 ),用NaOH初步处理钇矿石可以得到
),用NaOH初步处理钇矿石可以得到 、
、 、
、 和
和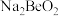 的共熔物。工业上利用该共熔物制取
的共熔物。工业上利用该共熔物制取 ,并获得副产物BeO,流程如图:
,并获得副产物BeO,流程如图:
ⅱ.在室温的条件下, ;
;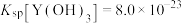 ;水的离子积
;水的离子积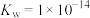 。
。
(1)基态铍原子的核外电子排布式为___________ 。
(2)滤渣1的主要成分是___________ 。沉铍时,过量的试剂最好选用___________ (填序号)。
A.NaOH溶液 B.氨水 C. D.CaO
D.CaO
(3)制取 时,第一次加氨水调pH的目的是
时,第一次加氨水调pH的目的是___________ 。
(4)计算常温下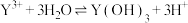 的平衡常数
的平衡常数
___________ 。
(5)过滤2所得的滤液经过一系列处理可得到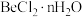 ,将
,将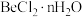 与足量的
与足量的 共热可以制备无水
共热可以制备无水 ,写出该过程的化学反应方程式:
,写出该过程的化学反应方程式:___________ 。
(6)BeO的立方晶胞如图所示:___________ 。
②若BeO晶体的密度为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则晶胞中
,则晶胞中 与最近
与最近 之间的距离为
之间的距离为___________ nm。
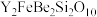 ),用NaOH初步处理钇矿石可以得到
),用NaOH初步处理钇矿石可以得到 、
、 、
、 和
和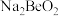 的共熔物。工业上利用该共熔物制取
的共熔物。工业上利用该共熔物制取 ,并获得副产物BeO,流程如图:
,并获得副产物BeO,流程如图: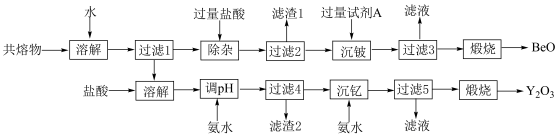
ⅱ.在室温的条件下,
 ;
;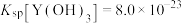 ;水的离子积
;水的离子积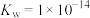 。
。(1)基态铍原子的核外电子排布式为
(2)滤渣1的主要成分是
A.NaOH溶液 B.氨水 C.
 D.CaO
D.CaO(3)制取
 时,第一次加氨水调pH的目的是
时,第一次加氨水调pH的目的是(4)计算常温下
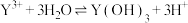 的平衡常数
的平衡常数
(5)过滤2所得的滤液经过一系列处理可得到
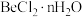 ,将
,将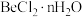 与足量的
与足量的 共热可以制备无水
共热可以制备无水 ,写出该过程的化学反应方程式:
,写出该过程的化学反应方程式:(6)BeO的立方晶胞如图所示:
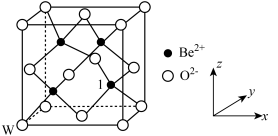
②若BeO晶体的密度为
 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则晶胞中
,则晶胞中 与最近
与最近 之间的距离为
之间的距离为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E是元素周期表中五种常见元素,其原子序数依次增大。详细信息见表:
请回答下列问题:
(1)D的价电子排布式可表示为__ 。
(2)BC3-的空间构型为__ (用文字描述)。
(3)根据等电子原理,AC分子的结构式为__ 。
(4)1molAC2中σ键、π键数目之比为__ 。
(5)A、B、C的第一电离能由大到小顺序为__ 。
(6)E为__ 堆积金属,已知E原子的半径为acm,阿伏加 德罗常数的值为NA,则E晶体的密度是__ g·cm-3。(列出算式即可)。
(7)E晶胞结构如图所示,E晶体中每个E原子周围距离最近的E原子数目为__ ;E2S为半导体材料,在其立方晶胞内部有4个S原子,其余S原子位于面心和顶点,则该晶胞中有__ 个E原子。
(8)将E单质的粉末加入NH3的浓溶液中,通入O2,充分反应后溶液呈深蓝色,写出该反应的离子方程式__ 。
| ① | A的一种核素在考古时常用来鉴定一些文物的年代 |
| ② | B的氧化物是导致光化学烟雾的主要物质之一 |
| ③ | C的某一种单质是空气的主要成分之一 |
| ④ | D的基态原子核外有6个原子轨道处于半充满状态 |
| ⑤ | E能形成红色的E2O和黑色的EO两种氧化物 |
(1)D的价电子排布式可表示为
(2)BC3-的空间构型为
(3)根据等电子原理,AC分子的结构式为
(4)1molAC2中σ键、π键数目之比为
(5)A、B、C的第一电离能由大到小顺序为
(6)E为
(7)E晶胞结构如图所示,E晶体中每个E原子周围距离最近的E原子数目为

(8)将E单质的粉末加入NH3的浓溶液中,通入O2,充分反应后溶液呈深蓝色,写出该反应的离子方程式
您最近半年使用:0次



