元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)与氯元素同族的短周期元素的原子核外电子排布式为___ 。
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是___ (填序号)。
a.Cl2、Br2、I2的熔点 b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d.HCl、HBr、HI的酸性
(3)工业上,通过如图转化可制得KClO3晶体:
NaCl溶液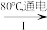 NaClO3溶液
NaClO3溶液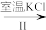 KClO3晶体
KClO3晶体
II中转化的基本反应类型是___ ,该反应过程能析出KClO3晶体而无其它晶体析出的原因是___ 。
(4)晶体硅(熔点1410℃)是良好的半导体材料;四氯化硅熔点-70℃,沸点57.6℃;由粗硅制纯硅过程如图:
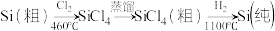
写出SiCl4的电子式:___ ;在上述由SiCl4制纯硅的反应中,测得生成7kg纯硅需吸收akJ热量,写出该反应的热化学方程式:___ 。
(5)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并用单线桥标出电子转移的方向和数目___ 。
(1)与氯元素同族的短周期元素的原子核外电子排布式为
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是
a.Cl2、Br2、I2的熔点 b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d.HCl、HBr、HI的酸性
(3)工业上,通过如图转化可制得KClO3晶体:
NaCl溶液
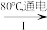 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体II中转化的基本反应类型是
(4)晶体硅(熔点1410℃)是良好的半导体材料;四氯化硅熔点-70℃,沸点57.6℃;由粗硅制纯硅过程如图:
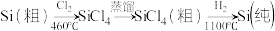
写出SiCl4的电子式:
(5)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并用单线桥标出电子转移的方向和数目
更新时间:2020-03-22 18:27:36
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】写出镁带在点燃条件下与氮气反应生成氮化镁的化学方程式_____ 。分析该反应中化合价发生变化的元素,指出氧化剂和还原剂,并标出电子转移的方向和数目_____ 。
您最近一年使用:0次
【推荐2】有以下转化关系:

(1)上述转化中属于氧化还原反应的是_______ 。
(2)用单线桥标出下列反应电子转移的方向和数目_______ 。
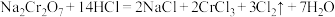
氧化剂为_______ ,氧化产物为_______ ,生成一个 转移
转移_______ 个电子

(1)上述转化中属于氧化还原反应的是
(2)用单线桥标出下列反应电子转移的方向和数目
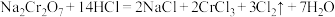
氧化剂为
 转移
转移
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】钠和钠的化合物有许多重要的用途,碳酸钠可用于从海水提取溴,涉及的反应如下:3Br2+6Na2CO3+3H2O=5NaBr+NaBrO3+6NaHCO3
(1)用双线桥法标出电子转移的方向和数目_______ 。
(2)该反应的离子方程式为_______ 。
(3)该反应中氧化剂与还原剂的物质的量之比是_______ ,若80gBr2被氧化时,转移的电子数目是_______ 。
(4)少量的钠应保存在_______ 中;钠着火时应采取的灭火措施是_______ ,不能用水灭火,原因是_______ (涉及反应的离子方程式)。
(1)用双线桥法标出电子转移的方向和数目
(2)该反应的离子方程式为
(3)该反应中氧化剂与还原剂的物质的量之比是
(4)少量的钠应保存在
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量 N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256kJ的热量。
N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256kJ的热量。
(1)写出该反应的热化学方程式________________ 。
(2)已知H2O(l)═H2O(g);△H=+44kJ·mol−1,则16g液态肼燃烧生成氮气和液态水时,放出的热量是________ kJ。
(3)丙烷燃烧可以通过以下两种途径:
途径I:C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=−a kJ·mol−1
途径II:C3H8(g)═C3H6(g)+H2(g)△H=+b kJ·mol−1
2C3H6(g)+9O2(g)═6CO2(g)+6H2O(l)△H=−c kJ·mol−1
2H2(g)+O2(g)═2H2O(l)△H=−d kJ·mol−1(abcd均为正值)
①判断等量的丙烷通过两种途径放出的热量,途径I放出的热量_______ (填“大于”、“等于”或“小于”)途径II放出的热量。
②在C3H8(g)═C3H6(g)+H2(g) 的反应中,反应物具有的总能量________ (填“大于”、“等于”或“小于”)生成物具有的总能量。
③b 与a、c、d的数学关系式是_____________ 。
 N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256kJ的热量。
N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256kJ的热量。(1)写出该反应的热化学方程式
(2)已知H2O(l)═H2O(g);△H=+44kJ·mol−1,则16g液态肼燃烧生成氮气和液态水时,放出的热量是
(3)丙烷燃烧可以通过以下两种途径:
途径I:C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=−a kJ·mol−1
途径II:C3H8(g)═C3H6(g)+H2(g)△H=+b kJ·mol−1
2C3H6(g)+9O2(g)═6CO2(g)+6H2O(l)△H=−c kJ·mol−1
2H2(g)+O2(g)═2H2O(l)△H=−d kJ·mol−1(abcd均为正值)
①判断等量的丙烷通过两种途径放出的热量,途径I放出的热量
②在C3H8(g)═C3H6(g)+H2(g) 的反应中,反应物具有的总能量
③b 与a、c、d的数学关系式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学反应过程中发生物质变化的同时,常常伴有能量的变化.这种能量的变化常以热量的形式表现出来,叫做反应热.由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等。
(1)下列△H表示物质燃烧热的是_______ ;表示物质中和热的是_______ (填“△H1”、“△H2”、“△H3”等).
A.2H2(g)+O2(g)═2H2O(l)△H1
B.C(s)+1/2O2(g)═CO(g)△H2
C.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H3
D.C(s)+O2(g)═CO2(g)△H4
E.C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(l)△H5
F. NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H6
G.2NaOH(aq)+H2SO4(aq)═Na2SO4(aq)+2H2O(l)△H7
H.CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H8
(2)依据事实,写出下列反应的热化学方程式.
Ⅰ、在25℃、101kPa下,1gCH3OH燃烧生成CO2和液态水时放热22.68kJ.则表示甲醇燃烧热的热化学方程式为_______________________ ;
Ⅱ、1.00L 1.00mol/L H2SO4溶液与2.00L 1.00mol/L NaOH溶液完全反应,放出114.6kJ的热量,表示其中和热的热化学方程式为________________________ ;
Ⅲ、已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、 946kJ,则N2与H2反应生成NH3的热化学方程式为_______________________ 。
(1)下列△H表示物质燃烧热的是
A.2H2(g)+O2(g)═2H2O(l)△H1
B.C(s)+1/2O2(g)═CO(g)△H2
C.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H3
D.C(s)+O2(g)═CO2(g)△H4
E.C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(l)△H5
F. NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H6
G.2NaOH(aq)+H2SO4(aq)═Na2SO4(aq)+2H2O(l)△H7
H.CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H8
(2)依据事实,写出下列反应的热化学方程式.
Ⅰ、在25℃、101kPa下,1gCH3OH燃烧生成CO2和液态水时放热22.68kJ.则表示甲醇燃烧热的热化学方程式为
Ⅱ、1.00L 1.00mol/L H2SO4溶液与2.00L 1.00mol/L NaOH溶液完全反应,放出114.6kJ的热量,表示其中和热的热化学方程式为
Ⅲ、已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、 946kJ,则N2与H2反应生成NH3的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氯碱工业中电解饱和食盐水的原理示意图如右图所示。

(1)电极b是电源的_________ ;
(2)溶液A的溶质是(填化学式)_________ ;
(3)电解饱和食盐水的化学方程式是_______________________ 。
(4)电解时用盐酸控制阳极区溶液的pH在2~3。用化学平衡移动原理解释盐酸的作用:________________________________________________________________________________ 。
(5)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1mol Cl2参与反应时释
放出145kJ热量,写出该反应的热化学方程:________________________ 。

(1)电极b是电源的
(2)溶液A的溶质是(填化学式)
(3)电解饱和食盐水的化学方程式是
(4)电解时用盐酸控制阳极区溶液的pH在2~3。用化学平衡移动原理解释盐酸的作用:
(5)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1mol Cl2参与反应时释
放出145kJ热量,写出该反应的热化学方程:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】为纪念元素周期表诞生 150 周年,IUPAC 等从世界范围征集优秀青年化学家为化学元素代言,我国有8 位化学家成为硫(S)等元素的代言人。回答下列问题:
(1)S 在周期表中的位置是___________
(2)下列有关性质的比较,能用元素周期律解释的是___________ (填字母序号)
a.非金属性:O>S b.离子半径:S2->Cl- c.酸性:H2SO4>H2SO3 d.酸性:H2SO4>H3PO4
(3)Se 与 S 位于同一主族,二者氢化物稳定性较强的是:___________ (用化学式表示),用原子结构解释原因___________
(4)某同学用如下装置探究不同价态硫元素之间的转化。培养皿中 A、B、C 三个塑料瓶盖内盛有不同物质。向 Na2SO3 固体上滴加 70%硫酸,迅速用玻璃片将培养皿盖严,实验记录如下。
能够说明硫元素由+4 价转化为+6 价的证据是___________
(1)S 在周期表中的位置是
(2)下列有关性质的比较,能用元素周期律解释的是
a.非金属性:O>S b.离子半径:S2->Cl- c.酸性:H2SO4>H2SO3 d.酸性:H2SO4>H3PO4
(3)Se 与 S 位于同一主族,二者氢化物稳定性较强的是:
(4)某同学用如下装置探究不同价态硫元素之间的转化。培养皿中 A、B、C 三个塑料瓶盖内盛有不同物质。向 Na2SO3 固体上滴加 70%硫酸,迅速用玻璃片将培养皿盖严,实验记录如下。
| 实验装置 | 瓶盖 | 物质 | 实验现象 |
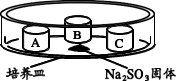 | A | 蘸有品红溶液的棉花 | 品红溶液褪色 |
| B | HCl、BaCl2 的混合溶液 | 无明显变化 | |
| C | HCl、BaCl2、FeCl3 的混合溶液 | 产生白色沉淀 |
能够说明硫元素由+4 价转化为+6 价的证据是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分。
试用合适的化学用语回答下列问题:
(1)请画出元素④简单阴离子的结构示意图:____________ 。
(2) ③⑤⑧的原子半径由小到大的顺序为__________ (填元素符号)。
(3)⑧和⑨的最高价氧化物对应水化物的酸性强弱为_____ > _____ (填化学式)。
(4) ③⑤两种元素的原子按1:1组成的常见化合物的电子式 为_______ 。
(5)写出⑦的单质与⑤的最高价氧化物对应水化物溶液反应的化学方程式_____________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
| 4 |
(1)请画出元素④简单阴离子的结构示意图:
(2) ③⑤⑧的原子半径由小到大的顺序为
(3)⑧和⑨的最高价氧化物对应水化物的酸性强弱为
(4) ③⑤两种元素的原子按1:1组成的常见化合物的电子式 为
(5)写出⑦的单质与⑤的最高价氧化物对应水化物溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知铷是37号元素。根据相关知识回答下列问题:
(1)请推测铷(Rb)在元素周期表的第___________ 周期第___________ 族。
(2)关于铷的结构和性质判断正确的是___________(填字母,下同)。
①与水反应比钠剧烈 ②它的原子半径比钠小
③它的氧化物暴露在空气中易吸收CO2 ④它的阳离子最外层电子数和镁相同
⑤它是还原剂
(3)氢化铷与水反应可放出氢气,则下列叙述正确的是___________。
(4)现有铷和另一种碱金属形成的合金50 g,当它与足量水反应时,放出标准状况下的氢气22.4 L,这种碱金属可能是________。
(1)请推测铷(Rb)在元素周期表的第
(2)关于铷的结构和性质判断正确的是___________(填字母,下同)。
①与水反应比钠剧烈 ②它的原子半径比钠小
③它的氧化物暴露在空气中易吸收CO2 ④它的阳离子最外层电子数和镁相同
⑤它是还原剂
| A.①③④ | B.①③⑤ | C.②③⑤ | D.②④ |
| A.氢化铷溶于水显酸性 |
| B.氢化铷与水反应时被还原为氢气 |
| C.氢化铷是离子化合物,其中氢离子最外层有2个电子 |
| D.氢化铷与水反应时,生成1mol H2将转移2mol e- |
| A.Li | B.Na | C.K | D.Cs |
您最近一年使用:0次
【推荐1】①、②、③、④是原子序数依次增大的四种短周期元素,①周期表中原子半径最小的元素,②的最外层电子数比次外层多1,③的第一电离能比左右相邻两元素的都要大,④是周期表中电负性最大的元素。元素①和③可形成一种三角锥形的分子A,元素②和④可形成一种平面三角形的分子B。
(1)元素②的基态原子的电子排布式为___________ 。
(2)元素③的价电子的轨道表示式为___________ 。
(3)已知元素①与②形成的化合物中元素①呈负价,将元素①、②、③、④按电负性由大到小排序:___________ (用元素符号表示)。
(4)分子A的电子式为___________ ,分子B的中心原子杂化方式为___________ ;A与B之间能否形成配位键?若能,用化学用语表示出两者之间的配位键;若不能,说明理由:___________ 。
(5)这四种元素可形成一种离子化合物,其阴、阳离子均为正四面体结构,阴、阳离子各含其中两种元素,写出一种符合要求的化学式:___________ 。
(1)元素②的基态原子的电子排布式为
(2)元素③的价电子的轨道表示式为
(3)已知元素①与②形成的化合物中元素①呈负价,将元素①、②、③、④按电负性由大到小排序:
(4)分子A的电子式为
(5)这四种元素可形成一种离子化合物,其阴、阳离子均为正四面体结构,阴、阳离子各含其中两种元素,写出一种符合要求的化学式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据所学知识回答问题:
(1)写出表示含有8个质子,10个中子的原子的结构示意图:___________ 。
(2)最外层电子数为次外层电子数 的原子
的原子___________ 或___________ ;(填元素符号)
(3)根据下列微粒回答问题: 、
、 、
、 、
、 、
、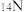 、
、 、
、 、
、 。
。
①以上8种微粒共有___________ 种核素,共___________ 种元素。
②互为同位素的是___________ 。
③中子数相等的是___________ 。
(4)相同物质的量的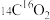 与
与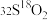 的质量之比为
的质量之比为___________ ;电子数之比为___________ 。
(1)写出表示含有8个质子,10个中子的原子的结构示意图:
(2)最外层电子数为次外层电子数
 的原子
的原子(3)根据下列微粒回答问题:
 、
、 、
、 、
、 、
、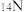 、
、 、
、 、
、 。
。①以上8种微粒共有
②互为同位素的是
③中子数相等的是
(4)相同物质的量的
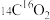 与
与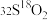 的质量之比为
的质量之比为
您最近一年使用:0次

 Cl
Cl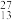 Al
Al S2-
S2-

