1 . 实验室中利用固体KMnO4进行如图实验,下列说法错误的是
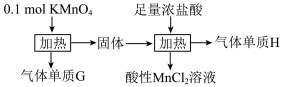

| A.G与H均为氧化产物 | B.Mn元素至少参与了3个氧化还原反应 |
| C.氧化性MnO2>Cl2 | D.G与H的物质的量之和为0.25mol |
您最近半年使用:0次
2 . 已知下列反应:①Cl2+2NaBr=2NaCl+Br2;②2KI+Br2=2KBr+I2;③Na2S+I2=2NaI+S↓。
(1)Cl-、Br-、I-、S2-四种离子的还原性由强到弱的顺序是_______ 。
(2)判断Cl2与Na2S能否反应?_______ (填“否”或书写反应的离子方程式)。
(3)判断I2与NaBr能否反应?_______ (填“否”或书写反应的离子方程式)。
(4)已知NH3和Cl2可以发生氧化还原反应,配平该方程式:_______ 。
_______NH3+_______Cl2=_______N2+_______HCl
(5)在硫酸溶液中,NaClO3和Na2SO3能按物质的量之比1∶2完全反应,生成一种棕黄色气体X,同时Na2SO3被氧化为Na2SO4,则X为_______。
(1)Cl-、Br-、I-、S2-四种离子的还原性由强到弱的顺序是
(2)判断Cl2与Na2S能否反应?
(3)判断I2与NaBr能否反应?
(4)已知NH3和Cl2可以发生氧化还原反应,配平该方程式:
_______NH3+_______Cl2=_______N2+_______HCl
(5)在硫酸溶液中,NaClO3和Na2SO3能按物质的量之比1∶2完全反应,生成一种棕黄色气体X,同时Na2SO3被氧化为Na2SO4,则X为_______。
| A.Cl2O7 | B.ClO2 | C.Cl2O | D.Cl2 |
您最近半年使用:0次
3 . 关于反应H2O+SO2+HClO=H2SO4(稀)+HCl,下列说法正确的是
| A.HClO发生氧化反应 |
| B.氧化性:HClO>H2SO4(稀) |
| C.参加反应的还原剂与氧化剂的质量之比为1∶1 |
| D.每生成2molHCl,转移2mol电子 |
您最近半年使用:0次
4 . 已知反应(1)、(2)分别是从海藻灰和智利硝石中提取碘的主要反应:
(1)2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
(2)2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是
(1)2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
(2)2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是
| A.两个反应中NaHSO4均为氧化产物 |
| B.I2在反应(1)中是还原产物,在反应(2)中是氧化产物 |
C.氧化性:MnO2>IO >I2 >I2 |
| D.反应(1)、(2)中生成等量的I2时转移电子数之比为1:5 |
您最近半年使用:0次
解题方法
5 . 氧化还原反应是一类非常重要的反应.回答下列问题:
(1)按如图所示操作,充分反应后.

①Ⅰ中发生反应的离子方程式为:____________________________________ 。
②Ⅱ中溶液中观察到的现象是:____________________________________ 。
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为:____________________ 。
(2)火药是中国的“四大发明”之一,黑火药在发生爆炸时,发生如下反应: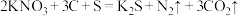 ,其中氧化产物是
,其中氧化产物是_______ .
(3)人体内的铁元素以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转化成Fe2+,有利于人体吸收,说明维生素C具有_______ (填“氧化性”或“还原性”)。
(4)市场上出售的某种麦片中含有微量铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成Fe2+。用单线桥法标出该化学方程式反应电子转移数目为_____________ 。
(5)写出氢气还原氧化铜的化学方程式,用双线桥法表示电子转移的方向数目:___________________________ .
(6)在 的反应中,每有1个Fe参加反应,被还原的HNO3为
的反应中,每有1个Fe参加反应,被还原的HNO3为_______ 个。
(1)按如图所示操作,充分反应后.

①Ⅰ中发生反应的离子方程式为:
②Ⅱ中溶液中观察到的现象是:
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为:
(2)火药是中国的“四大发明”之一,黑火药在发生爆炸时,发生如下反应:
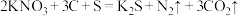 ,其中氧化产物是
,其中氧化产物是(3)人体内的铁元素以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转化成Fe2+,有利于人体吸收,说明维生素C具有
(4)市场上出售的某种麦片中含有微量铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成Fe2+。用单线桥法标出该化学方程式反应电子转移数目为
(5)写出氢气还原氧化铜的化学方程式,用双线桥法表示电子转移的方向数目:
(6)在
 的反应中,每有1个Fe参加反应,被还原的HNO3为
的反应中,每有1个Fe参加反应,被还原的HNO3为
您最近半年使用:0次
名校
解题方法
6 . 已知反应① 和②
和② 。下列说法错误的是
。下列说法错误的是
 和②
和② 。下列说法错误的是
。下列说法错误的是A.反应①中氧化产物与还原产物均为 |
B.反应①中 具有遇淀粉溶液变蓝的特性 具有遇淀粉溶液变蓝的特性 |
C.反应②中 是导致酸雨的主要有害污染物 是导致酸雨的主要有害污染物 |
D.由反应①和②可判断氧化性: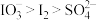 |
您最近半年使用:0次
2024-02-26更新
|
252次组卷
|
2卷引用:河北省唐山市2023-2024学年高一上学期1月期末考试化学试题
解题方法
7 . 对于下列实验,能正确描述其反应的离子方程式是
A.向Ba(OH)2溶液中滴加NaHSO4溶液至Ba2+恰好沉淀: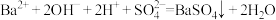 |
B.向NH4HSO4溶液中滴入过量的NaOH溶液: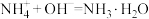 |
| C.向FeI2和FeBr2的混合溶液中通入少量氯气:Cl2+2I-=I2+2Cl- |
D.过氧化钠与水反应: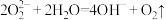 |
您最近半年使用:0次
8 . 已知常温下在溶液中可发生如下两个离子反应:


由此可以确定 、
、 、
、 三种离子的还原性由弱到强的顺序是
三种离子的还原性由弱到强的顺序是


由此可以确定
 、
、 、
、 三种离子的还原性由弱到强的顺序是
三种离子的还原性由弱到强的顺序是A. | B.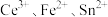 |
C.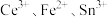 | D.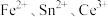 |
您最近半年使用:0次
9 . 甲钴胺是神经元营养药物,由C、H、Co、N、O、P元素组成。下列说法正确的是
A.还原性: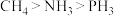 |
| B.基态P原子的最高能级轨道形状为球形 |
| C.同周期中第一电离能小于N的元素有5种 |
D.基态Co原子价层电子轨道表示式为 |
您最近半年使用:0次
2024-02-24更新
|
152次组卷
|
2卷引用:山东省淄博市2023-2024学年高二上学期教学质量检测化学试题
名校
解题方法
10 . 将一定量的铁粉投入硫酸铜和硫酸铁混合溶液中充分反应,下列说法正确的是
A.反应后若无固体剩余,则溶液中一定含有 |
B.反应后若无固体剩余,则溶液中一定含有 |
| C.反应后若有固体,则固体一定为Fe和Cu的混合物 |
D.反应后若有固体,则溶液中的金属离子只有 |
您最近半年使用:0次



