1 . 目前生产钛的方法之一是先将TiO2转化为TiCl4,再进一步还原得到钛。以下是碳氯化法制备TiCl4:TiO2(s)+2Cl2(g)+2C(s) TiCl4(g)+2CO(g) ∆H
TiCl4(g)+2CO(g) ∆H kJ·mol−1。
kJ·mol−1。
(1)对于该反应:增大压强,平衡___________ 移动(填“正向”“不”或“逆向”);温度升高,平衡转化率___________ (填“增大”“减小”或“不变”)。
(2)恒温恒容时,下列叙述一定能说明该反应达到平衡状态的是______。
(3)在某温度下,该恒容体系已经达到平衡,若向其中加入少量碳,TiCl4的体积分数将___________ (填选项);若加入少量氯气,TiCl4的体积分数将___________ (填选项)。
A.减小 B.不变 C.增大
 TiCl4(g)+2CO(g) ∆H
TiCl4(g)+2CO(g) ∆H kJ·mol−1。
kJ·mol−1。(1)对于该反应:增大压强,平衡
(2)恒温恒容时,下列叙述一定能说明该反应达到平衡状态的是______。
| A.混合气体的压强保持不变 | B.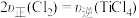 |
| C.混合气体的密度保持不变 | D.Cl2和CO物质的量相等 |
A.减小 B.不变 C.增大
您最近半年使用:0次
2 . 氢能是一种重要的绿色能源,在实现“碳中和”与“碳达峰”目标中起到重要作用。乙醇与水催化重整制氢发生以下反应:
反应Ⅰ: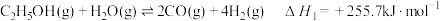
反应Ⅱ: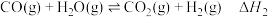
回答下列问题:
(1)①已知反应Ⅲ: ,则
,则
______  。
。
②反应I能自发进行的条件为______ 。
(2)压强为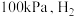 的平衡产率与温度、起始时
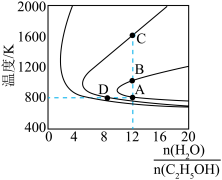
的平衡产率与温度、起始时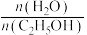 的关系如图所示,每条曲线表示
的关系如图所示,每条曲线表示
相同 的平衡产率。
______ 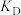 (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
② 的产率:B点
的产率:B点______ C点(填“>”、“=”或“<”);
③A、B两点 产率相等的原因是
产率相等的原因是______ 。
(3)压强为 下,
下, 和
和 发生上述反应,平衡时
发生上述反应,平衡时 和
和 的选择性、乙醇的转化率随温度的升高曲线如图所示。[已知:CO的选择性
的选择性、乙醇的转化率随温度的升高曲线如图所示。[已知:CO的选择性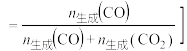
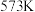 时,10分钟反应达到平衡,则乙醇的物质的量的变化量
时,10分钟反应达到平衡,则乙醇的物质的量的变化量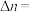
______ mol。
②表示 选择性的曲线是
选择性的曲线是______ (填标号)。
③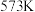 时,反应II的
时,反应II的
______ (保留三位有效数字)。
反应Ⅰ:
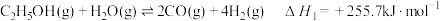
反应Ⅱ:
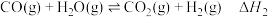
回答下列问题:
(1)①已知反应Ⅲ:
 ,则
,则
 。
。②反应I能自发进行的条件为
(2)压强为
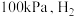 的平衡产率与温度、起始时
的平衡产率与温度、起始时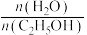 的关系如图所示,每条曲线表示
的关系如图所示,每条曲线表示

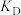 (填“>”、“=”或“<”)
(填“>”、“=”或“<”)②
 的产率:B点
的产率:B点③A、B两点
 产率相等的原因是
产率相等的原因是(3)压强为
 下,
下, 和
和 发生上述反应,平衡时
发生上述反应,平衡时 和
和 的选择性、乙醇的转化率随温度的升高曲线如图所示。[已知:CO的选择性
的选择性、乙醇的转化率随温度的升高曲线如图所示。[已知:CO的选择性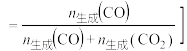
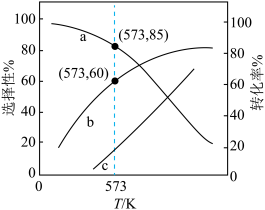
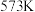 时,10分钟反应达到平衡,则乙醇的物质的量的变化量
时,10分钟反应达到平衡,则乙醇的物质的量的变化量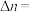
②表示
 选择性的曲线是
选择性的曲线是③
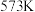 时,反应II的
时,反应II的
您最近半年使用:0次
3 . 2NO2(g)  N2O4(g),
N2O4(g),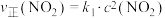 ,
,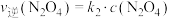 ,其中
,其中 、
、 只与温度有关,T0时,
只与温度有关,T0时, ,将一定量的
,将一定量的 充入注射器中,改变活塞位置,气体透光率随时间的变化如下图所示(气体颜色越深,透光率越低),下列说法错误的是
充入注射器中,改变活塞位置,气体透光率随时间的变化如下图所示(气体颜色越深,透光率越低),下列说法错误的是
 N2O4(g),
N2O4(g),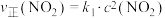 ,
,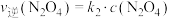 ,其中
,其中 、
、 只与温度有关,T0时,
只与温度有关,T0时, ,将一定量的
,将一定量的 充入注射器中,改变活塞位置,气体透光率随时间的变化如下图所示(气体颜色越深,透光率越低),下列说法错误的是
充入注射器中,改变活塞位置,气体透光率随时间的变化如下图所示(气体颜色越深,透光率越低),下列说法错误的是
A.d点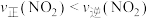 |
| B.T0时,K=0.5 |
C.T1时, ,则T1<T0 ,则T1<T0 |
D.保持容积不变,再充入一定量 气体, 气体, 的平衡转化率不变 的平衡转化率不变 |
您最近半年使用:0次
4 . 在四个不同容积的恒容密闭容器中按图甲充入相应的气体,发生反应:2N2O(g) 2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图乙所示。
2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图乙所示。
_____ (选填“>”或“<”)0.
(2)若容器Ⅰ的体积为2L,反应在370℃下进行,20s后达到平衡,则从起始到平衡过程中N2O反应速率为_____ 。
(3)容器Ⅱ中,反应在B点时对应的平衡常数K=_____ (保留两位有效数字)。
(4)根据题给信息,下列有关说法正确的是_____。
(5)若容器Ⅳ的体积为1L,反应在370℃下进行,则起始时反应_____
 2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图乙所示。
2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O的平衡转化率如图乙所示。

(2)若容器Ⅰ的体积为2L,反应在370℃下进行,20s后达到平衡,则从起始到平衡过程中N2O反应速率为
(3)容器Ⅱ中,反应在B点时对应的平衡常数K=
(4)根据题给信息,下列有关说法正确的是_____。
| A.体积之比:VⅠ>VⅡ>VⅢ |
| B.容器Ⅲ中,当N2与O2物质的量之比为2:1时反应达平衡状态 |
| C.图乙中A、C、D对应的容器中混合气体平均相对分子质量相等 |
| D.图乙中A、C、D三点由于转化率相等,因而平衡常数相等 |
| A.υ正>υ逆 | B.υ正<υ逆 | C.υ正=υ逆 |
您最近半年使用:0次
5 . 氨分解制氢是一种极具前景的便携式制氢方法,不同压强下氨的平衡转化率随温度变化如下。下列说法正确的是
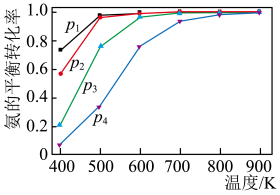
A.2NH3  3H2 + N2 ΔH < 0 3H2 + N2 ΔH < 0 |
| B.氢气和氮气的物质的量之比保持不变,说明氨分解反应达到平衡状态 |
| C.p1 < p2 < p3 < p4 |
| D.500 K时,p3压强下氨分解反应的平衡常数比p4压强下的大 |
您最近半年使用:0次
6 . 从烟道废气中回收硫的原理之一: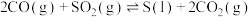
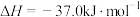 ,在恒压密闭容器中,平衡时SO2的转化率
,在恒压密闭容器中,平衡时SO2的转化率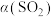 与起始充入的
与起始充入的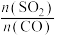 和温度(T)的关系如图所示。下列说法中正确的是
和温度(T)的关系如图所示。下列说法中正确的是
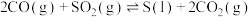
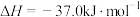 ,在恒压密闭容器中,平衡时SO2的转化率
,在恒压密闭容器中,平衡时SO2的转化率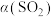 与起始充入的
与起始充入的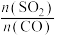 和温度(T)的关系如图所示。下列说法中正确的是
和温度(T)的关系如图所示。下列说法中正确的是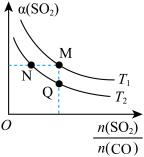
A.正反应的活化能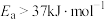 |
B.CO的转化率 :M>N :M>N |
C.正反应速率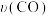 :M>Q :M>Q |
D.该反应的化学平衡常数表达式: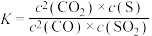 |
您最近半年使用:0次
2024-04-17更新
|
452次组卷
|
4卷引用:2024届河北省张家口市高三下学期一模化学试题
2024届河北省张家口市高三下学期一模化学试题河北省沧州市2024届高三下学期一模化学试卷(已下线)通关练08 聚焦反应热、速率及化学平衡-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)题型7 化学反应速率与化学平衡 水溶液中的离子反应与平衡(25题)-2024年高考化学常考点必杀300题(新高考通用)
7 . 苯乙烯是制备高分子的原料.乙苯脱氢制苯乙烯的反应如下:
反应I:
制备过程中会发生如下两个副反应:
反应Ⅱ:
反应Ⅲ:
在 下,将质量比为
下,将质量比为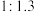 的水蒸气和乙苯在催化剂作用下反应,测得乙苯的转化率、苯乙烯、苯、甲苯的选择性与时间的关系如下图所示.
的水蒸气和乙苯在催化剂作用下反应,测得乙苯的转化率、苯乙烯、苯、甲苯的选择性与时间的关系如下图所示.
苯乙烯的选择性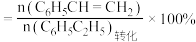
苯的选择性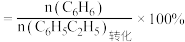
甲苯的选择性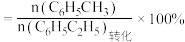
下列说法不正确 的是
反应I:

制备过程中会发生如下两个副反应:
反应Ⅱ:

反应Ⅲ:

在
 下,将质量比为
下,将质量比为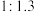 的水蒸气和乙苯在催化剂作用下反应,测得乙苯的转化率、苯乙烯、苯、甲苯的选择性与时间的关系如下图所示.
的水蒸气和乙苯在催化剂作用下反应,测得乙苯的转化率、苯乙烯、苯、甲苯的选择性与时间的关系如下图所示.苯乙烯的选择性
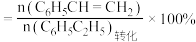
苯的选择性
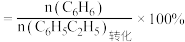
甲苯的选择性
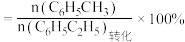
下列说法

| A.曲线a表示乙苯的转化率 |
B. 时,所得 时,所得 的物质的量逐渐减少 的物质的量逐渐减少 |
| C.其他条件不变,增大水蒸气与乙苯的质量比,可以提高乙苯的平衡转化率 |
D. 时,苯乙烯选择性下降的原因之一是反应I生成的 时,苯乙烯选择性下降的原因之一是反应I生成的 促进了反应Ⅲ的进行 促进了反应Ⅲ的进行 |
您最近半年使用:0次
8 . 下列事实能用勒夏特列原理解释的
| A.用排饱和食盐水的方法收集氯气 |
B.500℃左右比室温更有利于工业合成 的反应 的反应 |
C.加入催化剂有利于 的氧化反应 的氧化反应 |
D.对 ,减小容器体积,气体颜色变深 ,减小容器体积,气体颜色变深 |
您最近半年使用:0次
9 . 碳粉高温下还原 制取纳米级
制取纳米级 :
: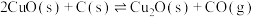
 ,反应达平衡后,下列说法正确的是
,反应达平衡后,下列说法正确的是
 制取纳米级
制取纳米级 :
: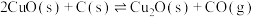
 ,反应达平衡后,下列说法正确的是
,反应达平衡后,下列说法正确的是A.升高温度, 增大、 增大、 减小 减小 |
B.保持温度不变,通入少量CO,达新平衡后 变大 变大 |
C.加入少量碳粉,可提高 的平衡转化率 的平衡转化率 |
D.分离出CO,有利于 的生成 的生成 |
您最近半年使用:0次
10 . 对于放热的可逆反应,某一给定转化率下,最大反应速率对应的温度称为最适宜温度。反应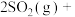
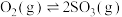
 在催化剂作用下原料的总转化率与最适宜温度(曲线Ⅰ)、原料的总平衡转化率与温度(曲线Ⅱ)的关系曲线示意图最合理的是
在催化剂作用下原料的总转化率与最适宜温度(曲线Ⅰ)、原料的总平衡转化率与温度(曲线Ⅱ)的关系曲线示意图最合理的是
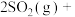
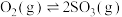
 在催化剂作用下原料的总转化率与最适宜温度(曲线Ⅰ)、原料的总平衡转化率与温度(曲线Ⅱ)的关系曲线示意图最合理的是
在催化剂作用下原料的总转化率与最适宜温度(曲线Ⅰ)、原料的总平衡转化率与温度(曲线Ⅱ)的关系曲线示意图最合理的是A.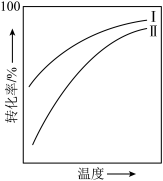 | B.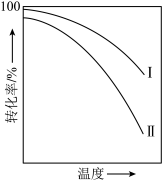 |
C.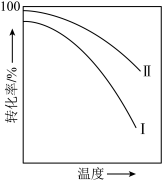 | D.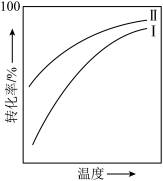 |
您最近半年使用:0次



