名校
解题方法
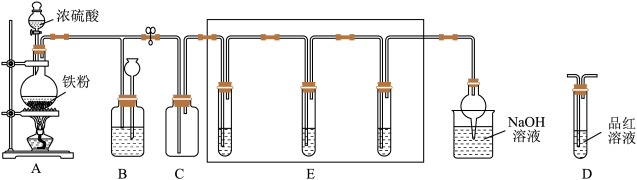
1 . 某化学兴趣小组为探究铁跟浓硫酸的反应,用如图所示装置进行有关实验。请回答下列问题: 的化学方程式:
的化学方程式:____________ 。
(2)甲同学欲确定C中的二氧化硫是否收集满,在CE之间加入装置D(如图所示),当观察到D中________________ 时,证明C中气体已满。不过他认为这样收集到的气体不纯,原因是_________ ,装置B的一个作用是储存多余的气体,B中应盛装的液体是________ (填标号)。
A.饱和 溶液 B.酸性
溶液 B.酸性 溶液 C.浓溴水 D.饱和
溶液 C.浓溴水 D.饱和 溶液
溶液
(3)乙同学设计装置E探究 的酸性强于HClO,E中三支试管中的试剂(足量)分别为①酸性
的酸性强于HClO,E中三支试管中的试剂(足量)分别为①酸性 溶液 ②漂白粉溶液 ③小苏打溶液,连接顺序为
溶液 ②漂白粉溶液 ③小苏打溶液,连接顺序为_____________ , 的酸性强于HClO的实验现象是
的酸性强于HClO的实验现象是________________ ;该现象能进一步说明硫和氯的非金属性强弱吗?请说明原因:_____________ 。
(4)丙同学欲探究铁与浓硫酸反应生成 的临界浓度,设计实验:将足量铁片和20mL 18
的临界浓度,设计实验:将足量铁片和20mL 18 浓硫酸放入圆底烧瓶中,有少量气体产生,反应很快停止,加热,充分反应产生大量气体直到反应完毕,然后用导管通入足量的
浓硫酸放入圆底烧瓶中,有少量气体产生,反应很快停止,加热,充分反应产生大量气体直到反应完毕,然后用导管通入足量的 ,以确保烧瓶中的
,以确保烧瓶中的 气体全部进入盛装了足量双氧水的烧杯中,将充分反应后的烧杯取下,向其中加入足量的
气体全部进入盛装了足量双氧水的烧杯中,将充分反应后的烧杯取下,向其中加入足量的 溶液,再过滤、洗涤、干燥,称量固体的质量为b g。浓硫酸与Fe反应生成
溶液,再过滤、洗涤、干燥,称量固体的质量为b g。浓硫酸与Fe反应生成 时的最低浓度为
时的最低浓度为__________ (列出含b的计算式即可) 。
。
 的化学方程式:
的化学方程式:(2)甲同学欲确定C中的二氧化硫是否收集满,在CE之间加入装置D(如图所示),当观察到D中
A.饱和
 溶液 B.酸性
溶液 B.酸性 溶液 C.浓溴水 D.饱和
溶液 C.浓溴水 D.饱和 溶液
溶液(3)乙同学设计装置E探究
 的酸性强于HClO,E中三支试管中的试剂(足量)分别为①酸性
的酸性强于HClO,E中三支试管中的试剂(足量)分别为①酸性 溶液 ②漂白粉溶液 ③小苏打溶液,连接顺序为
溶液 ②漂白粉溶液 ③小苏打溶液,连接顺序为 的酸性强于HClO的实验现象是
的酸性强于HClO的实验现象是(4)丙同学欲探究铁与浓硫酸反应生成
 的临界浓度,设计实验:将足量铁片和20mL 18
的临界浓度,设计实验:将足量铁片和20mL 18 浓硫酸放入圆底烧瓶中,有少量气体产生,反应很快停止,加热,充分反应产生大量气体直到反应完毕,然后用导管通入足量的
浓硫酸放入圆底烧瓶中,有少量气体产生,反应很快停止,加热,充分反应产生大量气体直到反应完毕,然后用导管通入足量的 ,以确保烧瓶中的
,以确保烧瓶中的 气体全部进入盛装了足量双氧水的烧杯中,将充分反应后的烧杯取下,向其中加入足量的
气体全部进入盛装了足量双氧水的烧杯中,将充分反应后的烧杯取下,向其中加入足量的 溶液,再过滤、洗涤、干燥,称量固体的质量为b g。浓硫酸与Fe反应生成
溶液,再过滤、洗涤、干燥,称量固体的质量为b g。浓硫酸与Fe反应生成 时的最低浓度为
时的最低浓度为 。
。
您最近半年使用:0次
名校
2 . 太空特殊环境对太空芯片有着极为苛刻的要求,太空芯片的材料有硅基芯片、GaN芯片、金刚石、石墨烯、AlN等。已知Ga与Al的性质相似,下列说法正确的是
| A.金刚石、石墨烯互为同位素 |
| B.上述物质涉及的元素均为短周期元素 |
C.使用石英砂与焦炭制备粗硅时发生的反应为 |
D.Ga与NaOH溶液反应的化学方程式为 |
您最近半年使用:0次
名校
3 . 下列物质的性质与用途的表述均正确且有对应关系的是
A. 两性,可用于制造耐高温陶瓷 两性,可用于制造耐高温陶瓷 |
| B.浓硝酸不与铁铝反应,可用铝制或铁制容器盛装浓硝酸 |
C. 具有还原性,可用作抗氧化剂添加到特定食品中 具有还原性,可用作抗氧化剂添加到特定食品中 |
D. 传输信号不衰减,可用做芯片 传输信号不衰减,可用做芯片 |
您最近半年使用:0次
名校
解题方法
4 . 根据下列实验操作和现象得出的结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向铁的氯化物溶液中滴入2滴酸性 溶液,酸性 溶液,酸性 溶液褪色 溶液褪色 | 氯化物中一定含有 |
| B | 向溶有 的 的 溶液中通入气体X,出现白色沉淀 溶液中通入气体X,出现白色沉淀 | X一定具有强氧化性 |
| C | 向铜与浓硫酸反应后的试管加水,观察溶液颜色 | Cu与浓 反应的氧化产物为 反应的氧化产物为 |
| D | 向某溶液中加入少量铜粉并振荡,铜粉不溶解,再滴入2滴稀硫酸,铜粉溶解,产生红棕色气体 | 原溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
5 .  可用作脱硝剂。某科研小组为了探究
可用作脱硝剂。某科研小组为了探究 能否被
能否被 还原,设计的装置如图所示(夹持、加热装置已略去,
还原,设计的装置如图所示(夹持、加热装置已略去, 、
、 为止水夹),下列说法不正确的是
为止水夹),下列说法不正确的是
 可用作脱硝剂。某科研小组为了探究
可用作脱硝剂。某科研小组为了探究 能否被
能否被 还原,设计的装置如图所示(夹持、加热装置已略去,
还原,设计的装置如图所示(夹持、加热装置已略去, 、
、 为止水夹),下列说法不正确的是
为止水夹),下列说法不正确的是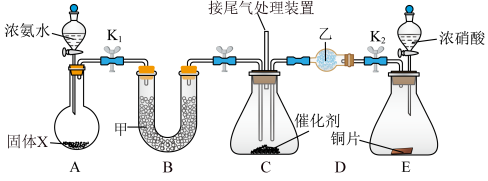
| A.固体X可以是碱石灰 |
| B.甲、乙试剂均可以是无水氯化钙 |
C.实验时宜先通入 ,再通入 ,再通入 有利于减少空气对实验的干扰 有利于减少空气对实验的干扰 |
| D.装置C的反应中n(还原剂)∶n(氧化剂)=4∶3 |
您最近半年使用:0次
解题方法
6 . 丰富多彩的氯家族
18世纪70年代,瑞典化学家舍勒将软锰矿主要成分是MnO2与浓盐酸混合加热。产生了氯气。氯气是一种重要的化工原料,工业上大量用于制造盐酸、次氯酸盐、有机溶剂、农药、染料和药品等,从而形成了品种繁多、功能各异的氯家族。工业上通过电解饱和食盐水的方法制取率气,称为氯碱工业,氯碱工业的产品除应用于化学工业本身之外,还广泛应用于冶金、造纸、农药、有机合成等工业。食盐水在电解前需要精制,主要是为了除去混在氯化钠中的杂质。1.下列物质不能通过单质间的化合反应得到的是________。
| A.FeCl2 | B.FeCl3 | C.CuCl2 | D.HCl |
3.将一瓶新制的氯水长期放置后,溶液中离子取分子浓度不会减少的是________。
| A.Cl2 | B.Cl- | C.H2O | D.HClO |

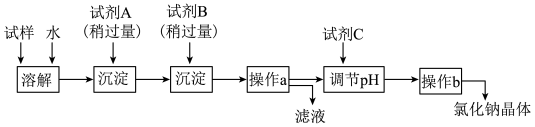
②试剂B是
③试剂C是
④操作b的名称是
您最近半年使用:0次
7 . 下列有关物质的性质与用途不具有对应关系的是
| A.干冰升华时吸热,可用作人工降雨 |
B. 吸收 吸收 产生 产生 ,可用作呼吸面具供氧剂 ,可用作呼吸面具供氧剂 |
C. 溶液显酸性,可蚀刻印刷电路板上的Cu 溶液显酸性,可蚀刻印刷电路板上的Cu |
D. 固体受热分解产生 固体受热分解产生 ,可用作膨松剂 ,可用作膨松剂 |
您最近半年使用:0次
名校
解题方法
8 . 实验小组研究铜与过量硝酸的反应,实验如下(加持装置和尾气处理装置略)。
(1)氮在元素周期表中的位置为___________ 。
(2)实验Ⅰ、Ⅱ中的红棕色气体均是NO2.实验Ⅰ产生NO2的化学方程式是___________ 。
(3)对实验Ⅰ产生NO2,实验Ⅱ产生NO的原因提出解释。
①硝酸浓度越稀,溶液中单位体积内的NO 数目越少。被还原时,每个NO
数目越少。被还原时,每个NO 从铜片处获得较多电子的机会越
从铜片处获得较多电子的机会越___________ (填“大”或“小”),因此越易被还原为较低价态的含氮物质。
②浓硝酸具有较强的___________ 性,可将NO转化为NO2。
(4)有同学针对I中溶液呈绿色的原因,提出假设:
假设1:Cu2+的浓度较大所致;假设2:溶解了生成的NO2。
探究如下:取I中绿色溶液,分为两等份。
①取一份于如图所示装置中,向上拉动活塞a,___________ (填现象),证实I中溶解了NO2。___________ (填化学试剂),溶液变为蓝色。证实假设1不成立,假设2成立。
(5)硝酸与金属反应会产生氮氧化物。
①下列环境问题与氮的氧化物排放无关的是___________ 。
A.酸雨B.光化学烟雾C温室效应 D.白色污染
②在含有agHNO3的稀硝酸中,加入bg铁粉充分反应,铁全部溶解并生成NO,有0.25agHNO3被还原,则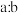 可能为
可能为___________ 。
A.2:1 B.3:1 C.4:1 D.9:2
③为避免氮氧化物污染环境,人们开发了溶液吸收法。比如用碱性的Na2CO3溶液吸收NO2,请写出相关的化学反应方程式:___________ 。
| 装置 | 编号 | 试剂a | 现象 |
| Ⅰ | 4mL浓硝酸(过量) | 铜片完全溶解,溶液变绿,出现大量红棕色气体 |
| Ⅱ | 4mL稀硝酸(过量) | 铜片完全溶解,溶液变蓝,液面上方气体呈浅红棕色 |
(1)氮在元素周期表中的位置为
(2)实验Ⅰ、Ⅱ中的红棕色气体均是NO2.实验Ⅰ产生NO2的化学方程式是
(3)对实验Ⅰ产生NO2,实验Ⅱ产生NO的原因提出解释。
①硝酸浓度越稀,溶液中单位体积内的NO
 数目越少。被还原时,每个NO
数目越少。被还原时,每个NO 从铜片处获得较多电子的机会越
从铜片处获得较多电子的机会越②浓硝酸具有较强的
(4)有同学针对I中溶液呈绿色的原因,提出假设:
假设1:Cu2+的浓度较大所致;假设2:溶解了生成的NO2。
探究如下:取I中绿色溶液,分为两等份。
①取一份于如图所示装置中,向上拉动活塞a,

(5)硝酸与金属反应会产生氮氧化物。
①下列环境问题与氮的氧化物排放无关的是
A.酸雨B.光化学烟雾C温室效应 D.白色污染
②在含有agHNO3的稀硝酸中,加入bg铁粉充分反应,铁全部溶解并生成NO,有0.25agHNO3被还原,则
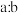 可能为
可能为A.2:1 B.3:1 C.4:1 D.9:2
③为避免氮氧化物污染环境,人们开发了溶液吸收法。比如用碱性的Na2CO3溶液吸收NO2,请写出相关的化学反应方程式:
您最近半年使用:0次
7日内更新
|
114次组卷
|
2卷引用:四川省绵阳南山中学2023-2024学年高一下学期3月月考试题 化学试题
名校
解题方法
9 . 下列关于硅及其化合物的叙述中,错误的是
| A.二氧化硅可用于生产玻璃 |
B.虽然 为酸性氧化物,但可以用带橡胶塞的玻璃瓶盛放 为酸性氧化物,但可以用带橡胶塞的玻璃瓶盛放 溶液 溶液 |
| C.硅是应用最广泛的半导体材料,所以常用作光导纤维 |
| D.硅酸盐材料大多化学性质稳定,是因为其结构中含有硅氧四面体 |
您最近半年使用:0次
解题方法
10 . 下列说法中,正确的是
| A.所有非金属元素都分布在p区 |
| B.最外层电子数为2的元素都分布在s区 |
| C.元素周期表中从第IIIB族到第IIB族的10个纵列的元素都是金属元素 |
| D.第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性 |
您最近半年使用:0次