名校
1 . 硫酸亚铁铵 是分析化学中的重要试剂。隔绝空气加热至
是分析化学中的重要试剂。隔绝空气加热至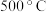 时硫酸亚铁铵能完全分解,分解产物中含有铁的氧化物、疏的氧化物、氨气和水蒸气等。
时硫酸亚铁铵能完全分解,分解产物中含有铁的氧化物、疏的氧化物、氨气和水蒸气等。
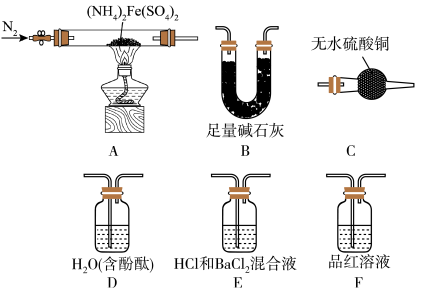
[实验探究]某化学小组选用如图所示部分装置进行实验(夹持装置略)
(2)有关硫酸亚铁铵所含的元素,下列说法正确的是___________。
实验I:探究分解产物中硫的氧化物,连接装置A-E-F-B进行实验。
(3)实验现象:E中没有明显现象,F中溶液褪色,据此得出的结论是___________ 。
实验Ⅱ:验证分解产物中含有氨气和水蒸气、探究残留固体成分。连接A-C-B-D进行实验。
(4)关于氨气和水,下列说法错误的是___________。
(5)装置B在实验Ⅱ中的作用是___________ 。
(6)A中固体完全分解后变为红棕色粉末,设计实验证明A中残留固体仅为Fe2O3
,而不含 或
或 :
:___________ 。
(7)实验证明 受热分解除生成上述两个实验中的产物外,还有
受热分解除生成上述两个实验中的产物外,还有 产生,写出A中反应的化学方程式
产生,写出A中反应的化学方程式___________ 。
实验Ⅲ:为测定硫酸亚铁铵 晶体纯度,某同学取m克硫酸亚铁铵晶体样品配成
晶体纯度,某同学取m克硫酸亚铁铵晶体样品配成 溶液,取
溶液,取 硫酸亚铁铵溶液进行如下实验:
硫酸亚铁铵溶液进行如下实验:___________ (用含w、m的式子表示)。
(9)若缺少“洗涤”步骤,最终结果会___________ (填偏大、偏小或不变)。
 是分析化学中的重要试剂。隔绝空气加热至
是分析化学中的重要试剂。隔绝空气加热至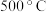 时硫酸亚铁铵能完全分解,分解产物中含有铁的氧化物、疏的氧化物、氨气和水蒸气等。
时硫酸亚铁铵能完全分解,分解产物中含有铁的氧化物、疏的氧化物、氨气和水蒸气等。[实验探究]某化学小组选用如图所示部分装置进行实验(夹持装置略)
| A.溶于水部分电离 | B.固体中只有离子键 |
| C.固体中既含离子键又含共价键 | D.能发生复分解反应或氧化还原反应 |
(2)有关硫酸亚铁铵所含的元素,下列说法正确的是___________。
| A.都位于短周期 | B.只有一个副族元素 |
C.同主族元素非金属性: | D.同周期元素原子半径: |
实验I:探究分解产物中硫的氧化物,连接装置A-E-F-B进行实验。
(3)实验现象:E中没有明显现象,F中溶液褪色,据此得出的结论是
实验Ⅱ:验证分解产物中含有氨气和水蒸气、探究残留固体成分。连接A-C-B-D进行实验。
(4)关于氨气和水,下列说法错误的是___________。
| A.都是弱电解质 | B.都是共价化合物 | C.都是以分子构成物质 | D.氨水中只有两种离子 |
(5)装置B在实验Ⅱ中的作用是
(6)A中固体完全分解后变为红棕色粉末,设计实验证明A中残留固体仅为Fe2O3
,而不含
 或
或 :
:(7)实验证明
 受热分解除生成上述两个实验中的产物外,还有
受热分解除生成上述两个实验中的产物外,还有 产生,写出A中反应的化学方程式
产生,写出A中反应的化学方程式实验Ⅲ:为测定硫酸亚铁铵
 晶体纯度,某同学取m克硫酸亚铁铵晶体样品配成
晶体纯度,某同学取m克硫酸亚铁铵晶体样品配成 溶液,取
溶液,取 硫酸亚铁铵溶液进行如下实验:
硫酸亚铁铵溶液进行如下实验:
(9)若缺少“洗涤”步骤,最终结果会
您最近半年使用:0次
名校
解题方法
2 . 向一定质量的Cu和Cu2O组成的混合物中加入一定浓度的稀硝酸250mL,当固体物质完全溶解后生成Cu(NO3)2和2.24LNO气体(标况下)。在所得溶液中加入0.5mol/L的NaOH溶液1.0L,生成沉淀的质量为19.6g,此时溶液呈中性且铜离子已完全沉淀。下列有关说法正确的是
| A.Cu、Cu2O与硝酸反应后剩余的HNO3为0.1mol |
| B.原稀硝酸中HNO3的物质的量浓度为2.6mol/L |
| C.铜离子刚好沉淀完全,溶液中溶质为NaNO3,浓度为0.5mol/L |
| D.原固体混合物中Cu和Cu2O的物质的量之比为1:2 |
您最近半年使用:0次
2024-04-15更新
|
270次组卷
|
2卷引用:四川省绵阳南山中学2023-2024学年高一下学期3月月考试题 化学试题
名校
解题方法
3 . 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球体积的影响)。则滴管和烧瓶中所用试剂可能是
甲 | 乙 | ||
A | 稀硫酸和铜片 | 水和 |
|
B | 双氧水和 | NaOH溶液和 | |
C |
| NaOH溶液和 | |
D |
| 硝酸银溶液和HCl |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
4 . 类比法可预测物质的性质。如根据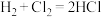 推测
推测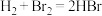 。但类比是相对的,如根据
。但类比是相对的,如根据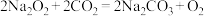 推测
推测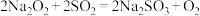 是错误的,应该是
是错误的,应该是 。下列各组类比中正确的是
。下列各组类比中正确的是
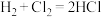 推测
推测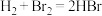 。但类比是相对的,如根据
。但类比是相对的,如根据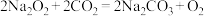 推测
推测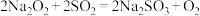 是错误的,应该是
是错误的,应该是 。下列各组类比中正确的是
。下列各组类比中正确的是A.钠与水反应生成NaOH和 ,推测:所有金属与水反应都生成碱和 ,推测:所有金属与水反应都生成碱和 |
B.由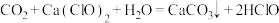 ,推测: ,推测: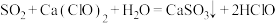 |
C.由 与 与 不反应,推测: 不反应,推测: 与 与 不反应 不反应 |
D.由 ,推测: ,推测: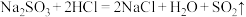 |
您最近半年使用:0次
名校
解题方法
5 . I.某实验小组利用以下装置制取氨气并探究氨气的性质:
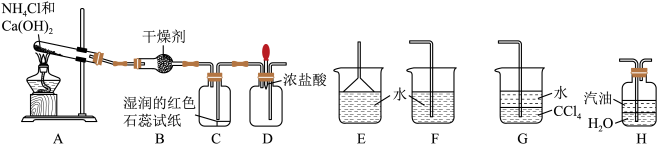
(1)装置B中的干燥剂是____________ (填名称)。
(2)装置C中的现象是____________ 。
(3)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是_________ ,发生反应的化学方程式为______________ 。
(4)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置是____________ 或_____________ (填“E”、“F”、“G”或“H”)。
Ⅱ.为探究氨的还原性,某同学设计了如图所示实验装置(其中夹持装置略去),在实验室中进行实验探究。回答下列问题
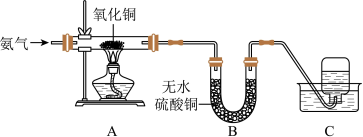
实验现象:A中氧化铜全部转化成光亮的红色固体,B中U形管内物质变蓝
(5)C中集气瓶内收集到一种无色气态单质,该气体用排水法收集的理由是____________ 。
(6)从C中水槽里取适量液体于试管内,向试管里滴入无色酚酞试液,溶液呈红色,原因是______________ 。
实验结论:
(7)氧化铜可以和氨气发生反应,化学方程式是___________ 。

(1)装置B中的干燥剂是
(2)装置C中的现象是
(3)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(4)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置是
Ⅱ.为探究氨的还原性,某同学设计了如图所示实验装置(其中夹持装置略去),在实验室中进行实验探究。回答下列问题

实验现象:A中氧化铜全部转化成光亮的红色固体,B中U形管内物质变蓝
(5)C中集气瓶内收集到一种无色气态单质,该气体用排水法收集的理由是
(6)从C中水槽里取适量液体于试管内,向试管里滴入无色酚酞试液,溶液呈红色,原因是
实验结论:
(7)氧化铜可以和氨气发生反应,化学方程式是
您最近半年使用:0次
名校
解题方法
6 . 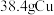 与一定量浓硝酸恰好完全反应生成氮的氧化物,这些氧化物恰好溶解在
与一定量浓硝酸恰好完全反应生成氮的氧化物,这些氧化物恰好溶解在 溶液中得到
溶液中得到 和
和 的混合溶液,反应过程及有关数据如图所示
的混合溶液,反应过程及有关数据如图所示
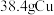 与一定量浓硝酸恰好完全反应生成氮的氧化物,这些氧化物恰好溶解在
与一定量浓硝酸恰好完全反应生成氮的氧化物,这些氧化物恰好溶解在 溶液中得到
溶液中得到 和
和 的混合溶液,反应过程及有关数据如图所示
的混合溶液,反应过程及有关数据如图所示
| A.硝酸在反应中既体现氧化性又体现酸性 |
B.氮的氧化物和 溶液反应时, 溶液反应时, 作还原剂 作还原剂 |
C.混合气体中 的物质的量是 的物质的量是 ,生成 ,生成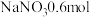 |
D.若浓硝酸体积为 ,则其物质的量浓度为 ,则其物质的量浓度为 |
您最近半年使用:0次
2024-04-04更新
|
473次组卷
|
3卷引用:湖北省武汉市第二中学2023-2024学年高一下学期化学周练A卷(1)试卷
名校
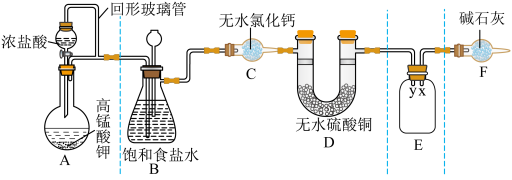
7 . 某同学用 与浓盐酸反应制备纯净的
与浓盐酸反应制备纯净的 的装置如图所示。回答下列问题:
的装置如图所示。回答下列问题:
已知: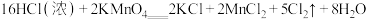
(1)装置A中盛放浓盐酸的仪器名称是
(2)E装置中导管(填“x”或“y”)
(3)装置F的作用有两个:一是
请写出氯气与碱石灰反应的化学方程式
(4)
 、HClO和
、HClO和 三种微粒的物质的量分数随pH(即
三种微粒的物质的量分数随pH(即 )变化的关系如图所示。
)变化的关系如图所示。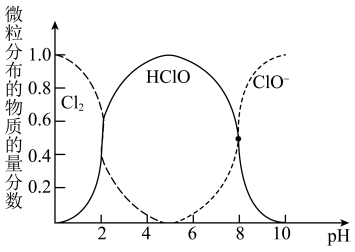
回答问题:①使用84消毒液时为增强消毒效果常调节4<pH<6,原因是
②通常购买的84消毒液pH在12左右,为增强消毒效果可向其中滴加
A.可口可乐 B.稀 C.食醋 D.浓盐酸
C.食醋 D.浓盐酸
(5)实验室将
 通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为
通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为 ,计算此时所得溶液中NaClO的质量分数为
,计算此时所得溶液中NaClO的质量分数为
您最近半年使用:0次
解题方法
8 . 下列实验操作、现象、结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用铁丝蘸取某溶液于酒精灯上灼烧 | 火焰呈黄色 | 该溶液为钠盐溶液 |
| B | 向Al(OH)3沉淀中滴加NaOH溶液 | 沉淀溶解 | Al有一定的非金属性 |
| C | 在一支试管中先加入1mLNa2S溶液,边振荡边向其中滴加Na2SO3溶液 | 混合液呈浑浊 | 说明有硫单质生成 |
| D | 向某溶液中加入NaOH溶液并加热,在试管口用湿润蓝色石蕊试纸检验 | 试纸变红色 | 该溶液中有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
9 . 向100mLNaOH溶液中通入一定量的CO2气体。充分反应后。再向所得溶液中逐滴加入0.2ml/L的盐酸。产生CO2气体的体积与所加盐酸体积之间的关系如图所示。下列判断正确的是


| A.所得溶液溶质成分为NaOH和Na2CO3 |
| B.通入CO2在标准状况下的体积为448mL |
| C.原NaOH溶液的浓度为0.2mol/L |
| D.所得溶液溶质成分的物质的量之比为1:3 |
您最近半年使用:0次
名校
解题方法
10 . 将一定量的氯气通入30ml浓度为10mol/L的氢氧化钠浓溶液中,加热少许时间后恰好完全反应,形成了 、
、 、
、 共存体系,下列判断不正确的是
共存体系,下列判断不正确的是
 、
、 、
、 共存体系,下列判断不正确的是
共存体系,下列判断不正确的是A.当溶液中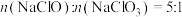 时,反应的离子方程式为 时,反应的离子方程式为 |
B.与 反应的氯气为3.36L 反应的氯气为3.36L |
C. 可能为8∶3∶1 可能为8∶3∶1 |
D.溶液中氯离子的物质的量取值范围是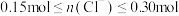 |
您最近半年使用:0次




 和
和


