名校
解题方法
1 . 硅、硫、氮等非金属元素在化工生产中扮演着重要角色。
(1)下列物品或设施:①陶瓷餐具②门窗玻璃③水晶镜片④硅太阳能电池⑤光导纤维⑥手机芯片。
直接使用了硅单质的是_______ (用序号填空)。
(2)写出实验室用Cu制备 的化学方程式:
的化学方程式:_______
(3)下列五种有色溶液与 作用均能褪色
作用均能褪色
①品红溶液②酸性 溶液③溴水④滴有酚酞的NaOH溶液⑤淀粉-碘溶液
溶液③溴水④滴有酚酞的NaOH溶液⑤淀粉-碘溶液
体现了 还原性的是(用序号填空)
还原性的是(用序号填空)_______ 。
(4)氮氧化物(NO、 )、
)、 会造成的环境问题有
会造成的环境问题有_______ (写一种即可)。
(5)如图包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室制备并收集 ,制备原理为
,制备原理为_______ (用化学方程式表示);应选择的装置是_______ (填字母)。 的化学反应方程式:
的化学反应方程式:_______
(1)下列物品或设施:①陶瓷餐具②门窗玻璃③水晶镜片④硅太阳能电池⑤光导纤维⑥手机芯片。
直接使用了硅单质的是
(2)写出实验室用Cu制备
 的化学方程式:
的化学方程式:(3)下列五种有色溶液与
 作用均能褪色
作用均能褪色①品红溶液②酸性
 溶液③溴水④滴有酚酞的NaOH溶液⑤淀粉-碘溶液
溶液③溴水④滴有酚酞的NaOH溶液⑤淀粉-碘溶液体现了
 还原性的是(用序号填空)
还原性的是(用序号填空)(4)氮氧化物(NO、
 )、
)、 会造成的环境问题有
会造成的环境问题有(5)如图包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室制备并收集
 ,制备原理为
,制备原理为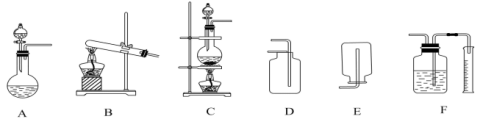
 的化学反应方程式:
的化学反应方程式:
您最近半年使用:0次
名校
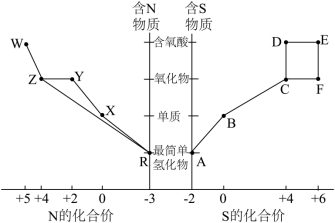
2 . I.元素的“价—类”二维图体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。
(1)写出实验室利用两种固体物质加热制备物质R的化学方程式___________ 。
(2)物质R→Y是工业制硝酸的重要反应,其化学方程式是___________ 。
(3)写出物质E的浓溶液与碳单质反应的化学方程式:___________ 。
(4)写出物质Z与水反应的离子方程式:___________ ,当反应消耗0.3mol物质Z时,转移电子数为___________ 。
(5)下列有关图中所示含N、S物质的叙述,正确的是___________(填标号)。
II.粗盐中含有泥沙及 、
、 、
、 等杂质,其提纯过程一般经过以下流程:
等杂质,其提纯过程一般经过以下流程: 溶液、
溶液、 溶液等药品以及必备的实验仪器若干。请回答下列问题:
溶液等药品以及必备的实验仪器若干。请回答下列问题:
(6)操作③按a、b、c顺序依次加入过量的试剂。若a为NaOH溶液,则c为___________ 。
(7)加盐酸调溶液pH的目的是___________ 。
(1)写出实验室利用两种固体物质加热制备物质R的化学方程式
(2)物质R→Y是工业制硝酸的重要反应,其化学方程式是
(3)写出物质E的浓溶液与碳单质反应的化学方程式:
(4)写出物质Z与水反应的离子方程式:
(5)下列有关图中所示含N、S物质的叙述,正确的是___________(填标号)。
| A.在催化剂的作用下,R可将Y、Z还原为X |
| B.图中所示的物质中,只有W、D、E属于电解质 |
| C.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生 |
| D.Z、C、F均能与NaOH溶液反应,都是酸性氧化物 |
II.粗盐中含有泥沙及
 、
、 、
、 等杂质,其提纯过程一般经过以下流程:
等杂质,其提纯过程一般经过以下流程: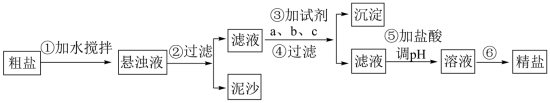
 溶液、
溶液、 溶液等药品以及必备的实验仪器若干。请回答下列问题:
溶液等药品以及必备的实验仪器若干。请回答下列问题:(6)操作③按a、b、c顺序依次加入过量的试剂。若a为NaOH溶液,则c为
(7)加盐酸调溶液pH的目的是
您最近半年使用:0次
解题方法
3 . 以次氯酸盐为有效成分的消毒剂应用广泛。电解 溶液制备
溶液制备 溶液的装置示意如下。
溶液的装置示意如下。
(1)产生
①生成 的反应包括:
的反应包括: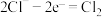 、
、 、
、___________ 。
②测所得溶液 ,试纸先变蓝
,试纸先变蓝 后褪色,说明溶液具有的性质是
后褪色,说明溶液具有的性质是___________ 。
(2)相同温度下,在不同初始 下电解
下电解 溶液,
溶液, 对
对 浓度影响如下所示。
浓度影响如下所示。 浓度在
浓度在 为3或13时较小的原因:
为3或13时较小的原因:
Ⅰ. 时,
时, 的溶解度减小
的溶解度减小
Ⅱ. 时,___________
时,___________
①根据化学平衡移动原理,推测Ⅰ合理。依据的化学平衡是___________ 。
②补全猜想Ⅱ,经过检验,推测Ⅱ成立___________ 。
根据上述实验,说明电解法制备 溶液,初始
溶液,初始 不宜过小或过大。
不宜过小或过大。
(3)用同样方法电解 溶液制备
溶液制备 ,电解难以持续,推测原因:
,电解难以持续,推测原因:___________ 。
【测量】
(4)取 所得
所得 样液,加水稀释。依次加入
样液,加水稀释。依次加入 溶液、稀
溶液、稀 。析出的
。析出的 用
用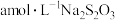 标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗
标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗 溶液
溶液 。(已知:
。(已知: )样液中
)样液中
___________  。
。
 溶液制备
溶液制备 溶液的装置示意如下。
溶液的装置示意如下。
(1)产生

①生成
 的反应包括:
的反应包括: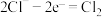 、
、 、
、②测所得溶液
 ,试纸先变蓝
,试纸先变蓝 后褪色,说明溶液具有的性质是
后褪色,说明溶液具有的性质是(2)相同温度下,在不同初始
 下电解
下电解 溶液,
溶液, 对
对 浓度影响如下所示。
浓度影响如下所示。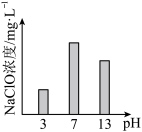
 浓度在
浓度在 为3或13时较小的原因:
为3或13时较小的原因:Ⅰ.
 时,
时, 的溶解度减小
的溶解度减小Ⅱ.
 时,___________
时,___________①根据化学平衡移动原理,推测Ⅰ合理。依据的化学平衡是
②补全猜想Ⅱ,经过检验,推测Ⅱ成立
根据上述实验,说明电解法制备
 溶液,初始
溶液,初始 不宜过小或过大。
不宜过小或过大。(3)用同样方法电解
 溶液制备
溶液制备 ,电解难以持续,推测原因:
,电解难以持续,推测原因:【测量】
(4)取
 所得
所得 样液,加水稀释。依次加入
样液,加水稀释。依次加入 溶液、稀
溶液、稀 。析出的
。析出的 用
用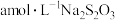 标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗
标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗 溶液
溶液 。(已知:
。(已知: )样液中
)样液中
 。
。
您最近半年使用:0次
4 . 现有下列5种与生产生活相关的物质。
①碳酸氢钠②浓硫酸③氧化铁④次氯酸钠⑤四氧化三铁
(1)常用作油漆、涂料的红色颜料的是_______ (填序号)。
(2)用作治疗胃酸的是_______ (填序号)。
(3)84消毒液的主要成分是_______ (填序号)。
(4)具有磁性的是_______ (填序号)。
(5)能作干燥剂的是_______ (填序号)。
①碳酸氢钠②浓硫酸③氧化铁④次氯酸钠⑤四氧化三铁
(1)常用作油漆、涂料的红色颜料的是
(2)用作治疗胃酸的是
(3)84消毒液的主要成分是
(4)具有磁性的是
(5)能作干燥剂的是
您最近半年使用:0次
5 . 化学与生产、生活息息相关。回答下列问题:
(1)小苏打在面包行业,不仅可以做膨松剂,还可以调节酸度。写出用小苏打调节酸度时发生反应的离子方程式:___________ 。
(2)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为___________ 。
(3)补铁剂中的铁元素化合价为___________ ,常和维生素 C 一起服用,说明维 C 具有 ___________ 性。
(4)我国“四大发明”在人类发展史上起到了非常重要的作用,其中黑火药的爆炸反应为 。该反应中被还原的元素是
。该反应中被还原的元素是___________ (填元素符号)。
(5)安全气囊弹出时发生反应: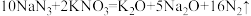 ,该反应中氧化产物与还原产物的物质的量之比为
,该反应中氧化产物与还原产物的物质的量之比为___________ 。标准状况下生成 44.8LN2时转移电子个数为 ___________ NA ( NA为阿伏加德罗常数的值)。
(1)小苏打在面包行业,不仅可以做膨松剂,还可以调节酸度。写出用小苏打调节酸度时发生反应的离子方程式:
(2)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为
(3)补铁剂中的铁元素化合价为
(4)我国“四大发明”在人类发展史上起到了非常重要的作用,其中黑火药的爆炸反应为
 。该反应中被还原的元素是
。该反应中被还原的元素是(5)安全气囊弹出时发生反应:
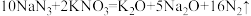 ,该反应中氧化产物与还原产物的物质的量之比为
,该反应中氧化产物与还原产物的物质的量之比为
您最近半年使用:0次
名校
解题方法
6 . 人类农业生产离不开氮肥,科学合理使用氮肥,不仅能提高化肥的使用率,而且能够更好地保护环境,请回答下列问题:
(1)某小组在实验室模拟以 为原料,制备少量硝态氮肥
为原料,制备少量硝态氮肥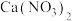 ,转化途径如下(转化所需试剂及条件已略去)。
,转化途径如下(转化所需试剂及条件已略去)。
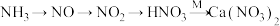
①工业合成氨是制取氮肥的基础。写出工业合成氨的化学反应方程式______ 。
②写出实验室用 和消石灰共热制备氨气的化学反应方程式
和消石灰共热制备氨气的化学反应方程式______ 。
③写出 发生催化氧化反应生成NO的化学方程式
发生催化氧化反应生成NO的化学方程式______ 。
向装置中通入4mol 和2mol
和2mol  ,转移的电子数
,转移的电子数______ 。
④工业上为了提高NO的转化率,可以适当增加 的量,理论上在一定的温度和压强下将2L NO完全转化成
的量,理论上在一定的温度和压强下将2L NO完全转化成 ,至少应该通入空气(空气中氧气体积约20%)的体积为
,至少应该通入空气(空气中氧气体积约20%)的体积为______ 。
(2)过渡施用氮肥将导致大气中 含量增高,加剧雾霾的形成。
含量增高,加剧雾霾的形成。 是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去)
是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去) 或
或______ 。
②尿素 是一种常用有机氮肥,缓慢与
是一种常用有机氮肥,缓慢与 发生非氧化还原反应释放出
发生非氧化还原反应释放出 和另外一种气体,该反应的化学方程式为
和另外一种气体,该反应的化学方程式为______ 。
(1)某小组在实验室模拟以
 为原料,制备少量硝态氮肥
为原料,制备少量硝态氮肥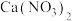 ,转化途径如下(转化所需试剂及条件已略去)。
,转化途径如下(转化所需试剂及条件已略去)。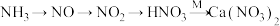
①工业合成氨是制取氮肥的基础。写出工业合成氨的化学反应方程式
②写出实验室用
 和消石灰共热制备氨气的化学反应方程式
和消石灰共热制备氨气的化学反应方程式③写出
 发生催化氧化反应生成NO的化学方程式
发生催化氧化反应生成NO的化学方程式向装置中通入4mol
 和2mol
和2mol  ,转移的电子数
,转移的电子数④工业上为了提高NO的转化率,可以适当增加
 的量,理论上在一定的温度和压强下将2L NO完全转化成
的量,理论上在一定的温度和压强下将2L NO完全转化成 ,至少应该通入空气(空气中氧气体积约20%)的体积为
,至少应该通入空气(空气中氧气体积约20%)的体积为(2)过渡施用氮肥将导致大气中
 含量增高,加剧雾霾的形成。
含量增高,加剧雾霾的形成。 是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去)
是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去)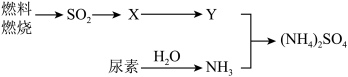
 或
或②尿素
 是一种常用有机氮肥,缓慢与
是一种常用有机氮肥,缓慢与 发生非氧化还原反应释放出
发生非氧化还原反应释放出 和另外一种气体,该反应的化学方程式为
和另外一种气体,该反应的化学方程式为
您最近半年使用:0次
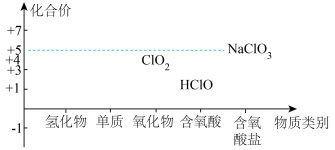
7 . 氯及其化合物的价类二维图如图,回答下列问题: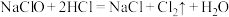 。写出反应①离子方程式
。写出反应①离子方程式___________ ;反应②中HCl体现的性质是___________ 。
(2)溶质质量分数为36.5%、密度为1.2g/cm3的浓盐酸中,盐酸的物质的量浓度为___________ mol/L,取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是___________ 。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)若用(2)中浓盐酸配制500 mL0.3mol/L稀盐酸。该学生需要用量筒量取___________ mL上述浓盐酸进行配制。完成此实验需用到的玻璃仪器除了量筒、烧杯、玻璃棒、胶头滴管外,还需要___________ 。
(4)现将200 mL0.3 mol/L盐酸与300 mL0.4 mol/LCuCl2溶液混合,溶液体积变化忽略不计,所得溶液中Cl-的物质的量浓度是___________ mol/L。
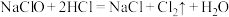 。写出反应①离子方程式
。写出反应①离子方程式(2)溶质质量分数为36.5%、密度为1.2g/cm3的浓盐酸中,盐酸的物质的量浓度为
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)若用(2)中浓盐酸配制500 mL0.3mol/L稀盐酸。该学生需要用量筒量取
(4)现将200 mL0.3 mol/L盐酸与300 mL0.4 mol/LCuCl2溶液混合,溶液体积变化忽略不计,所得溶液中Cl-的物质的量浓度是
您最近半年使用:0次
名校
解题方法
8 .  是常见的主要大气污染物质。某学习小组利用如图探究
是常见的主要大气污染物质。某学习小组利用如图探究 的部分性质,进行以下系列实验。请回答下列问题:
的部分性质,进行以下系列实验。请回答下列问题: 的是
的是___________ (填序号)。
① 浴液与稀硝酸 ②
浴液与稀硝酸 ② 固体与浓硫酸 ③固体硫在氧气中燃烧
固体与浓硫酸 ③固体硫在氧气中燃烧
浓 与铜反应也可以制取
与铜反应也可以制取 ,写出反应的化学方程式
,写出反应的化学方程式___________ 。
(2)当足量的 进入装置A中后,品红溶液将
进入装置A中后,品红溶液将___________ (填“褪色”或“不褪色”),说明 具有
具有___________ (填“氧化性”或“漂白性”)。
(3)当 进入装置B中后,
进入装置B中后, 黄色溶液变浅绿色,说明
黄色溶液变浅绿色,说明 具有
具有___________ (填“氧化性”或“还原性”)。
(4)当 不断通入装置C中,含淀粉的碘水溶液由蓝色逐渐褪为无色,反应的化学方程式表示为
不断通入装置C中,含淀粉的碘水溶液由蓝色逐渐褪为无色,反应的化学方程式表示为___________ 。
(5)当 进入装置D中后,溶液中产生白色沉淀,其化学式为
进入装置D中后,溶液中产生白色沉淀,其化学式为___________ ,反应的离子方程式表示为___________ 。
 是常见的主要大气污染物质。某学习小组利用如图探究
是常见的主要大气污染物质。某学习小组利用如图探究 的部分性质,进行以下系列实验。请回答下列问题:
的部分性质,进行以下系列实验。请回答下列问题: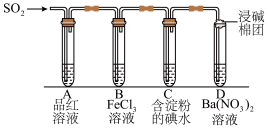
 的是
的是①
 浴液与稀硝酸 ②
浴液与稀硝酸 ② 固体与浓硫酸 ③固体硫在氧气中燃烧
固体与浓硫酸 ③固体硫在氧气中燃烧浓
 与铜反应也可以制取
与铜反应也可以制取 ,写出反应的化学方程式
,写出反应的化学方程式(2)当足量的
 进入装置A中后,品红溶液将
进入装置A中后,品红溶液将 具有
具有(3)当
 进入装置B中后,
进入装置B中后, 黄色溶液变浅绿色,说明
黄色溶液变浅绿色,说明 具有
具有(4)当
 不断通入装置C中,含淀粉的碘水溶液由蓝色逐渐褪为无色,反应的化学方程式表示为
不断通入装置C中,含淀粉的碘水溶液由蓝色逐渐褪为无色,反应的化学方程式表示为(5)当
 进入装置D中后,溶液中产生白色沉淀,其化学式为
进入装置D中后,溶液中产生白色沉淀,其化学式为
您最近半年使用:0次
9 . 按要求回答下列问题:
(1)写出漂白粉中有效成分的化学式___________ 。
(2)写出中子数为8的碳原子符号___________ 。
(3)镁离子的结构示意图___________ 。
(4)工业上用覆铜板制作印刷电路板,对应的离子方程式为___________ 。
(5)写出实验室制取氧气反应的化学方程式___________ 。
(1)写出漂白粉中有效成分的化学式
(2)写出中子数为8的碳原子符号
(3)镁离子的结构示意图
(4)工业上用覆铜板制作印刷电路板,对应的离子方程式为
(5)写出实验室制取氧气反应的化学方程式
您最近半年使用:0次
名校
10 . 如图是无机物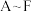 在一定条件下的转化关系(部分产物及反应条件未标出)。
在一定条件下的转化关系(部分产物及反应条件未标出)。
已知: 为气体,
为气体,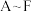 都含有相同的元素。
都含有相同的元素。
(1)写出下列物质的化学式:C______ 、F______ 。
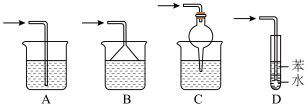
(2)写出实验室制物质B的化学反应方程式:______ ,干燥B可用的干燥剂为______ (填试剂名称),尾气吸收可选用______ 装置(填序号)。 和
和 的混合气体充满容积为
的混合气体充满容积为 的试管后倒扣在水中。
的试管后倒扣在水中。
①假设气体不扩散,最终试管中所得溶液的物质的量浓度为______  。
。
②为了消除 的污染,可将它与
的污染,可将它与 在催化剂作用下反应,生成水和一种无污染物质,该反应的化学方程式是
在催化剂作用下反应,生成水和一种无污染物质,该反应的化学方程式是______ 。
③描述检验 中阳离子的操作:
中阳离子的操作:______ 。
(4)工业上可用①②③由B制取E,为了提高原料的利用率并尽量减轻对环境的污染,C必须循环使用.若消耗 的
的 制取
制取 ,在该过程中至少消耗的
,在该过程中至少消耗的 的物质的量为
的物质的量为______ 。
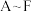 在一定条件下的转化关系(部分产物及反应条件未标出)。
在一定条件下的转化关系(部分产物及反应条件未标出)。已知:
 为气体,
为气体,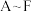 都含有相同的元素。
都含有相同的元素。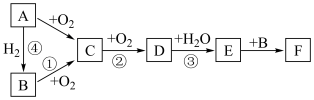
(1)写出下列物质的化学式:C
(2)写出实验室制物质B的化学反应方程式:
 和
和 的混合气体充满容积为
的混合气体充满容积为 的试管后倒扣在水中。
的试管后倒扣在水中。①假设气体不扩散,最终试管中所得溶液的物质的量浓度为
 。
。②为了消除
 的污染,可将它与
的污染,可将它与 在催化剂作用下反应,生成水和一种无污染物质,该反应的化学方程式是
在催化剂作用下反应,生成水和一种无污染物质,该反应的化学方程式是③描述检验
 中阳离子的操作:
中阳离子的操作:(4)工业上可用①②③由B制取E,为了提高原料的利用率并尽量减轻对环境的污染,C必须循环使用.若消耗
 的
的 制取
制取 ,在该过程中至少消耗的
,在该过程中至少消耗的 的物质的量为
的物质的量为
您最近半年使用:0次



