1 . 过二硫酸钾( )是工业上一种重要的消毒剂和织物漂白剂,可通过电解
)是工业上一种重要的消毒剂和织物漂白剂,可通过电解 溶液制备。它在
溶液制备。它在 下能发生分解反应:
下能发生分解反应: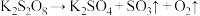 (未配平),设
(未配平),设 是阿伏加德罗常数的值。下列说法错误的是
是阿伏加德罗常数的值。下列说法错误的是
 )是工业上一种重要的消毒剂和织物漂白剂,可通过电解
)是工业上一种重要的消毒剂和织物漂白剂,可通过电解 溶液制备。它在
溶液制备。它在 下能发生分解反应:
下能发生分解反应: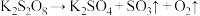 (未配平),设
(未配平),设 是阿伏加德罗常数的值。下列说法错误的是
是阿伏加德罗常数的值。下列说法错误的是A.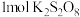 中存在 中存在 个非极性共价键 个非极性共价键 |
B.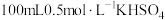 溶液的离子总数为 溶液的离子总数为 |
C.标准状况下,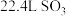 含有的原子数大于 含有的原子数大于 |
D.上述反应,每生成 ,转移 ,转移 个电子 个电子 |
您最近一年使用:0次
2024-02-27更新
|
532次组卷
|
3卷引用:2024届吉林省延边州高三教学质量检测(一模)化学试题
名校
解题方法
2 . 为探究“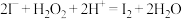 ”碘离子氧化过程进行如下实验.
”碘离子氧化过程进行如下实验.
下列说法不正确的是
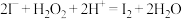 ”碘离子氧化过程进行如下实验.
”碘离子氧化过程进行如下实验.编号 | 1 | 2 |
实验内容 |
|
|
实验现象 | 随着液体不断滴入,产生大量气体;溶液变黄并不断加深至棕黄色后又变浅 | 随着液体不断滴入,溶液变黄,摇匀后又褪色,不断重复直至析出紫色沉淀 |
A.实验1中溶液变浅是因为 |
B.实验2中出现紫色沉淀是因为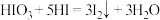 |
C.实验1中产生大量气体的原因是 被氧化的过程大量放热 被氧化的过程大量放热 |
| D.实验2相较于实验1,可节约H2O2用量且有利于反应终点观察 |
您最近一年使用:0次
2023-03-08更新
|
800次组卷
|
3卷引用:2024届吉林省延边州高三教学质量检测(一模)化学试题
名校
解题方法
3 . 向含废水中加入 ,铁元素会形成如图所示的
,铁元素会形成如图所示的 胶团,在静电吸附作用下,胶团可以除去废水中的
胶团,在静电吸附作用下,胶团可以除去废水中的 价砷元素,下列说法正确的是
价砷元素,下列说法正确的是

 ,铁元素会形成如图所示的
,铁元素会形成如图所示的 胶团,在静电吸附作用下,胶团可以除去废水中的
胶团,在静电吸附作用下,胶团可以除去废水中的 价砷元素,下列说法正确的是
价砷元素,下列说法正确的是
| A.废水中的含砷微粒是带正电荷的离子 |
B. 可以形成的胶团数目小于 可以形成的胶团数目小于 |
C.增大废水的 , , 胶粒的吸附絮凝效能提升 胶粒的吸附絮凝效能提升 |
D. 可以还原废水中的含砷微粒到 可以还原废水中的含砷微粒到 价 价 |
您最近一年使用:0次
2022-12-09更新
|
1232次组卷
|
5卷引用:吉林省延边第一中学2023届高三下学期第七次模拟考试理科综合化学试题
4 . 下列过程中的化学反应对应的离子方程式正确的是
| A.用KSCN试剂检验Fe3+:Fe3++3SCN-=Fe(SCN)3↓ |
B.向Na2S2O3溶液中加入足量稀硫酸:2S2O +4H+=SO +4H+=SO +3S↓+2H2O +3S↓+2H2O |
C.向Na2CO3溶液中通入过量SO2:CO +2SO2+H2O=CO2+2HSO +2SO2+H2O=CO2+2HSO |
| D.将洗净的鸡蛋壳浸泡在米醋中获得溶解液:2H++CaCO3=Ca2++H2O+CO2↑ |
您最近一年使用:0次
名校
5 . 一种矿石[Y3Z2X5(XW)4]的组成元素W、X、Y、Z为原子序数依次增大的短周期元素,其中W、X、Z分别位于不同周期,Z核外最外层电子数是X核外电子数的一半,1个W2X分子含有10个电子。下列说法正确的是
| A.原子半径:Y>Z>X>W | B.Y与X形成的化合物可与NaOH溶液反应 |
| C.简单氢化物的沸点:Z>X | D.Z的最高价氧化物不能与酸、碱反应 |
您最近一年使用:0次
2022-04-16更新
|
1246次组卷
|
6卷引用:吉林省延边州2022届高三教学质量检测(一模)理科综合化学试题
吉林省延边州2022届高三教学质量检测(一模)理科综合化学试题(已下线)化学-2022年高考押题预测卷03(广东卷)(已下线)专题06物质结构元素周期律-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题06物质结构元素周期律-2022年高考真题+模拟题汇编(全国卷)(已下线)专题06物质结构元素周期律-三年(2020~2022)高考真题汇编(全国卷)宁夏石嘴山市第三中学2022届高三下学期第四次模拟理科综合化学试题
6 . 硫酸盐(含SO 、HSO
、HSO )气溶胶是PM2.5的成分之一。近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如下。下列说法不正确的是( )
)气溶胶是PM2.5的成分之一。近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如下。下列说法不正确的是( )

 、HSO
、HSO )气溶胶是PM2.5的成分之一。近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如下。下列说法不正确的是( )
)气溶胶是PM2.5的成分之一。近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如下。下列说法不正确的是( )
| A.该过程中有H2O参与反应 | B.硫酸盐气溶胶呈酸性 |
| C.NO2是生成硫酸盐的催化剂 | D.该过程中有氧氢键断裂 |
您最近一年使用:0次
解题方法
7 . 科学家利用四种原子序数依次递增的短周期元素W、X、Y、Z“组合”成一种超分子,具有高效的催化性能,其结构示意图如下(实线代表共价键,其他重复单元的W、X未标注),W、X、Z分别位于不同周期,Z的原子半径在同周期中最大。下列说法不正确的是


| A.Y单质的氧化性在同周期元素形成的单质中最强 |
| B.Z与Y可能组成多种离子化合物 |
| C.ZW与水反应生成W2的反应中,ZW为还原剂 |
| D.Y的最简单氢化物热稳定性大于X |
您最近一年使用:0次
名校
8 . 我国的科技发展改变着人们的生活、生产方式。下列说法正确的是
| A.闻名世界的秦兵马俑是陶制品,由石灰石经高温烧结而成 |
| B.“嫦娥四号”使用的SiC—Al材料属于复合材料 |
| C.5G芯片“巴龙5000”的主要材料是SiO2 |
| D.港珠澳大桥采用超高分子量聚乙烯纤维吊绳,其商品名为“力纶”,是有机高分子化合物,属于纯净物 |
您最近一年使用:0次
2020-06-12更新
|
246次组卷
|
2卷引用:吉林省延边州2020届高三4月教学质量检测理科综合化学试题
名校
9 . 已知NA是阿伏加 德罗常数的值,下列说法正确的是
| A.常温常压下,1mol甲基(-14CD3)所含的中子数和电子数分别为11NA、9NA |
B.CH4和P4都是正四面体结构,物质的量相同的CH4和P4的共价键数之比为 |
| C.标准状态下,1molH2和1molF2混合后,所含气体的体积为44.8L |
| D.常温常压下,0.5molFe和足量浓硝酸混合,转移电子数为1.5NA |
您最近一年使用:0次
2020-06-12更新
|
209次组卷
|
2卷引用:吉林省延边州2020届高三4月教学质量检测理科综合化学试题
10 . 草酸亚铁晶体(FeC2O4·2H2O,M=180g/mol)呈淡黄色,可用于晒制蓝图。某实验小组对其进行了一系列探究。
Ⅰ.纯净草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究。小组成员采用如图装置进行实验:
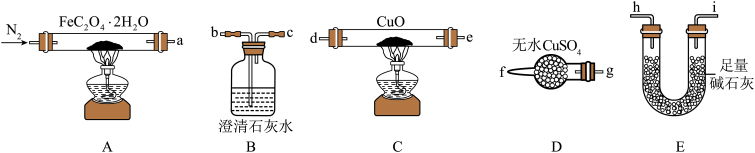
①按照气流从左到右的方向,上述装置的接口顺序为a→g→f→___ →尾气处理装置(仪器可重复使用)。
②检查装置气密性后,先通入一段时间N2,其目的为__ 。
③实验证明了气体产物中含有CO,依据的实验现象为__ 。
④结束实验时先熄灭A、C处的酒精灯再停止通入N2,其目的是__ 。
(2)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为__ 。
(3)晒制蓝图时,草酸亚铁晶体是感光剂,会失去结晶水转化为FeC2O4,现以K3[Fe(CN)6]溶液为显色剂,该显色反应的化学方程式为__ 。
Ⅱ.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用cmol·L-1KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用cmol·L-1KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤2中滴定终点的现象为__ ;步骤3中加入锌粉的目的为___ 。
(5)若步骤 配制溶液时部分Fe2+被氧化变质,则测定结果将
配制溶液时部分Fe2+被氧化变质,则测定结果将__ (填“偏高”、“偏低”或“不变”)
Ⅰ.纯净草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究。小组成员采用如图装置进行实验:

①按照气流从左到右的方向,上述装置的接口顺序为a→g→f→
②检查装置气密性后,先通入一段时间N2,其目的为
③实验证明了气体产物中含有CO,依据的实验现象为
④结束实验时先熄灭A、C处的酒精灯再停止通入N2,其目的是
(2)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为
(3)晒制蓝图时,草酸亚铁晶体是感光剂,会失去结晶水转化为FeC2O4,现以K3[Fe(CN)6]溶液为显色剂,该显色反应的化学方程式为
Ⅱ.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用cmol·L-1KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用cmol·L-1KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤2中滴定终点的现象为
(5)若步骤
 配制溶液时部分Fe2+被氧化变质,则测定结果将
配制溶液时部分Fe2+被氧化变质,则测定结果将
您最近一年使用:0次
2020-06-12更新
|
1222次组卷
|
3卷引用:吉林省延边州2020届高三4月教学质量检测理科综合化学试题





