名校
解题方法
1 . 某无色透明溶液中可能含有下列离子中的若干种: 。为了确定该溶液的组成,某同学取上述溶液进行如下实验:
。为了确定该溶液的组成,某同学取上述溶液进行如下实验:
①向溶液中加入足量的稀盐酸,得到能使澄清石灰水变浑浊的气体;
②向①所得溶液加入足量 溶液,得到白色沉淀;
溶液,得到白色沉淀;
③向②中加入足量稀盐酸,沉淀部分溶解。
下列说法正确的是
 。为了确定该溶液的组成,某同学取上述溶液进行如下实验:
。为了确定该溶液的组成,某同学取上述溶液进行如下实验:①向溶液中加入足量的稀盐酸,得到能使澄清石灰水变浑浊的气体;
②向①所得溶液加入足量
 溶液,得到白色沉淀;
溶液,得到白色沉淀;③向②中加入足量稀盐酸,沉淀部分溶解。
下列说法正确的是
A.溶液中一定不存在 和 和 |
B.溶液中一定存在 ,可能存在 ,可能存在 |
C.②中得到的白色沉淀是 和 和 的混合物 的混合物 |
D.取③的上层清液,加入适量 溶液,若有白色沉淀生成,则原溶液中存在 溶液,若有白色沉淀生成,则原溶液中存在 |
您最近一年使用:0次
2024-01-22更新
|
199次组卷
|
2卷引用:辽宁省丹东市2023-2024学年高一上学期期末质量检测化学试题
2 . 下列电离方程式书写不正确 的是
A.HNO3=H++ | B.Ba(OH)2=Ba2++2OH- |
C.NaHCO3=Na++H++ | D.NH4NO3= + + |
您最近一年使用:0次
2024-01-02更新
|
104次组卷
|
3卷引用:北京市第三中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
3 . 聚合硫酸铁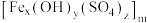 (铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
(铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
①称取一定质量的聚合硫酸铁,配成 溶液。
溶液。
②准确量取①中溶液 于烧杯中,加入足量的盐酸酸化的
于烧杯中,加入足量的盐酸酸化的 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体 。
。
③准确量取①中溶液 于烧杯中,加入足量的
于烧杯中,加入足量的 溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体
溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体 。
。
该聚合硫酸铁组成中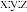 为
为
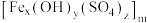 (铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
(铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:①称取一定质量的聚合硫酸铁,配成
 溶液。
溶液。②准确量取①中溶液
 于烧杯中,加入足量的盐酸酸化的
于烧杯中,加入足量的盐酸酸化的 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体 。
。③准确量取①中溶液
 于烧杯中,加入足量的
于烧杯中,加入足量的 溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体
溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体 。
。该聚合硫酸铁组成中
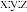 为
为A. | B. | C.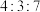 | D. |
您最近一年使用:0次
2023-12-30更新
|
178次组卷
|
3卷引用:河南省新未来2023-2024学年高一上学期12月质量检测化学试题
名校
解题方法
4 . 下列选项描述与对应图像相符的是
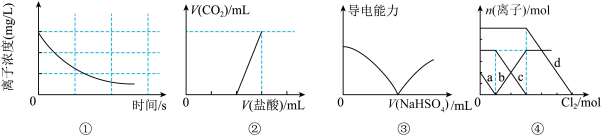

A.图①为新制氯水在阳光直射时,溶液中 浓度随着时间变化的曲线 浓度随着时间变化的曲线 |
B.图②为往 与 与 的物质的量之比为 的物质的量之比为 的混合液中滴加盐酸的体积与产生 的混合液中滴加盐酸的体积与产生 体积变化的图像 体积变化的图像 |
C.图③为往 溶液中滴加 溶液中滴加 溶液的体积与导电性变化的图像 溶液的体积与导电性变化的图像 |
D.图④为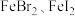 混合液中部分离子的物质的量随氯气通入的变化图像,其中a代表的是 混合液中部分离子的物质的量随氯气通入的变化图像,其中a代表的是 |
您最近一年使用:0次
2023-12-27更新
|
541次组卷
|
3卷引用:广东省汕头市金山中学2023-2024学年高一上学期期末考试 化学试题
5 . 电解质在人体内的作用是十分重要的,当电解质紊乱时人体就会出现一系列不适症状,甚至危及生命。 固体④漂白粉粉末 ⑤熔融的
固体④漂白粉粉末 ⑤熔融的 ⑥
⑥ 溶液
溶液
(1)上述物质中,属于电解质的是___________ (填序号,下同),能导电的是___________ 。
(2)16.8g由 和
和 组成的混合物与200g质量分数为7.3%的盐酸恰好反应,蒸干反应后的溶液,最终得到的固体质量为___________(填字母序号)。
组成的混合物与200g质量分数为7.3%的盐酸恰好反应,蒸干反应后的溶液,最终得到的固体质量为___________(填字母序号)。
(3)将①投入⑥的溶液中产生气泡,写出离子方程式___________ 。
Ⅱ.完成下列问题
(4)配制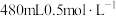 的
的 溶液。
溶液。
①配制时,用托盘天平称取 固体的质量为
固体的质量为___________ g
②其操作步骤如下图所示:___________ (填序号)操作之间。___________ (填字母序号)。
a.定容时俯视刻度线
b.溶解时,烧杯中有少量蒸馏水
c.加水时不慎超过了刻度线,立即用胶头滴管吸出
(5)从配制好的 溶液中取出10mL,加蒸馏水将其稀释至100mL,稀释后溶液中
溶液中取出10mL,加蒸馏水将其稀释至100mL,稀释后溶液中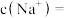
___________  。
。
 固体④漂白粉粉末 ⑤熔融的
固体④漂白粉粉末 ⑤熔融的 ⑥
⑥ 溶液
溶液(1)上述物质中,属于电解质的是
(2)16.8g由
 和
和 组成的混合物与200g质量分数为7.3%的盐酸恰好反应,蒸干反应后的溶液,最终得到的固体质量为___________(填字母序号)。
组成的混合物与200g质量分数为7.3%的盐酸恰好反应,蒸干反应后的溶液,最终得到的固体质量为___________(填字母序号)。| A.8g | B.15.5g | C.11.7g | D.23.4g |
(3)将①投入⑥的溶液中产生气泡,写出离子方程式
Ⅱ.完成下列问题
(4)配制
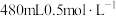 的
的 溶液。
溶液。①配制时,用托盘天平称取
 固体的质量为
固体的质量为②其操作步骤如下图所示:
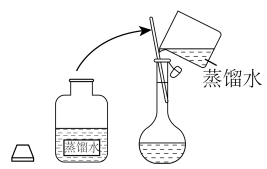
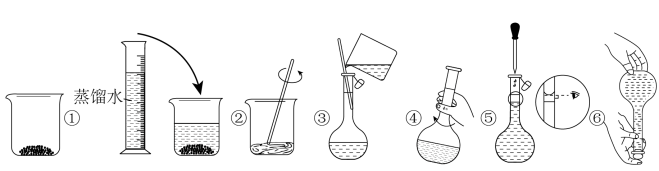
a.定容时俯视刻度线
b.溶解时,烧杯中有少量蒸馏水
c.加水时不慎超过了刻度线,立即用胶头滴管吸出
(5)从配制好的
 溶液中取出10mL,加蒸馏水将其稀释至100mL,稀释后溶液中
溶液中取出10mL,加蒸馏水将其稀释至100mL,稀释后溶液中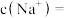
 。
。
您最近一年使用:0次
2023-12-24更新
|
76次组卷
|
2卷引用:江苏省“江南十校”2023-2024学年高一上学期分科诊断摸底联考化学试卷
解题方法
6 . 一种带有多孔结构的镍铝合金对 有较强的吸附性,其高催化活性和热稳定性使该镍铝合金被广泛用于工业生产和有机合成反应中。以镍黄铁矿(主要成分为NiS、FeS等)为原料制备该镍铝合金的工艺流程如图所示。
有较强的吸附性,其高催化活性和热稳定性使该镍铝合金被广泛用于工业生产和有机合成反应中。以镍黄铁矿(主要成分为NiS、FeS等)为原料制备该镍铝合金的工艺流程如图所示。

回答下列有关问题:
(1)在空气中“煅烧”镍黄铁矿生成 、
、 和一种有刺激性气味的气体,该气体为
和一种有刺激性气味的气体,该气体为______ (填化学式)。
(2)已知 中C的化合价为+2,则Ni的化合价为
中C的化合价为+2,则Ni的化合价为______ ,“ ”中发生的反应类型为
”中发生的反应类型为____________ 。
(3)Ni、Al高温熔融时,通入Ar的主要作用是____________ 。高温熔融物冷却后,需要进行粉碎处理,粉碎的目的是____________ 。
(4)为增强镍铝合金对 的吸附性,“碱浸”需溶解部分铝的主要目的是
的吸附性,“碱浸”需溶解部分铝的主要目的是____________ ,主要反应的离子方程式为____________ 。
(5)“浸出液”中的铝元素可循环利用,回收铝元素并制备铝的流程为:

已知 的熔点高达
的熔点高达 。无色无味气体X的化学式是
。无色无味气体X的化学式是____________ ,加入冰晶石的作用是____________ 。
 有较强的吸附性,其高催化活性和热稳定性使该镍铝合金被广泛用于工业生产和有机合成反应中。以镍黄铁矿(主要成分为NiS、FeS等)为原料制备该镍铝合金的工艺流程如图所示。
有较强的吸附性,其高催化活性和热稳定性使该镍铝合金被广泛用于工业生产和有机合成反应中。以镍黄铁矿(主要成分为NiS、FeS等)为原料制备该镍铝合金的工艺流程如图所示。
回答下列有关问题:
(1)在空气中“煅烧”镍黄铁矿生成
 、
、 和一种有刺激性气味的气体,该气体为
和一种有刺激性气味的气体,该气体为(2)已知
 中C的化合价为+2,则Ni的化合价为
中C的化合价为+2,则Ni的化合价为 ”中发生的反应类型为
”中发生的反应类型为(3)Ni、Al高温熔融时,通入Ar的主要作用是
(4)为增强镍铝合金对
 的吸附性,“碱浸”需溶解部分铝的主要目的是
的吸附性,“碱浸”需溶解部分铝的主要目的是(5)“浸出液”中的铝元素可循环利用,回收铝元素并制备铝的流程为:

已知
 的熔点高达
的熔点高达 。无色无味气体X的化学式是
。无色无味气体X的化学式是
您最近一年使用:0次
2023-03-06更新
|
316次组卷
|
2卷引用:广西南宁市2022-2023学年高一下学期开学联考化学试题
名校
解题方法
7 . 铁是人类较早使用的金属之一,FeSO4和FeCl3是重要的化工原料。
(I)硫酸亚铁晶体(FeSO4·7H2O)在医药上可作补血剂。
(1)为防止FeSO4溶液变质,应在溶液中加入少量_______ (填标号,下同);向FeSO4溶液加入_______ 可验证该溶液是否变质。
A.铜片 B.KSCN溶液 C.氯气 D.铁粉
(2)该补血剂与维生素C同时服用,有利于Fe2+的吸收。某同学设计如下实验探究维生素C的作用:取少量Fe2(SO4)3溶液于试管中,加入维生素C片2片,振荡溶解,再滴加铁氰化钾溶液,溶液出现蓝色沉淀,由此得出结论是_______ 。(已知:Fe2+遇铁氰化钾溶液产生蓝色沉淀)
(II)氯化铁溶液可用于腐蚀印刷电路板上的铜,某腐蚀后的废液中含有FeCl3、FeCl2和CuCl2,且c(Fe3+)=c(Fe2+)。
(3)从废液中可回收铜,并获得FeCl3溶液,设计如下方案:
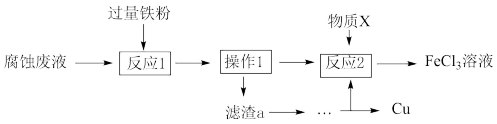
①滤渣a为_______ 。
②物质X为_______ 。
A.HCl B.酸性KMnO4溶液 C.Cl2
(4)取该废液20mL并加入mg铁粉,充分反应。
①对反应后的溶液分析错误的是_______
A.溶液中一定含有Fe2+
B.若有固体剩余,则固体中一定含有铁
C.若溶液中有Cu2+,则可能有固体析出
D.溶液若有Fe3+剩余,则一定没有固体析出
②若m=2.72,则充分反应后得到20mL3.0mol/L氯化亚铁溶液和2.24g固体混合物。则原废液中Fe3+的物质的量浓度为_______ 。
(I)硫酸亚铁晶体(FeSO4·7H2O)在医药上可作补血剂。
(1)为防止FeSO4溶液变质,应在溶液中加入少量
A.铜片 B.KSCN溶液 C.氯气 D.铁粉
(2)该补血剂与维生素C同时服用,有利于Fe2+的吸收。某同学设计如下实验探究维生素C的作用:取少量Fe2(SO4)3溶液于试管中,加入维生素C片2片,振荡溶解,再滴加铁氰化钾溶液,溶液出现蓝色沉淀,由此得出结论是
(II)氯化铁溶液可用于腐蚀印刷电路板上的铜,某腐蚀后的废液中含有FeCl3、FeCl2和CuCl2,且c(Fe3+)=c(Fe2+)。
(3)从废液中可回收铜,并获得FeCl3溶液,设计如下方案:

①滤渣a为
②物质X为
A.HCl B.酸性KMnO4溶液 C.Cl2
(4)取该废液20mL并加入mg铁粉,充分反应。
①对反应后的溶液分析错误的是
A.溶液中一定含有Fe2+
B.若有固体剩余,则固体中一定含有铁
C.若溶液中有Cu2+,则可能有固体析出
D.溶液若有Fe3+剩余,则一定没有固体析出
②若m=2.72,则充分反应后得到20mL3.0mol/L氯化亚铁溶液和2.24g固体混合物。则原废液中Fe3+的物质的量浓度为
您最近一年使用:0次
2023-02-14更新
|
299次组卷
|
3卷引用:山东省聊城市2022-2023学年高一上学期期末教学质量抽测化学试题
名校
解题方法
8 . 将一定量的 、
、 组成的混合物溶于水,配成1L溶液,取出
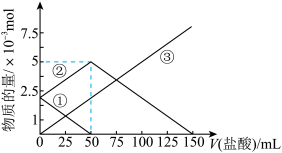
组成的混合物溶于水,配成1L溶液,取出 ,向其中逐滴加入一定物质的量浓度的盐酸,部分物质的物质的量与加入盐酸的体积的关系如图所示,下列说法中正确的是
,向其中逐滴加入一定物质的量浓度的盐酸,部分物质的物质的量与加入盐酸的体积的关系如图所示,下列说法中正确的是
 、
、 组成的混合物溶于水,配成1L溶液,取出
组成的混合物溶于水,配成1L溶液,取出 ,向其中逐滴加入一定物质的量浓度的盐酸,部分物质的物质的量与加入盐酸的体积的关系如图所示,下列说法中正确的是
,向其中逐滴加入一定物质的量浓度的盐酸,部分物质的物质的量与加入盐酸的体积的关系如图所示,下列说法中正确的是
A.直线③代表产生的 的物质的量 的物质的量 |
B.原混合物中 的质量为 的质量为 |
C.滴加的盐酸浓度为 |
D.当收集到标准状况下 气体 气体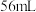 时消耗的盐酸为 时消耗的盐酸为 |
您最近一年使用:0次
2023-02-12更新
|
400次组卷
|
3卷引用:山东省德州市2022-2023学年高一上学期期末考试化学试题
名校
解题方法
9 . 铁及其化合物与生产、生活息息相关。回答下列问题:
(1) 易被人体吸收,医生建议在服用该补铁剂时,同时服用维生素C.维生素C的作用是
易被人体吸收,医生建议在服用该补铁剂时,同时服用维生素C.维生素C的作用是_______ 。
(2)印刷电路板的制作原理是用足量的 溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的化学方程式:
溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的化学方程式:_______ 。
(3)生铁是通过高炉冶炼而得到的,以赤铁矿为例用 将其还原的化学方程式为
将其还原的化学方程式为_______ 。
(4)某废料铁泥的主要成分为 、
、 、
、 和杂质(杂质不与硫酸反应)。现取
和杂质(杂质不与硫酸反应)。现取 废料铁泥提取
废料铁泥提取 ,设计实验流程如下:
,设计实验流程如下:

①分离溶液A和沉淀C的操作中使用到的玻璃仪器有烧杯、_______ 、_______ 。
②能检验溶液A中含有 的试剂是
的试剂是_______ (填字母)。
A.铁粉 B.酸性 溶液 C.KSCN溶液
溶液 C.KSCN溶液
③步骤Ⅱ中发生反应的离子方程式为_______ 。
④若最终获得 ,则废料铁泥中铁元素的质量分数为
,则废料铁泥中铁元素的质量分数为_______ 。
(1)
 易被人体吸收,医生建议在服用该补铁剂时,同时服用维生素C.维生素C的作用是
易被人体吸收,医生建议在服用该补铁剂时,同时服用维生素C.维生素C的作用是(2)印刷电路板的制作原理是用足量的
 溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的化学方程式:
溶液腐蚀覆铜板上不需要的铜箔。写出上述反应的化学方程式:(3)生铁是通过高炉冶炼而得到的,以赤铁矿为例用
 将其还原的化学方程式为
将其还原的化学方程式为(4)某废料铁泥的主要成分为
 、
、 、
、 和杂质(杂质不与硫酸反应)。现取
和杂质(杂质不与硫酸反应)。现取 废料铁泥提取
废料铁泥提取 ,设计实验流程如下:
,设计实验流程如下:
①分离溶液A和沉淀C的操作中使用到的玻璃仪器有烧杯、
②能检验溶液A中含有
 的试剂是
的试剂是A.铁粉 B.酸性
 溶液 C.KSCN溶液
溶液 C.KSCN溶液③步骤Ⅱ中发生反应的离子方程式为
④若最终获得
 ,则废料铁泥中铁元素的质量分数为
,则废料铁泥中铁元素的质量分数为
您最近一年使用:0次
2023-01-20更新
|
519次组卷
|
7卷引用:河南省叶县高级中学2022-2023学年高一上学期1月期末考试化学试题
名校
10 . 钠和氯的化合物常用于化工生产与生活中。
(1)将一小块钠放在水平放置的试管中部,用酒精灯加热至充分反应,化学方程式为_______ 。将试管冷却后加水,发生反应的离子方程式为_______ 。
(2)实验室欲用NaOH固体配制1.0mol/L的NaOH溶液480mL。
①完成本实验需要用托盘天平称量NaOH_______ g。
②在配制过程中,若其他操作都正确,下列操作会使浓度偏高的是_______ (填序号)。
A.定容时仰视刻度线 B.未冷就转移溶液
C.未洗涤烧杯和玻璃棒 D.NaOH已部分变质
(3) 将逐渐用来取代
将逐渐用来取代 成为自来水的消毒剂。已知
成为自来水的消毒剂。已知 是一种易溶于水难溶于有机物的气体,
是一种易溶于水难溶于有机物的气体, 等卤素单质在水中溶解度远小于在有机溶剂
等卤素单质在水中溶解度远小于在有机溶剂 中的溶解度。制备
中的溶解度。制备 的原理为
的原理为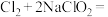
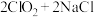 。实验装置如下图:
。实验装置如下图:

①装置A中发生反应的化学方程式为_______ 。
②E中加入的试剂可以是_______ (任意填一种)
③F用于收集 ,可选用
,可选用_______ (气流均左进右出)

④ 在消毒过程中被还原为
在消毒过程中被还原为 。
。 消毒效率是
消毒效率是 的
的_______ 倍。(消毒效率:单位质量消毒剂得到电子数,答案保留到小数点后一位。)
(1)将一小块钠放在水平放置的试管中部,用酒精灯加热至充分反应,化学方程式为
(2)实验室欲用NaOH固体配制1.0mol/L的NaOH溶液480mL。
①完成本实验需要用托盘天平称量NaOH
②在配制过程中,若其他操作都正确,下列操作会使浓度偏高的是
A.定容时仰视刻度线 B.未冷就转移溶液
C.未洗涤烧杯和玻璃棒 D.NaOH已部分变质
(3)
 将逐渐用来取代
将逐渐用来取代 成为自来水的消毒剂。已知
成为自来水的消毒剂。已知 是一种易溶于水难溶于有机物的气体,
是一种易溶于水难溶于有机物的气体, 等卤素单质在水中溶解度远小于在有机溶剂
等卤素单质在水中溶解度远小于在有机溶剂 中的溶解度。制备
中的溶解度。制备 的原理为
的原理为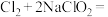
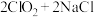 。实验装置如下图:
。实验装置如下图:
①装置A中发生反应的化学方程式为
②E中加入的试剂可以是
③F用于收集
 ,可选用
,可选用
④
 在消毒过程中被还原为
在消毒过程中被还原为 。
。 消毒效率是
消毒效率是 的
的
您最近一年使用:0次
2023-01-13更新
|
235次组卷
|
3卷引用:重庆市育才中学校2022-2023学年高一上学期期末考试化学试题



