1 . 表中是元素周期表的一部分,按要求完成各小题。
(1)化学性质最不活泼的元素____ (填编号,下同),非金属性最强的元素是____ 。金属性最强的单质____ 。
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强的____ (化学式)。①③⑤三种元素的原子半径由大到小的顺序为____ 。
(3)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素的最高价氧化物和盐酸反应的化学方程式为____ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ⑥ | ⑦ | ⑾ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强的
(3)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素的最高价氧化物和盐酸反应的化学方程式为
您最近一年使用:0次
解题方法
2 . 锆产品的主要原料是锆英砂,全球90%的氧氯化锆(ZrOCl2)来源于中国。氧氯化锆可溶于水,微溶于盐酸,工业上以锆英砂(含91.5%ZrSiO4,杂质不与NaOH溶液反应)为原料生产ZrOCl2的一种工艺流程如图所示。
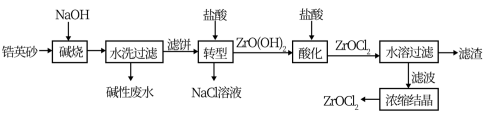
已知:碱金属的锆酸盐在水中溶解度很小,可在酸性条件下水解。
请回答下列问题:
(1)锆英砂在“碱烧”前粉碎的目的是____ ,“碱烧”时ZrSiO4生成了Na2ZrO3和另一种钠盐X,X的化学式为___ ,X的用途是___ (写一种)。
(2)“转型”时发生反应的化学方程式为___ 。
(3)“酸化”过程需加入过量盐酸,该操作中发生反应的化学方程式是___ 。
(4)“水溶过滤”操作后要对滤渣进行洗涤,洗涤液与滤液合并浓缩结晶,检查滤渣已经洗涤干净的实验是___ 。
(5)将锆英砂和焦炭混合,再与Cl2反应生成ZrCl4、SiCl4和一种可燃性气体,ZrCl4水解也可得到ZrOCl2。生成 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为___ 。
(6)某工厂用2t锆英砂来制备ZrOCl2,若这个过程中Zr的损耗率为15%,则最终制得ZrOCl2的质量为___ t。

已知:碱金属的锆酸盐在水中溶解度很小,可在酸性条件下水解。
请回答下列问题:
(1)锆英砂在“碱烧”前粉碎的目的是
(2)“转型”时发生反应的化学方程式为
(3)“酸化”过程需加入过量盐酸,该操作中发生反应的化学方程式是
(4)“水溶过滤”操作后要对滤渣进行洗涤,洗涤液与滤液合并浓缩结晶,检查滤渣已经洗涤干净的实验是
(5)将锆英砂和焦炭混合,再与Cl2反应生成ZrCl4、SiCl4和一种可燃性气体,ZrCl4水解也可得到ZrOCl2。生成
 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为(6)某工厂用2t锆英砂来制备ZrOCl2,若这个过程中Zr的损耗率为15%,则最终制得ZrOCl2的质量为
您最近一年使用:0次
2021-10-01更新
|
516次组卷
|
5卷引用:贵州省黔西南州2021~2022学年高二上学期期中考试化学试题
贵州省黔西南州2021~2022学年高二上学期期中考试化学试题河南省偃师市第一高级中学2022届高三阶段性测试化学试题福建省南平市2022届高三10月联考化学试卷重庆市2021-2022学年高二上学期期中考试化学试题(已下线)专题11 无机工艺流程题—2022年高考化学二轮复习讲练测(全国版)-测试
名校
3 . 周期表中前20号几种元素,其相关信息如下(铍的原子半径为0.089nm);F原子中无中子,G在地壳中含量居第二位,H元素焰色反应呈紫色。根据题意请回答下列问题:
(1)B的原子结构示意图为___________ 。
(2)F2C和F2E两种化合物中,沸点较高的是____ (填化学式)。
(3)用电子式表示化合物H2E的形成过程_______________________________ 。
(4)某同学设计了以G同族的短周期元素的最低价氢化物为燃料的电池,电解质为KOH。 则该电池的负极的电极反应式为__________________________________ 。
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.075 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +5,—3 | +3 | +6,—2 | —1 | —2 |
(2)F2C和F2E两种化合物中,沸点较高的是
(3)用电子式表示化合物H2E的形成过程
(4)某同学设计了以G同族的短周期元素的最低价氢化物为燃料的电池,电解质为KOH。 则该电池的负极的电极反应式为
您最近一年使用:0次
名校
解题方法
4 . 某溶液中只含有Ba2+ Mg2+ Ag+三种阳离子,现用适量的NaOH溶液、稀盐酸和Na2SO4溶液将这三种离子逐一沉淀分离,其流程如图所示:
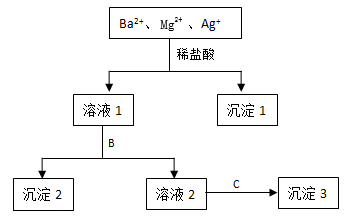
(1)沉淀1的化学式为_________ ,生成该沉淀的离子方程式为______________ 。
(2)若试剂B为Na2SO4溶液,则沉淀2化学式为______________ 。
(3)若试剂B为NaOH溶液,则生成沉淀2的离子方程式为______________ 。
(4)如果原溶液中Ba2+ Mg2+ Ag+的浓度均为0.1 mol·L-1,且溶液中含有的阴离子只有NO3-,则溶液中NO3- 浓度为_______ mol·L-1。

(1)沉淀1的化学式为
(2)若试剂B为Na2SO4溶液,则沉淀2化学式为
(3)若试剂B为NaOH溶液,则生成沉淀2的离子方程式为
(4)如果原溶液中Ba2+ Mg2+ Ag+的浓度均为0.1 mol·L-1,且溶液中含有的阴离子只有NO3-,则溶液中NO3- 浓度为
您最近一年使用:0次
2017-02-17更新
|
895次组卷
|
6卷引用:贵州省兴义中学2017-2018学年高一上学期期中考试化学试题
11-12高一上·广西百色·阶段练习
5 . 按如图所示操作,充分反应后:

(1) I中铁丝上观察到的现象是______ ;反应的化学方程式为______ ;
(2) II中发生反应的化学方程式为______ ;
(3)结合I、II实验现象可知,Fe、Cu、Ag的还原性顺序为______ 。

(1) I中铁丝上观察到的现象是
(2) II中发生反应的化学方程式为
(3)结合I、II实验现象可知,Fe、Cu、Ag的还原性顺序为
您最近一年使用:0次



