解题方法
1 . 配制100mL1mol/LNaOH溶液,请完成下列填空。
(1)计算并用“托盘天平称”取_____ gNaOH。
(2)配制过程部分操作如下图所示(没有按先后排序),正确的先后顺序为_____ 。
_____→_____→_____→_____→_____→E(填写“下列字母”)。
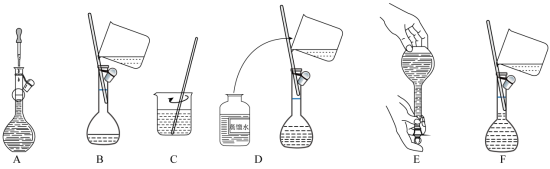
(3)判断下列操作对NaOH溶液的物质的量浓度的影响(填“偏高”“偏低”或“无影响”)。
①定容时俯视刻度线,配得溶液浓度将_____ 。
②容量瓶中原有少量蒸馏水,配得溶液浓度将_____ 。
(1)计算并用“托盘天平称”取
(2)配制过程部分操作如下图所示(没有按先后排序),正确的先后顺序为
_____→_____→_____→_____→_____→E(填写“下列字母”)。

(3)判断下列操作对NaOH溶液的物质的量浓度的影响(填“偏高”“偏低”或“无影响”)。
①定容时俯视刻度线,配得溶液浓度将
②容量瓶中原有少量蒸馏水,配得溶液浓度将
您最近一年使用:0次
解题方法
2 . 下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色。
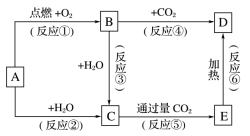
请填写下列空白:
(1)B为_____ (填“物质的颜色”)固体,D的化学式为_____ 。
(2)下列试剂不能鉴别等浓度D的水溶液和E的水溶液的是_____ (填“标号”)。
a.酚酞溶液 b.稀盐酸溶液 c.澄清石灰水 d.CaCl2溶液
(3)A→C反应的化学方程式:_____ 。
(4)B→C反应的离子方程式:_____ 。

请填写下列空白:
(1)B为
(2)下列试剂不能鉴别等浓度D的水溶液和E的水溶液的是
a.酚酞溶液 b.稀盐酸溶液 c.澄清石灰水 d.CaCl2溶液
(3)A→C反应的化学方程式:
(4)B→C反应的离子方程式:
您最近一年使用:0次
解题方法
3 . 已知实验室常用二氧化锰粉末和浓盐酸制取氯气,其反应的化学方程式为: ,某实验小组用下图所示装置制取纯净干燥的氯气。
,某实验小组用下图所示装置制取纯净干燥的氯气。
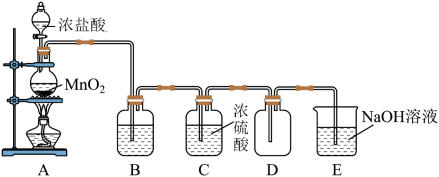
请回答下列问题:
(1)盛装MnO2的玻璃仪器的名称叫_____ 。
(2)B是除杂装置,盛放的试剂是_____ (填下列字母序号)
A.饱和食盐水 B.饱和NaHCO3溶液 C.饱和NaOH溶液
(3)C装置是用来干燥Cl2,其原理是利用了浓硫酸的_____ 性;
(4)装置D的收集方法为_____ 。
A.向上排空气法 B.向下排空气法
 ,某实验小组用下图所示装置制取纯净干燥的氯气。
,某实验小组用下图所示装置制取纯净干燥的氯气。
请回答下列问题:
(1)盛装MnO2的玻璃仪器的名称叫
(2)B是除杂装置,盛放的试剂是
A.饱和食盐水 B.饱和NaHCO3溶液 C.饱和NaOH溶液
(3)C装置是用来干燥Cl2,其原理是利用了浓硫酸的
(4)装置D的收集方法为
A.向上排空气法 B.向下排空气法
您最近一年使用:0次
4 . 某无色稀溶液X中,可能含有下表所列离子中的一种或几种。
现取适量该溶液于锥形瓶中,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示。

回答下列问题:
(1)仅通过观察颜色,可以判断溶液X中一定不存在的离子是_______ (用化学用语表示)。
(2)若Y是盐酸,则Oa段生成的沉淀为_______ (填化学式);ab段发生反应的离子为_______ (用化学用语表示),bc段发生反应的离子方程式为_______ ;取少量d点对应的上层清液于试管中,加入几滴硝酸银溶液,有白色沉淀生成,不能证明溶液X中含有 ,原因是
,原因是_______ 。
(3)若Y是NaOH溶液,则X中一定含有的离子是_______ ;ab段反应的离子方程式为_______ 。
| 阴离子 |  、 、 、 、 、 、 |
| 阳离子 |  、 、 、 、 、 、 、 、 |

回答下列问题:
(1)仅通过观察颜色,可以判断溶液X中一定不存在的离子是
(2)若Y是盐酸,则Oa段生成的沉淀为
 ,原因是
,原因是(3)若Y是NaOH溶液,则X中一定含有的离子是
您最近一年使用:0次
5 . 化学小组同学为研究氯气制备和氯水的成分及性质进行了如下实验。
【实验1】制备氯气。如图是实验室制取纯净、干燥氯气的装置图。
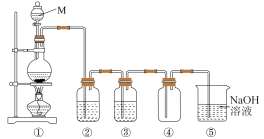
(1)M的名称是___________ ,①中反应的化学方程式是___________ 。
(2)③中存放的试剂是___________ 。(填“浓硫酸”或“饱和食盐水”)
(3)⑤中NaOH溶液的作用是___________ 。
【实验1】制备氯气。如图是实验室制取纯净、干燥氯气的装置图。

(1)M的名称是
(2)③中存放的试剂是
(3)⑤中NaOH溶液的作用是
您最近一年使用:0次
解题方法
6 . 请根据题意填空
(1)属于电解质的是___________ 。(填“铜”或“碳酸钠粉末”)
(2)NaHSO4在水溶液中的电离方程式为___________ 。
(3)现用0.5mol·L-1的NaCl溶液配制500mL0.1mol·L-1的NaCl溶液,按要求回答下列问题:
①应选用的玻璃仪器有烧杯、量筒、玻璃棒、500mL容量瓶、___________ 。
②容量瓶在使用前,首先要___________ 。
③需量取0.5mol·L-1NaCl溶液的体积是___________ mL。
(1)属于电解质的是
(2)NaHSO4在水溶液中的电离方程式为
(3)现用0.5mol·L-1的NaCl溶液配制500mL0.1mol·L-1的NaCl溶液,按要求回答下列问题:
①应选用的玻璃仪器有烧杯、量筒、玻璃棒、500mL容量瓶、
②容量瓶在使用前,首先要
③需量取0.5mol·L-1NaCl溶液的体积是
您最近一年使用:0次
名校
解题方法
7 . 某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取PAFC(聚合氯化铁铝)[AlFe(OH)nCl6-n]m,设计生产流程如下,请回答下列问题:

(1)用10mol·L-1的浓盐酸配制2mol·L-1的稀盐酸500mL,所取浓盐酸的体积_______ mL,所用玻璃仪器除量筒、玻璃棒和胶头滴管外,还有_______ 。
A.500mL容量瓶 B.蒸发皿 C.烧瓶
(2)写出Al2O3和Fe2O3粉末与盐酸反应的离子方程式:_______ 、_______ 。
(3)取少量酸性溶液滴加几滴KSCN试剂,溶液变为_______ 色,证明含有Fe3+。
(4)通入氯气的目的是_______ 。
(5)加入NaOH调节pH时,氢氧化钠不宜过多,生成一种红褐色沉淀,已知Al(OH)3+NaOH=NaAlO2+2H2O。写出溶液中Al3+和Fe3+分别与过量NaOH反应的离子方程式:_______ 、_______ 。

(1)用10mol·L-1的浓盐酸配制2mol·L-1的稀盐酸500mL,所取浓盐酸的体积
A.500mL容量瓶 B.蒸发皿 C.烧瓶
(2)写出Al2O3和Fe2O3粉末与盐酸反应的离子方程式:
(3)取少量酸性溶液滴加几滴KSCN试剂,溶液变为
(4)通入氯气的目的是
(5)加入NaOH调节pH时,氢氧化钠不宜过多,生成一种红褐色沉淀,已知Al(OH)3+NaOH=NaAlO2+2H2O。写出溶液中Al3+和Fe3+分别与过量NaOH反应的离子方程式:
您最近一年使用:0次
2023-08-25更新
|
127次组卷
|
2卷引用:贵州省黔西南布依族苗族自治州兴义第一中学2022-2023学年高一下学期第三次月考化学试题
名校
8 . 二氧化氯(ClO2)是一种新型高效安全消毒剂,易溶于水,沸点为 ,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备
,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备 :向三颈烧瓶中加入
:向三颈烧瓶中加入 溶液、浓
溶液、浓 并通入空气,调节恒温器至
并通入空气,调节恒温器至 ,通过固体加料器缓慢匀速加入硫铁矿粉末。
,通过固体加料器缓慢匀速加入硫铁矿粉末。
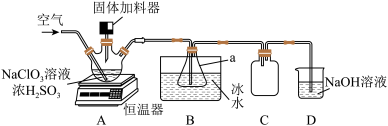
回答下列问题:
(1)仪器a的名称是_______ 。
(2)A装置中生成 的离子方程式为
的离子方程式为_______ ( 对应的产物为
对应的产物为 和
和 ),此离子反应中氧化产物与还原产物的物质的量之比为
),此离子反应中氧化产物与还原产物的物质的量之比为_______ 。
(3)装置C的作用是_______ 。
(4)装置D中 与NaOH溶液反应生成二种盐,其中一种为
与NaOH溶液反应生成二种盐,其中一种为 且二者物质的量之比为
且二者物质的量之比为 ,则另一种盐的化学式为
,则另一种盐的化学式为_______ 。
(5)一种主要成分为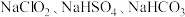 的“
的“ 泡腾片”,能快速溶于水,并产生大量气泡,得到含有
泡腾片”,能快速溶于水,并产生大量气泡,得到含有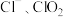 的溶液。上述过程中,每生成
的溶液。上述过程中,每生成 消耗
消耗 的物质的量为
的物质的量为_______ mol。
(6)工业上可用 与水中的
与水中的 在常温下反应,生成
在常温下反应,生成 和盐酸,以除去水中
和盐酸,以除去水中 。写出该反应的离子方程式:
。写出该反应的离子方程式:_______ 。
 ,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备
,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备 :向三颈烧瓶中加入
:向三颈烧瓶中加入 溶液、浓
溶液、浓 并通入空气,调节恒温器至
并通入空气,调节恒温器至 ,通过固体加料器缓慢匀速加入硫铁矿粉末。
,通过固体加料器缓慢匀速加入硫铁矿粉末。
回答下列问题:
(1)仪器a的名称是
(2)A装置中生成
 的离子方程式为
的离子方程式为 对应的产物为
对应的产物为 和
和 ),此离子反应中氧化产物与还原产物的物质的量之比为
),此离子反应中氧化产物与还原产物的物质的量之比为(3)装置C的作用是
(4)装置D中
 与NaOH溶液反应生成二种盐,其中一种为
与NaOH溶液反应生成二种盐,其中一种为 且二者物质的量之比为
且二者物质的量之比为 ,则另一种盐的化学式为
,则另一种盐的化学式为(5)一种主要成分为
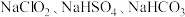 的“
的“ 泡腾片”,能快速溶于水,并产生大量气泡,得到含有
泡腾片”,能快速溶于水,并产生大量气泡,得到含有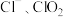 的溶液。上述过程中,每生成
的溶液。上述过程中,每生成 消耗
消耗 的物质的量为
的物质的量为(6)工业上可用
 与水中的
与水中的 在常温下反应,生成
在常温下反应,生成 和盐酸,以除去水中
和盐酸,以除去水中 。写出该反应的离子方程式:
。写出该反应的离子方程式:
您最近一年使用:0次
2022-10-08更新
|
213次组卷
|
3卷引用:贵州省顶效开发区顶兴学校2023-2024学年高三第三次月考化学试题
名校
解题方法
9 . 某研究性学习小组设计了用氧化浓盐酸的方法制取氯气的实验,其实验装置如图:

(1)写出圆底烧瓶中发生反应的化学方程式:__ 。
(2)如果将过量的二氧化锰与20mL12mol·L-1的盐酸混合加热,充分反应后生成的氯气明显少于0.06mol。其主要的原因有①__ ;②__ 。
(3)L的作用是___ ;饱和食盐水的作用是__ 。
(4)为了提高浓盐酸的利用率,你对实验的建议是__ 。

(1)写出圆底烧瓶中发生反应的化学方程式:
(2)如果将过量的二氧化锰与20mL12mol·L-1的盐酸混合加热,充分反应后生成的氯气明显少于0.06mol。其主要的原因有①
(3)L的作用是
(4)为了提高浓盐酸的利用率,你对实验的建议是
您最近一年使用:0次
2019-12-17更新
|
170次组卷
|
5卷引用:贵州省黔西县一中2018-2019学年高一第一学期12月考试化学试题
贵州省黔西县一中2018-2019学年高一第一学期12月考试化学试题河北省魏县第五中学2019-2020学年高一上学期第二次月考化学试题人教版高中化学必修1第四章《非金属及其化合物》测试卷2(已下线)3.1.1 氯气的发现与制备(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)上海市宝山区吴淞中学2022-2023学年高一上学期期中考试化学试题
解答题-实验探究题
|
适中(0.65)
|
名校
10 . 实验室欲用NaOH固体配制1.0 mol·L-1的NaOH溶液240 mL:
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却 ⑨摇动
其正确的操作顺序为__________________ 。必须用到的玻璃仪器有烧杯、胶头滴管、________________ 。
(2)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示。烧杯的实际质量为________ g,要完成本实验该同学应称出________ g NaOH。

(3)使用容量瓶前必须进行的一步操作是________ 。
(4)如图是该同学转移溶液的示意图,图中有两处错误,请写出:

①________________________________________________________________________
②________________________________________________________________________
(5)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是________ (填字母)。
A.所用NaOH已经潮解
B.向容量瓶中加水未到刻度线
C.有少量NaOH溶液残留在烧杯里
D.用带游码的托盘天平称5.4 g NaOH(1 g以下用游码)时误用了“左码右物”方法
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却 ⑨摇动
其正确的操作顺序为
(2)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示。烧杯的实际质量为

(3)使用容量瓶前必须进行的一步操作是
(4)如图是该同学转移溶液的示意图,图中有两处错误,请写出:

①
②
(5)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是
A.所用NaOH已经潮解
B.向容量瓶中加水未到刻度线
C.有少量NaOH溶液残留在烧杯里
D.用带游码的托盘天平称5.4 g NaOH(1 g以下用游码)时误用了“左码右物”方法
您最近一年使用:0次
2018-12-17更新
|
259次组卷
|
10卷引用:贵州省黔西县一中2018-2019学年高一第一学期12月考试化学试题
贵州省黔西县一中2018-2019学年高一第一学期12月考试化学试题贵州省遵义习水县一中2018-2019学年高一上学期11月份考试化学试题安徽省合肥市肥东县高级中学2019-2020学年高一上学期期末考试化学试题人教版高中化学必修1第一章《从实验学化学》测试卷1人教版高中化学必修1第一章《从实验学化学》测试卷4(已下线)【新东方】2020-42安徽省滁州市定远县重点中学2020-2021学年高一10月月考化学试题(已下线)第02讲 物质的量浓度(练)— 2022年高考化学一轮复习讲练测(新教材新高考)河南省柘城县第二高级中学2021-2022学年高一上学期第二次月考化学试题江苏省启东市东南中学2023-2024学年高一上学期第二次质量检测化学试卷



