解题方法
1 . 配制100mL1mol/LNaOH溶液,请完成下列填空。
(1)计算并用“托盘天平称”取_____ gNaOH。
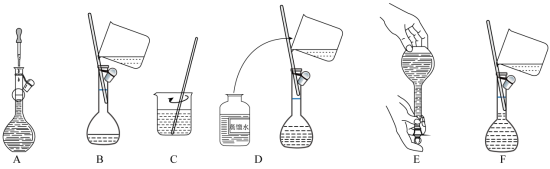
(2)配制过程部分操作如下图所示(没有按先后排序),正确的先后顺序为_____ 。
_____→_____→_____→_____→_____→E(填写“下列字母”)。
(3)判断下列操作对NaOH溶液的物质的量浓度的影响(填“偏高”“偏低”或“无影响”)。
①定容时俯视刻度线,配得溶液浓度将_____ 。
②容量瓶中原有少量蒸馏水,配得溶液浓度将_____ 。
(1)计算并用“托盘天平称”取
(2)配制过程部分操作如下图所示(没有按先后排序),正确的先后顺序为
_____→_____→_____→_____→_____→E(填写“下列字母”)。

(3)判断下列操作对NaOH溶液的物质的量浓度的影响(填“偏高”“偏低”或“无影响”)。
①定容时俯视刻度线,配得溶液浓度将
②容量瓶中原有少量蒸馏水,配得溶液浓度将
您最近一年使用:0次
解题方法
2 . 下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色。
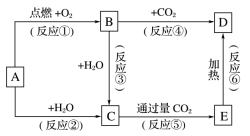
请填写下列空白:
(1)B为_____ (填“物质的颜色”)固体,D的化学式为_____ 。
(2)下列试剂不能鉴别等浓度D的水溶液和E的水溶液的是_____ (填“标号”)。
a.酚酞溶液 b.稀盐酸溶液 c.澄清石灰水 d.CaCl2溶液
(3)A→C反应的化学方程式:_____ 。
(4)B→C反应的离子方程式:_____ 。

请填写下列空白:
(1)B为
(2)下列试剂不能鉴别等浓度D的水溶液和E的水溶液的是
a.酚酞溶液 b.稀盐酸溶液 c.澄清石灰水 d.CaCl2溶液
(3)A→C反应的化学方程式:
(4)B→C反应的离子方程式:
您最近一年使用:0次
解题方法
3 . 已知实验室常用二氧化锰粉末和浓盐酸制取氯气,其反应的化学方程式为: ,某实验小组用下图所示装置制取纯净干燥的氯气。
,某实验小组用下图所示装置制取纯净干燥的氯气。
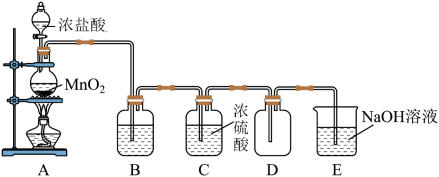
请回答下列问题:
(1)盛装MnO2的玻璃仪器的名称叫_____ 。
(2)B是除杂装置,盛放的试剂是_____ (填下列字母序号)
A.饱和食盐水 B.饱和NaHCO3溶液 C.饱和NaOH溶液
(3)C装置是用来干燥Cl2,其原理是利用了浓硫酸的_____ 性;
(4)装置D的收集方法为_____ 。
A.向上排空气法 B.向下排空气法
 ,某实验小组用下图所示装置制取纯净干燥的氯气。
,某实验小组用下图所示装置制取纯净干燥的氯气。
请回答下列问题:
(1)盛装MnO2的玻璃仪器的名称叫
(2)B是除杂装置,盛放的试剂是
A.饱和食盐水 B.饱和NaHCO3溶液 C.饱和NaOH溶液
(3)C装置是用来干燥Cl2,其原理是利用了浓硫酸的
(4)装置D的收集方法为
A.向上排空气法 B.向下排空气法
您最近一年使用:0次
4 . 某无色稀溶液X中,可能含有下表所列离子中的一种或几种。
现取适量该溶液于锥形瓶中,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示。

回答下列问题:
(1)仅通过观察颜色,可以判断溶液X中一定不存在的离子是_______ (用化学用语表示)。
(2)若Y是盐酸,则Oa段生成的沉淀为_______ (填化学式);ab段发生反应的离子为_______ (用化学用语表示),bc段发生反应的离子方程式为_______ ;取少量d点对应的上层清液于试管中,加入几滴硝酸银溶液,有白色沉淀生成,不能证明溶液X中含有 ,原因是
,原因是_______ 。
(3)若Y是NaOH溶液,则X中一定含有的离子是_______ ;ab段反应的离子方程式为_______ 。
| 阴离子 |  、 、 、 、 、 、 |
| 阳离子 |  、 、 、 、 、 、 、 、 |

回答下列问题:
(1)仅通过观察颜色,可以判断溶液X中一定不存在的离子是
(2)若Y是盐酸,则Oa段生成的沉淀为
 ,原因是
,原因是(3)若Y是NaOH溶液,则X中一定含有的离子是
您最近一年使用:0次
5 . 化学小组同学为研究氯气制备和氯水的成分及性质进行了如下实验。
【实验1】制备氯气。如图是实验室制取纯净、干燥氯气的装置图。
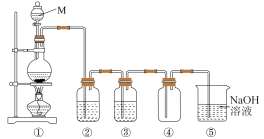
(1)M的名称是___________ ,①中反应的化学方程式是___________ 。
(2)③中存放的试剂是___________ 。(填“浓硫酸”或“饱和食盐水”)
(3)⑤中NaOH溶液的作用是___________ 。
【实验1】制备氯气。如图是实验室制取纯净、干燥氯气的装置图。

(1)M的名称是
(2)③中存放的试剂是
(3)⑤中NaOH溶液的作用是
您最近一年使用:0次
解题方法
6 . 请根据题意填空
(1)属于电解质的是___________ 。(填“铜”或“碳酸钠粉末”)
(2)NaHSO4在水溶液中的电离方程式为___________ 。
(3)现用0.5mol·L-1的NaCl溶液配制500mL0.1mol·L-1的NaCl溶液,按要求回答下列问题:
①应选用的玻璃仪器有烧杯、量筒、玻璃棒、500mL容量瓶、___________ 。
②容量瓶在使用前,首先要___________ 。
③需量取0.5mol·L-1NaCl溶液的体积是___________ mL。
(1)属于电解质的是
(2)NaHSO4在水溶液中的电离方程式为
(3)现用0.5mol·L-1的NaCl溶液配制500mL0.1mol·L-1的NaCl溶液,按要求回答下列问题:
①应选用的玻璃仪器有烧杯、量筒、玻璃棒、500mL容量瓶、
②容量瓶在使用前,首先要
③需量取0.5mol·L-1NaCl溶液的体积是
您最近一年使用:0次
名校
解题方法
7 . 某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取PAFC(聚合氯化铁铝)[AlFe(OH)nCl6-n]m,设计生产流程如下,请回答下列问题:

(1)用10mol·L-1的浓盐酸配制2mol·L-1的稀盐酸500mL,所取浓盐酸的体积_______ mL,所用玻璃仪器除量筒、玻璃棒和胶头滴管外,还有_______ 。
A.500mL容量瓶 B.蒸发皿 C.烧瓶
(2)写出Al2O3和Fe2O3粉末与盐酸反应的离子方程式:_______ 、_______ 。
(3)取少量酸性溶液滴加几滴KSCN试剂,溶液变为_______ 色,证明含有Fe3+。
(4)通入氯气的目的是_______ 。
(5)加入NaOH调节pH时,氢氧化钠不宜过多,生成一种红褐色沉淀,已知Al(OH)3+NaOH=NaAlO2+2H2O。写出溶液中Al3+和Fe3+分别与过量NaOH反应的离子方程式:_______ 、_______ 。

(1)用10mol·L-1的浓盐酸配制2mol·L-1的稀盐酸500mL,所取浓盐酸的体积
A.500mL容量瓶 B.蒸发皿 C.烧瓶
(2)写出Al2O3和Fe2O3粉末与盐酸反应的离子方程式:
(3)取少量酸性溶液滴加几滴KSCN试剂,溶液变为
(4)通入氯气的目的是
(5)加入NaOH调节pH时,氢氧化钠不宜过多,生成一种红褐色沉淀,已知Al(OH)3+NaOH=NaAlO2+2H2O。写出溶液中Al3+和Fe3+分别与过量NaOH反应的离子方程式:
您最近一年使用:0次
2023-08-25更新
|
123次组卷
|
2卷引用:贵州省黔西南布依族苗族自治州兴义第一中学2022-2023学年高一下学期第三次月考化学试题
名校
8 . 二氧化氯(ClO2)是一种新型高效安全消毒剂,易溶于水,沸点为 ,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备
,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备 :向三颈烧瓶中加入
:向三颈烧瓶中加入 溶液、浓
溶液、浓 并通入空气,调节恒温器至
并通入空气,调节恒温器至 ,通过固体加料器缓慢匀速加入硫铁矿粉末。
,通过固体加料器缓慢匀速加入硫铁矿粉末。
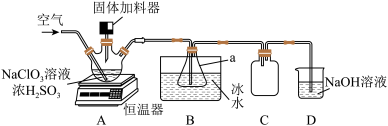
回答下列问题:
(1)仪器a的名称是_______ 。
(2)A装置中生成 的离子方程式为
的离子方程式为_______ ( 对应的产物为
对应的产物为 和
和 ),此离子反应中氧化产物与还原产物的物质的量之比为
),此离子反应中氧化产物与还原产物的物质的量之比为_______ 。
(3)装置C的作用是_______ 。
(4)装置D中 与NaOH溶液反应生成二种盐,其中一种为
与NaOH溶液反应生成二种盐,其中一种为 且二者物质的量之比为
且二者物质的量之比为 ,则另一种盐的化学式为
,则另一种盐的化学式为_______ 。
(5)一种主要成分为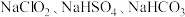 的“
的“ 泡腾片”,能快速溶于水,并产生大量气泡,得到含有
泡腾片”,能快速溶于水,并产生大量气泡,得到含有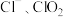 的溶液。上述过程中,每生成
的溶液。上述过程中,每生成 消耗
消耗 的物质的量为
的物质的量为_______ mol。
(6)工业上可用 与水中的
与水中的 在常温下反应,生成
在常温下反应,生成 和盐酸,以除去水中
和盐酸,以除去水中 。写出该反应的离子方程式:
。写出该反应的离子方程式:_______ 。
 ,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备
,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备 :向三颈烧瓶中加入
:向三颈烧瓶中加入 溶液、浓
溶液、浓 并通入空气,调节恒温器至
并通入空气,调节恒温器至 ,通过固体加料器缓慢匀速加入硫铁矿粉末。
,通过固体加料器缓慢匀速加入硫铁矿粉末。
回答下列问题:
(1)仪器a的名称是
(2)A装置中生成
 的离子方程式为
的离子方程式为 对应的产物为
对应的产物为 和
和 ),此离子反应中氧化产物与还原产物的物质的量之比为
),此离子反应中氧化产物与还原产物的物质的量之比为(3)装置C的作用是
(4)装置D中
 与NaOH溶液反应生成二种盐,其中一种为
与NaOH溶液反应生成二种盐,其中一种为 且二者物质的量之比为
且二者物质的量之比为 ,则另一种盐的化学式为
,则另一种盐的化学式为(5)一种主要成分为
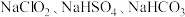 的“
的“ 泡腾片”,能快速溶于水,并产生大量气泡,得到含有
泡腾片”,能快速溶于水,并产生大量气泡,得到含有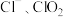 的溶液。上述过程中,每生成
的溶液。上述过程中,每生成 消耗
消耗 的物质的量为
的物质的量为(6)工业上可用
 与水中的
与水中的 在常温下反应,生成
在常温下反应,生成 和盐酸,以除去水中
和盐酸,以除去水中 。写出该反应的离子方程式:
。写出该反应的离子方程式:
您最近一年使用:0次
2022-10-08更新
|
212次组卷
|
3卷引用:贵州省顶效开发区顶兴学校2023-2024学年高三第三次月考化学试题
9 . 表中是元素周期表的一部分,按要求完成各小题。
(1)化学性质最不活泼的元素____ (填编号,下同),非金属性最强的元素是____ 。金属性最强的单质____ 。
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强的____ (化学式)。①③⑤三种元素的原子半径由大到小的顺序为____ 。
(3)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素的最高价氧化物和盐酸反应的化学方程式为____ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ⑥ | ⑦ | ⑾ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强的
(3)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素的最高价氧化物和盐酸反应的化学方程式为
您最近一年使用:0次
名校
解题方法
10 . 用铁、铝的混合物进行如下实验:
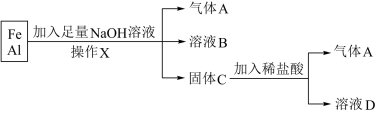
(1)操作X的名称是___________ 。
(2)气体A是___________ 。
(3)A与 混合光照可能发生爆炸,生成
混合光照可能发生爆炸,生成___________ (填化学式),A在该反应中作为___________ (填“氧化剂”或“还原剂”)。
(4)溶液B中阴离子除 外还有
外还有___________ ,溶液D中存在的金属离子为___________ 。

(1)操作X的名称是
(2)气体A是
(3)A与
 混合光照可能发生爆炸,生成
混合光照可能发生爆炸,生成(4)溶液B中阴离子除
 外还有
外还有
您最近一年使用:0次
2022-08-17更新
|
828次组卷
|
12卷引用:贵州省黔西南布依族苗族自治州晴隆县第二中学2019-2020学年高一上学期期末考试化学试题
贵州省黔西南布依族苗族自治州晴隆县第二中学2019-2020学年高一上学期期末考试化学试题(已下线)2011-2012学年北京市育园中学高二上学期期中考试化学(理)试卷云南省盈江县民族完全中学2019-2020学年高二上学期期末考试化学试题福建省晋江市养正中学2019-2020学年高二上学期第二次月考化学试题云南省丽江市宁蒗县第一中学2019—2020学年高一上学期期末考试化学试题云南省昭通市彝良县第二中学2019—2020学年高一上学期期末考试化学试题贵州省雷山县第四中学2019-2020学年高一上学期期末考试化学试题广西壮族自治区来宾市忻城县民族中学2019-2020学年高一上学期期末考试化学试题第二节 金属材料 第1课时 合金黑龙江省哈尔滨市第六中学校2022—2023学年高一上学期期中考试化学试题云南省广南县第一中学校2021-2022学年高一下学期3月份考试化学试题作业(十九) 常见的合金及其应用



