1 . 某无色稀溶液X中,可能含有下表所列离子中的一种或几种。
现取适量该溶液于锥形瓶中,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示。

回答下列问题:
(1)仅通过观察颜色,可以判断溶液X中一定不存在的离子是_______ (用化学用语表示)。
(2)若Y是盐酸,则Oa段生成的沉淀为_______ (填化学式);ab段发生反应的离子为_______ (用化学用语表示),bc段发生反应的离子方程式为_______ ;取少量d点对应的上层清液于试管中,加入几滴硝酸银溶液,有白色沉淀生成,不能证明溶液X中含有 ,原因是
,原因是_______ 。
(3)若Y是NaOH溶液,则X中一定含有的离子是_______ ;ab段反应的离子方程式为_______ 。
| 阴离子 |  、 、 、 、 、 、 |
| 阳离子 |  、 、 、 、 、 、 、 、 |

回答下列问题:
(1)仅通过观察颜色,可以判断溶液X中一定不存在的离子是
(2)若Y是盐酸,则Oa段生成的沉淀为
 ,原因是
,原因是(3)若Y是NaOH溶液,则X中一定含有的离子是
您最近一年使用:0次
2 . 化学小组同学为研究氯气制备和氯水的成分及性质进行了如下实验。
【实验1】制备氯气。如图是实验室制取纯净、干燥氯气的装置图。
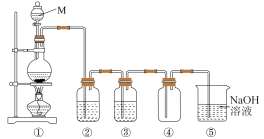
(1)M的名称是___________ ,①中反应的化学方程式是___________ 。
(2)③中存放的试剂是___________ 。(填“浓硫酸”或“饱和食盐水”)
(3)⑤中NaOH溶液的作用是___________ 。
【实验1】制备氯气。如图是实验室制取纯净、干燥氯气的装置图。

(1)M的名称是
(2)③中存放的试剂是
(3)⑤中NaOH溶液的作用是
您最近一年使用:0次
解题方法
3 . 请根据题意填空
(1)属于电解质的是___________ 。(填“铜”或“碳酸钠粉末”)
(2)NaHSO4在水溶液中的电离方程式为___________ 。
(3)现用0.5mol·L-1的NaCl溶液配制500mL0.1mol·L-1的NaCl溶液,按要求回答下列问题:
①应选用的玻璃仪器有烧杯、量筒、玻璃棒、500mL容量瓶、___________ 。
②容量瓶在使用前,首先要___________ 。
③需量取0.5mol·L-1NaCl溶液的体积是___________ mL。
(1)属于电解质的是
(2)NaHSO4在水溶液中的电离方程式为
(3)现用0.5mol·L-1的NaCl溶液配制500mL0.1mol·L-1的NaCl溶液,按要求回答下列问题:
①应选用的玻璃仪器有烧杯、量筒、玻璃棒、500mL容量瓶、
②容量瓶在使用前,首先要
③需量取0.5mol·L-1NaCl溶液的体积是
您最近一年使用:0次
名校
4 . 二氧化氯(ClO2)是一种新型高效安全消毒剂,易溶于水,沸点为 ,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备
,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备 :向三颈烧瓶中加入
:向三颈烧瓶中加入 溶液、浓
溶液、浓 并通入空气,调节恒温器至
并通入空气,调节恒温器至 ,通过固体加料器缓慢匀速加入硫铁矿粉末。
,通过固体加料器缓慢匀速加入硫铁矿粉末。
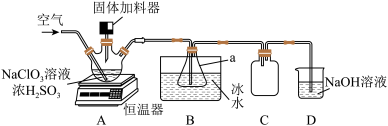
回答下列问题:
(1)仪器a的名称是_______ 。
(2)A装置中生成 的离子方程式为
的离子方程式为_______ ( 对应的产物为
对应的产物为 和
和 ),此离子反应中氧化产物与还原产物的物质的量之比为
),此离子反应中氧化产物与还原产物的物质的量之比为_______ 。
(3)装置C的作用是_______ 。
(4)装置D中 与NaOH溶液反应生成二种盐,其中一种为
与NaOH溶液反应生成二种盐,其中一种为 且二者物质的量之比为
且二者物质的量之比为 ,则另一种盐的化学式为
,则另一种盐的化学式为_______ 。
(5)一种主要成分为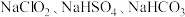 的“
的“ 泡腾片”,能快速溶于水,并产生大量气泡,得到含有
泡腾片”,能快速溶于水,并产生大量气泡,得到含有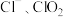 的溶液。上述过程中,每生成
的溶液。上述过程中,每生成 消耗
消耗 的物质的量为
的物质的量为_______ mol。
(6)工业上可用 与水中的
与水中的 在常温下反应,生成
在常温下反应,生成 和盐酸,以除去水中
和盐酸,以除去水中 。写出该反应的离子方程式:
。写出该反应的离子方程式:_______ 。
 ,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备
,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备 :向三颈烧瓶中加入
:向三颈烧瓶中加入 溶液、浓
溶液、浓 并通入空气,调节恒温器至
并通入空气,调节恒温器至 ,通过固体加料器缓慢匀速加入硫铁矿粉末。
,通过固体加料器缓慢匀速加入硫铁矿粉末。
回答下列问题:
(1)仪器a的名称是
(2)A装置中生成
 的离子方程式为
的离子方程式为 对应的产物为
对应的产物为 和
和 ),此离子反应中氧化产物与还原产物的物质的量之比为
),此离子反应中氧化产物与还原产物的物质的量之比为(3)装置C的作用是
(4)装置D中
 与NaOH溶液反应生成二种盐,其中一种为
与NaOH溶液反应生成二种盐,其中一种为 且二者物质的量之比为
且二者物质的量之比为 ,则另一种盐的化学式为
,则另一种盐的化学式为(5)一种主要成分为
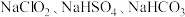 的“
的“ 泡腾片”,能快速溶于水,并产生大量气泡,得到含有
泡腾片”,能快速溶于水,并产生大量气泡,得到含有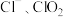 的溶液。上述过程中,每生成
的溶液。上述过程中,每生成 消耗
消耗 的物质的量为
的物质的量为(6)工业上可用
 与水中的
与水中的 在常温下反应,生成
在常温下反应,生成 和盐酸,以除去水中
和盐酸,以除去水中 。写出该反应的离子方程式:
。写出该反应的离子方程式:
您最近一年使用:0次
2022-10-08更新
|
213次组卷
|
3卷引用:贵州省顶效开发区顶兴学校2023-2024学年高三第三次月考化学试题
5 . 表中是元素周期表的一部分,按要求完成各小题。
(1)化学性质最不活泼的元素____ (填编号,下同),非金属性最强的元素是____ 。金属性最强的单质____ 。
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强的____ (化学式)。①③⑤三种元素的原子半径由大到小的顺序为____ 。
(3)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素的最高价氧化物和盐酸反应的化学方程式为____ 。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ⑥ | ⑦ | ⑾ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强的
(3)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素的最高价氧化物和盐酸反应的化学方程式为
您最近一年使用:0次
11-12高二上·北京·期中
名校
解题方法
6 . 用铁、铝的混合物进行如下实验:
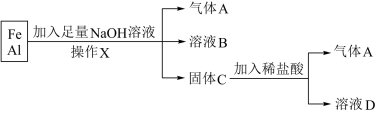
(1)操作X的名称是___________ 。
(2)气体A是___________ 。
(3)A与 混合光照可能发生爆炸,生成
混合光照可能发生爆炸,生成___________ (填化学式),A在该反应中作为___________ (填“氧化剂”或“还原剂”)。
(4)溶液B中阴离子除 外还有
外还有___________ ,溶液D中存在的金属离子为___________ 。

(1)操作X的名称是
(2)气体A是
(3)A与
 混合光照可能发生爆炸,生成
混合光照可能发生爆炸,生成(4)溶液B中阴离子除
 外还有
外还有
您最近一年使用:0次
2022-08-17更新
|
831次组卷
|
12卷引用:贵州省黔西南布依族苗族自治州晴隆县第二中学2019-2020学年高一上学期期末考试化学试题
贵州省黔西南布依族苗族自治州晴隆县第二中学2019-2020学年高一上学期期末考试化学试题(已下线)2011-2012学年北京市育园中学高二上学期期中考试化学(理)试卷云南省盈江县民族完全中学2019-2020学年高二上学期期末考试化学试题福建省晋江市养正中学2019-2020学年高二上学期第二次月考化学试题云南省丽江市宁蒗县第一中学2019—2020学年高一上学期期末考试化学试题云南省昭通市彝良县第二中学2019—2020学年高一上学期期末考试化学试题贵州省雷山县第四中学2019-2020学年高一上学期期末考试化学试题广西壮族自治区来宾市忻城县民族中学2019-2020学年高一上学期期末考试化学试题第二节 金属材料 第1课时 合金黑龙江省哈尔滨市第六中学校2022—2023学年高一上学期期中考试化学试题云南省广南县第一中学校2021-2022学年高一下学期3月份考试化学试题作业(十九) 常见的合金及其应用
7 .  与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐。某兴趣小组利用如图装置以
与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐。某兴趣小组利用如图装置以 分别与KOH溶液和NaOH溶液反应为原理,制备
分别与KOH溶液和NaOH溶液反应为原理,制备 和NaClO,并探究
和NaClO,并探究 和NaClO的部分性质。
和NaClO的部分性质。
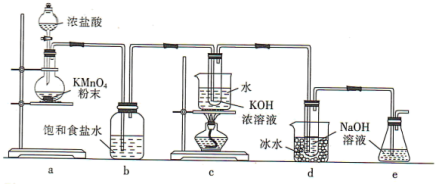
回答下列问题:
(1)a装置所用玻璃仪器的名称为______ (任意写一种);发生反应的离子方程式为____________ 。
(2)b装置的作用是____________ ;e装置的作用是____________ 。
(3)已知:c装置中得到的是 ,d装置中得到的是NaClO。
,d装置中得到的是NaClO。
①由此判断氯气与碱反应时,影响产物的因素有____________ 。
②NaClO溶液常温时稳定,受热时会生成两种盐,NaBrO溶液在0℃时稳定,常温时会生成两种盐,则常温时, 与KOH溶液反应的离子方程式为
与KOH溶液反应的离子方程式为____________ 。
(4)取少量c、d装置中生成的 和NaClO溶液(两溶液均调至碱性),分别置于1号和2号试管中,向两试管中分别滴加等量且适量的KI溶液。1号试管溶液颜色不变;2号试管溶液颜色变为棕色,加入
和NaClO溶液(两溶液均调至碱性),分别置于1号和2号试管中,向两试管中分别滴加等量且适量的KI溶液。1号试管溶液颜色不变;2号试管溶液颜色变为棕色,加入 ,振荡、静置后
,振荡、静置后 层显
层显_______ 色。由此可推知,在碱性条件下, 的氧化能力
的氧化能力______ (填“>”或“<”)NaClO的氧化能力。
(5)该兴趣小组在40℃条件下,将一定量的 通入600 mL
通入600 mL  NaOH溶液中,NaOH恰好反应完全,得到的产物中含有NaCl、NaClO和
NaOH溶液中,NaOH恰好反应完全,得到的产物中含有NaCl、NaClO和 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为______ mol。
 与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐。某兴趣小组利用如图装置以
与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐。某兴趣小组利用如图装置以 分别与KOH溶液和NaOH溶液反应为原理,制备
分别与KOH溶液和NaOH溶液反应为原理,制备 和NaClO,并探究
和NaClO,并探究 和NaClO的部分性质。
和NaClO的部分性质。
回答下列问题:
(1)a装置所用玻璃仪器的名称为
(2)b装置的作用是
(3)已知:c装置中得到的是
 ,d装置中得到的是NaClO。
,d装置中得到的是NaClO。①由此判断氯气与碱反应时,影响产物的因素有
②NaClO溶液常温时稳定,受热时会生成两种盐,NaBrO溶液在0℃时稳定,常温时会生成两种盐,则常温时,
 与KOH溶液反应的离子方程式为
与KOH溶液反应的离子方程式为(4)取少量c、d装置中生成的
 和NaClO溶液(两溶液均调至碱性),分别置于1号和2号试管中,向两试管中分别滴加等量且适量的KI溶液。1号试管溶液颜色不变;2号试管溶液颜色变为棕色,加入
和NaClO溶液(两溶液均调至碱性),分别置于1号和2号试管中,向两试管中分别滴加等量且适量的KI溶液。1号试管溶液颜色不变;2号试管溶液颜色变为棕色,加入 ,振荡、静置后
,振荡、静置后 层显
层显 的氧化能力
的氧化能力(5)该兴趣小组在40℃条件下,将一定量的
 通入600 mL
通入600 mL  NaOH溶液中,NaOH恰好反应完全,得到的产物中含有NaCl、NaClO和
NaOH溶液中,NaOH恰好反应完全,得到的产物中含有NaCl、NaClO和 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为
您最近一年使用:0次
2022-07-12更新
|
113次组卷
|
2卷引用:贵州省黔西南布依族苗族自治州2021-2022学年高二下学期期末质量检测化学试题
解题方法
8 . 锆产品的主要原料是锆英砂,全球90%的氧氯化锆(ZrOCl2)来源于中国。氧氯化锆可溶于水,微溶于盐酸,工业上以锆英砂(含91.5%ZrSiO4,杂质不与NaOH溶液反应)为原料生产ZrOCl2的一种工艺流程如图所示。
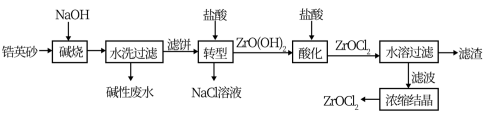
已知:碱金属的锆酸盐在水中溶解度很小,可在酸性条件下水解。
请回答下列问题:
(1)锆英砂在“碱烧”前粉碎的目的是____ ,“碱烧”时ZrSiO4生成了Na2ZrO3和另一种钠盐X,X的化学式为___ ,X的用途是___ (写一种)。
(2)“转型”时发生反应的化学方程式为___ 。
(3)“酸化”过程需加入过量盐酸,该操作中发生反应的化学方程式是___ 。
(4)“水溶过滤”操作后要对滤渣进行洗涤,洗涤液与滤液合并浓缩结晶,检查滤渣已经洗涤干净的实验是___ 。
(5)将锆英砂和焦炭混合,再与Cl2反应生成ZrCl4、SiCl4和一种可燃性气体,ZrCl4水解也可得到ZrOCl2。生成 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为___ 。
(6)某工厂用2t锆英砂来制备ZrOCl2,若这个过程中Zr的损耗率为15%,则最终制得ZrOCl2的质量为___ t。

已知:碱金属的锆酸盐在水中溶解度很小,可在酸性条件下水解。
请回答下列问题:
(1)锆英砂在“碱烧”前粉碎的目的是
(2)“转型”时发生反应的化学方程式为
(3)“酸化”过程需加入过量盐酸,该操作中发生反应的化学方程式是
(4)“水溶过滤”操作后要对滤渣进行洗涤,洗涤液与滤液合并浓缩结晶,检查滤渣已经洗涤干净的实验是
(5)将锆英砂和焦炭混合,再与Cl2反应生成ZrCl4、SiCl4和一种可燃性气体,ZrCl4水解也可得到ZrOCl2。生成
 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为(6)某工厂用2t锆英砂来制备ZrOCl2,若这个过程中Zr的损耗率为15%,则最终制得ZrOCl2的质量为
您最近一年使用:0次
2021-10-01更新
|
516次组卷
|
5卷引用:贵州省黔西南州2021~2022学年高二上学期期中考试化学试题
贵州省黔西南州2021~2022学年高二上学期期中考试化学试题河南省偃师市第一高级中学2022届高三阶段性测试化学试题福建省南平市2022届高三10月联考化学试卷重庆市2021-2022学年高二上学期期中考试化学试题(已下线)专题11 无机工艺流程题—2022年高考化学二轮复习讲练测(全国版)-测试
9 . 黄铜矿(主要成分为CuFeS2,还含有少量的SiO2和Al2O3)是制取铜及其化合物的主要原料之一,还可用于制备绿矾(化学式为FeSO4·7H2O)。
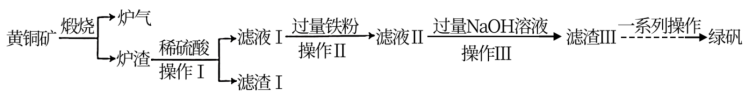
(1)黄铜矿“煅烧”时发生的反应为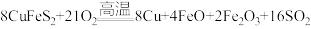 。若CuFeS2中Fe的化合价为+2价,则该反应中被还原的元素是
。若CuFeS2中Fe的化合价为+2价,则该反应中被还原的元素是___________ (填元素符号)。
(2)“滤渣Ⅰ”的主要成分为___________ ,“滤渣Ⅲ”的主要成分为___________ 。(填化学式)
(3)“滤液Ⅱ”中含有的金属阳离子有___________ (填离子符号)。
(4)上述“煅烧”过程会产生“炉气”(主要成分为SO2)。下列对“炉气”的处理方案中合理的是___________ (填标号)。
A.高空排放 B.用于制备硫酸
C.用纯碱溶液吸收制Na2SO3 D.用浓硫酸吸收
(5)“操作Ⅰ”的名称为___________ 。

(1)黄铜矿“煅烧”时发生的反应为
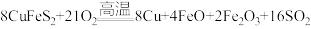 。若CuFeS2中Fe的化合价为+2价,则该反应中被还原的元素是
。若CuFeS2中Fe的化合价为+2价,则该反应中被还原的元素是(2)“滤渣Ⅰ”的主要成分为
(3)“滤液Ⅱ”中含有的金属阳离子有
(4)上述“煅烧”过程会产生“炉气”(主要成分为SO2)。下列对“炉气”的处理方案中合理的是
A.高空排放 B.用于制备硫酸
C.用纯碱溶液吸收制Na2SO3 D.用浓硫酸吸收
(5)“操作Ⅰ”的名称为
您最近一年使用:0次
10 . 下表是元素周期表的一部分。根据表中的8种元素,用元素符号或化学式填空。
(1)元素f、g的最高价氧化物对应水化物的酸性:___________ >___________ 。
(2)元素d、g、h的简单离子中,半径最大的是___________ (填离子符号)。
(3)c和h形成的化合物 中含有的化学键类型为
中含有的化学键类型为___________ 。
(4)写出元素a和c形成原子个数比为1∶1的化合物的电子式:___________ 。
(5)写出d的最高价氧化物对应的水化物与h的最高价氧化物对应的水化物反应的离子方程式:___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | a | |||||||
| 2 | b | c | ||||||
| 3 | d | e | f | g | ||||
| 4 | h |
(2)元素d、g、h的简单离子中,半径最大的是
(3)c和h形成的化合物
 中含有的化学键类型为
中含有的化学键类型为(4)写出元素a和c形成原子个数比为1∶1的化合物的电子式:
(5)写出d的最高价氧化物对应的水化物与h的最高价氧化物对应的水化物反应的离子方程式:
您最近一年使用:0次



