1 . 为了除去某NaCl固体样品中含有的 、
、 和
和 杂质,某化学小组选用
杂质,某化学小组选用 溶液、稀盐酸、
溶液、稀盐酸、 溶液三种试剂设计了如下流程。
溶液三种试剂设计了如下流程。______ 、____ 、____ 。
(2)沉淀C的成分是____ 。
(3)写出加入碳酸钠溶液后发生反应的化学方程式________ 。(写出一个即可)
 、
、 和
和 杂质,某化学小组选用
杂质,某化学小组选用 溶液、稀盐酸、
溶液、稀盐酸、 溶液三种试剂设计了如下流程。
溶液三种试剂设计了如下流程。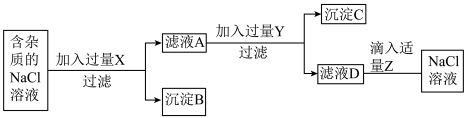
(2)沉淀C的成分是
(3)写出加入碳酸钠溶液后发生反应的化学方程式
您最近一年使用:0次
名校
解题方法
2 .  是一种高效多功能的绿色消毒剂和水处理剂。但是由于存在自催化现象[即分解产物
是一种高效多功能的绿色消毒剂和水处理剂。但是由于存在自催化现象[即分解产物 可催化高铁酸盐的分解],限制了它的大规模应用,研究使其稳定的方法尤为关键。
可催化高铁酸盐的分解],限制了它的大规模应用,研究使其稳定的方法尤为关键。
已知:①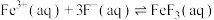
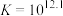
②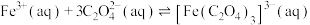

I.制备高铁酸盐
(1)在碱性条件下以多孔的磁铁矿作阳极电解制备高铁酸盐的电极反应式是___________ 。
Ⅱ.高铁酸盐稳定性的研究
(2)碱性环境下,久置的 溶液中除了产生红褐色
溶液中除了产生红褐色 外,同时还会产生绿色的
外,同时还会产生绿色的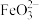 ,此过程的反应为
,此过程的反应为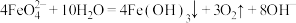 、
、___________ 。
为研究使稳定的方法,分别做以下4个实验:
资料:吸光度大小与溶液中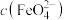 成正比。
成正比。___________ ,但吸光度结果图显示甲同学预测并不正确,原因可能是d试管加入的 与
与 发生配位反应的速率
发生配位反应的速率___________ (填“快”或“慢”),且进行程度大,导致催化剂 量减少,
量减少, 的分解速率
的分解速率___________ (填“快”或“慢”)。
(4)乙同学推测“ ”曲线为试管c的实验结果,依据是
”曲线为试管c的实验结果,依据是___________ 。
(5)综合以上分析,为增强高铁酸盐的稳定性,可向其中加入___________ (填化学式)。
Ⅲ.高铁酸盐产品纯度的测定
称取mg高铁酸钾粗品,配成250mL溶液,准确量取25.00mL放入锥形瓶,加入足量 和NaOH溶液,振荡,再加入稀硫酸酸化后得到
和NaOH溶液,振荡,再加入稀硫酸酸化后得到 和
和 ,滴入几滴二苯胺磺酸钠作指示剂,用
,滴入几滴二苯胺磺酸钠作指示剂,用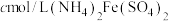 标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗
标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗 标准溶液VmL。
标准溶液VmL。
(6)粗品中 的质量分数为
的质量分数为___________ 。[已知: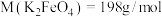 ]
]
 是一种高效多功能的绿色消毒剂和水处理剂。但是由于存在自催化现象[即分解产物
是一种高效多功能的绿色消毒剂和水处理剂。但是由于存在自催化现象[即分解产物 可催化高铁酸盐的分解],限制了它的大规模应用,研究使其稳定的方法尤为关键。
可催化高铁酸盐的分解],限制了它的大规模应用,研究使其稳定的方法尤为关键。已知:①
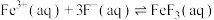
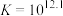
②
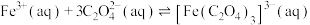

I.制备高铁酸盐
(1)在碱性条件下以多孔的磁铁矿作阳极电解制备高铁酸盐的电极反应式是
Ⅱ.高铁酸盐稳定性的研究
(2)碱性环境下,久置的
 溶液中除了产生红褐色
溶液中除了产生红褐色 外,同时还会产生绿色的
外,同时还会产生绿色的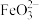 ,此过程的反应为
,此过程的反应为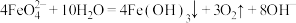 、
、为研究使稳定的方法,分别做以下4个实验:
| 序号 |  | 现象 | |
| a | 2滴0.01mol/LKI溶液 | 紫色迅速褪去 |
| b | 2滴蒸馏水 | 分别用紫外可见分光光度计测三支试管内溶液的吸光度,结果如下图所示。 | |
| c | 2滴0.01mol/LNaF溶液 | ||
| d | 2滴 溶液 溶液 |
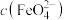 成正比。
成正比。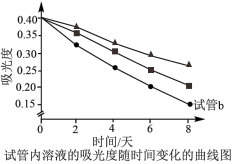
 与
与 发生配位反应的速率
发生配位反应的速率 量减少,
量减少, 的分解速率
的分解速率(4)乙同学推测“
 ”曲线为试管c的实验结果,依据是
”曲线为试管c的实验结果,依据是(5)综合以上分析,为增强高铁酸盐的稳定性,可向其中加入
Ⅲ.高铁酸盐产品纯度的测定
称取mg高铁酸钾粗品,配成250mL溶液,准确量取25.00mL放入锥形瓶,加入足量
 和NaOH溶液,振荡,再加入稀硫酸酸化后得到
和NaOH溶液,振荡,再加入稀硫酸酸化后得到 和
和 ,滴入几滴二苯胺磺酸钠作指示剂,用
,滴入几滴二苯胺磺酸钠作指示剂,用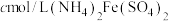 标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗
标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗 标准溶液VmL。
标准溶液VmL。(6)粗品中
 的质量分数为
的质量分数为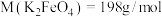 ]
]
您最近一年使用:0次
2024-06-05更新
|
261次组卷
|
4卷引用:2024届河南省信阳高级中学高三下学期考前最后一卷理科综合试题-高中化学
名校
解题方法
3 . 海水中化学元素的利用是指从海水中提取钠、镁、氯、溴等元素。_____________ 操作。
(2)过程c的化学反应方程式_____________________________________ 。
(3)过程b用于海水提溴.主要工业生产流程如下图所示。 ,利用了
,利用了 的氧化性,写出对应反应的离子方程式
的氧化性,写出对应反应的离子方程式_____________________________________________ 。
②吹出塔中通入热空气吹出 ,利用了
,利用了 的
的_____________ (填字母)。
A.氧化性 B.还原性 C.挥发性,沸点比水低 D.易溶于水
(4)实验室可以利用蒸馏的方法进行海水淡化,可选用如图装置完成。
①仪器B的名称是_____________ 。
②该装置中有一处明显的错误是________________________ 。
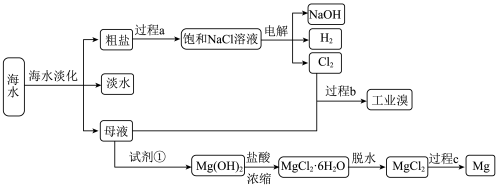
(2)过程c的化学反应方程式
(3)过程b用于海水提溴.主要工业生产流程如下图所示。

 ,利用了
,利用了 的氧化性,写出对应反应的离子方程式
的氧化性,写出对应反应的离子方程式②吹出塔中通入热空气吹出
 ,利用了
,利用了 的
的A.氧化性 B.还原性 C.挥发性,沸点比水低 D.易溶于水
(4)实验室可以利用蒸馏的方法进行海水淡化,可选用如图装置完成。
①仪器B的名称是
②该装置中有一处明显的错误是

您最近一年使用:0次
名校
解题方法
4 . 随着原子序数的递增,8种短周期元素(用英文字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示._____________ 。
(2)元素x分别与y、z、d形成的10电子气态分子中,热稳定性由强到弱的顺序为_____________ (填化学式).元素z、d、e、f形成的简单离子中半径最大的离子是_____________ (填离子符号)。
(3)将化合物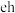 由固态加热至熔融态,吸收的能量主要用于断裂
由固态加热至熔融态,吸收的能量主要用于断裂_____________ 键(填“离子”或“共价”).x与d可形成多种共价分子,其中三原子共价分子的电子式为_____________ ;四原子共价分子的结构式为_____________ 。
(4)不能作为比较g与h的非金属性强弱的依据是____________。
(5)x和g的形成的二元化合物与h的单质发生反应的离子方程式为___________ 。
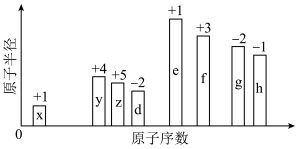
(2)元素x分别与y、z、d形成的10电子气态分子中,热稳定性由强到弱的顺序为
(3)将化合物
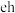 由固态加热至熔融态,吸收的能量主要用于断裂
由固态加热至熔融态,吸收的能量主要用于断裂(4)不能作为比较g与h的非金属性强弱的依据是____________。
| A.氢化物酸性h强于g | B.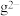 的还原性强于 的还原性强于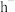 |
| C.与x单质反应,g单质比h单质更困难 | D.常温下g单质呈固态,h单质呈气态 |
(5)x和g的形成的二元化合物与h的单质发生反应的离子方程式为
您最近一年使用:0次
名校
5 . 常温下,二甲基亚砜( )为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸点为189℃。实验室模拟“
)为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸点为189℃。实验室模拟“ 氧化法”制备二甲基亚砜的装置如图所示(加热装置及夹持装置已省略)。
氧化法”制备二甲基亚砜的装置如图所示(加热装置及夹持装置已省略)。

①制备二甲基亚砜的反应原理为
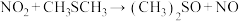 。
。②二甲基硫醚和二甲基亚砜的密度分别为
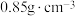 和
和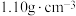 。
。③
 微热易分解为NO、
微热易分解为NO、 和
和 。
。实验过程:将仪器A中制得的气体通入15.00mL二甲基硫醚中,控制温度为60∼80℃,反应一段时间得到二甲基亚砜粗品,粗品经减压蒸馏后共收集到11.10mL二甲基亚砜纯品。回答下列问题:
(1)通入
 的目的是
的目的是a.碱石灰 b.
 c.硅胶
c.硅胶(2)冷凝管进出水的方向
(3)二甲基亚砜能与水混溶的原因可能为
(4)NaOH溶液吸收尾气中NO和
 生成亚硝酸盐的化学方程式为
生成亚硝酸盐的化学方程式为(5)本实验的产率是
您最近一年使用:0次
2024-05-29更新
|
248次组卷
|
6卷引用:2024届河南省周口市西华县第一高级中学高三下学期信息卷第四练理综试题-高中化学
解题方法
6 . 下表列出了①~⑩十种元素在元素周期表中的位置。
(1)⑦的单质和⑤的最高价氧化物对应的水化物反应的方程式:________ 。
(2)⑧的固态氢化物CaH2与H2O反应生成Ca(OH)2和一种可燃性气体单质____ 。(填化学式)
(3)某小组同学设计实验比较VIIA族元素的非金属性:Cl>Br>I。
甲同学设计实验如下:打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有KBr溶液的棉球变为橙黄色,湿润的淀粉KI试纸变蓝,已知:常温下浓盐酸与高锰酸钾反应生成氯气。____ 。
②除了利用卤素单质间的置换反应,下列可作为卤族元素非金属性递变规律的判断依据有____ 。(填字母)
A.Cl2、Br2、I2的熔点逐渐升高 B.HCl、HBr、HI的稳定性逐渐减弱
C.HCl、HBr、HI水溶液的酸性逐渐增强 D.Cl﹣、Br﹣、I﹣的还原性逐渐增强
③写出圆底烧瓶中发生的化学反应方程式____ 。
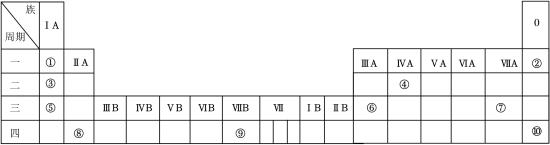
(1)⑦的单质和⑤的最高价氧化物对应的水化物反应的方程式:
(2)⑧的固态氢化物CaH2与H2O反应生成Ca(OH)2和一种可燃性气体单质
(3)某小组同学设计实验比较VIIA族元素的非金属性:Cl>Br>I。
甲同学设计实验如下:打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有KBr溶液的棉球变为橙黄色,湿润的淀粉KI试纸变蓝,已知:常温下浓盐酸与高锰酸钾反应生成氯气。
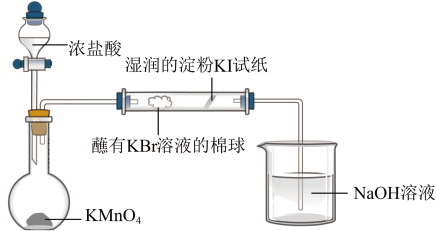
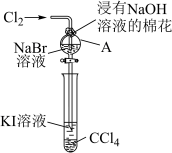
②除了利用卤素单质间的置换反应,下列可作为卤族元素非金属性递变规律的判断依据有
A.Cl2、Br2、I2的熔点逐渐升高 B.HCl、HBr、HI的稳定性逐渐减弱
C.HCl、HBr、HI水溶液的酸性逐渐增强 D.Cl﹣、Br﹣、I﹣的还原性逐渐增强
③写出圆底烧瓶中发生的化学反应方程式
您最近一年使用:0次
7 . 无水氯化铝是有机合成中常用的催化剂,易溶于水,吸水性强,易升华,熔融状态下不导电。某化学兴趣小组设计如图所示装置制备无水氯化铝,请回答下列问题:______ ;乙处洗气瓶中所盛装的试剂为______ ,乙装置的作用是_______ 。
(2)实验时先点燃甲处的酒精灯,当观察到_______ (填现象)时,点燃丁处的酒精灯;丁处硬质玻璃管内发生反应的化学方程式为______ ;己处干燥管内盛装的试剂可选择_______ (填标号),该装置的作用是_______ 。
a.NaCl b.碱石灰 c.
(3)工业上常将用砂纸打磨后的铝锭放入密闭的高温氯化反应炉内,氯气向上顺着导管送入炉内,与熔融的铝反应生成三氯化铝。用砂纸打磨铝锭的目的是_______ 。

(2)实验时先点燃甲处的酒精灯,当观察到
a.NaCl b.碱石灰 c.

(3)工业上常将用砂纸打磨后的铝锭放入密闭的高温氯化反应炉内,氯气向上顺着导管送入炉内,与熔融的铝反应生成三氯化铝。用砂纸打磨铝锭的目的是
您最近一年使用:0次
解题方法
8 . X、Y、Z、W、R、V是原子序数依次增大的短周期主族元素,Y形成的一种氧化物是常见的温室气体,Z、W是空气中含量排前二的元素,W与V、Z与R均为同主族元素,六种元素形成的一种化合物M的结构如图所示。请回答下列问题:______ ;R的原子结构示意图为_______ ;Z的最简单氢化物的化学式为______ 。
(2)原子半径:Y_____ (填“>”“<”或“=”,下同)W;非金属性:V____ W;R的K层电子总数与L层电子总数之比为_____ (填最简整数比)。
(3)下列说法正确的是_______(填标号)。
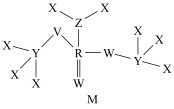
(2)原子半径:Y
(3)下列说法正确的是_______(填标号)。
| A.M分子中所有原子均满足8电子稳定结构 |
| B.仅由X、Z、W元素形成的化合物可能为离子化合物 |
C. 常用作保护气 常用作保护气 |
| D.R元素的氧化物对应的水化物为强酸 |
您最近一年使用:0次
名校
解题方法
9 . 现有下列短周期元素的数据(已知Be的原子半径为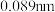 ):
):
(1)上述元素处于同一主族的有___________ (用元素符号表示);比较①⑤⑥的离子半径大小:___________ >___________ >___________ (用离子符号表示)
(2)元素①和⑥能形成两种化合物,写出其中较稳定的化合物与水反应的离子方程式:___________ 。
(3)②和⑦可形成一种化合物,写出该化合物的电子式:___________ 。
(4)含锂材料在社会中广泛应用,如各种储氢材料 等)、便携式电源材料
等)、便携式电源材料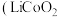 等);
等); 和
和 作核反应堆最佳热载体,
作核反应堆最佳热载体,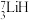 和
和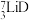 用作高温堆减速剂。下列说法中正确的是
用作高温堆减速剂。下列说法中正确的是___________ 。
A. 和
和 属于同种核素
属于同种核素
B.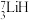 和
和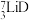 的化学性质不同
的化学性质不同
C.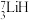 和
和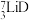 互为同素异形体
互为同素异形体
D.氧化性:
E.赋性:
F.半径: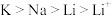
(5)胶奆磁流体在医学上有重要的用途,而纳米级 是磁流体中的重要粒子,其制备过程可简单表示如下:将⑦的最简单的气态氢化物通入到等物质的量的
是磁流体中的重要粒子,其制备过程可简单表示如下:将⑦的最简单的气态氢化物通入到等物质的量的 的混合燃液中,生成两种碱,写出该反应过程中的总离子方程式
的混合燃液中,生成两种碱,写出该反应过程中的总离子方程式___________ 。反应生成的两种䂸继续作用即得到产品。
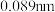 ):
):| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(nm) | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
| 最高正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低负化合价 | -2 | -3 | -1 | -3 |
(2)元素①和⑥能形成两种化合物,写出其中较稳定的化合物与水反应的离子方程式:
(3)②和⑦可形成一种化合物,写出该化合物的电子式:
(4)含锂材料在社会中广泛应用,如各种储氢材料
 等)、便携式电源材料
等)、便携式电源材料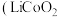 等);
等); 和
和 作核反应堆最佳热载体,
作核反应堆最佳热载体,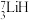 和
和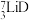 用作高温堆减速剂。下列说法中正确的是
用作高温堆减速剂。下列说法中正确的是A.
 和
和 属于同种核素
属于同种核素B.
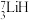 和
和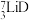 的化学性质不同
的化学性质不同C.
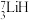 和
和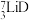 互为同素异形体
互为同素异形体D.氧化性:

E.赋性:

F.半径:
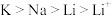
(5)胶奆磁流体在医学上有重要的用途,而纳米级
 是磁流体中的重要粒子,其制备过程可简单表示如下:将⑦的最简单的气态氢化物通入到等物质的量的
是磁流体中的重要粒子,其制备过程可简单表示如下:将⑦的最简单的气态氢化物通入到等物质的量的 的混合燃液中,生成两种碱,写出该反应过程中的总离子方程式
的混合燃液中,生成两种碱,写出该反应过程中的总离子方程式
您最近一年使用:0次
名校
10 . 某实验室利用 和
和 反应合成硫酰氯
反应合成硫酰氯 ,并对
,并对 和
和 的酸性强弱进行探究。已知:①
的酸性强弱进行探究。已知:① 的熔点为
的熔点为 ,沸点为
,沸点为 ,在空气中遇水蒸气发生剧烈反应,并产生大量
,在空气中遇水蒸气发生剧烈反应,并产生大量 白雾,
白雾,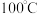 以上分解生成
以上分解生成 和
和 ;②实验室合成
;②实验室合成 的原理:
的原理: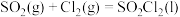 ,且反应会放出大量的热。实验装置如图(夹持仪器已省略)请回答下列问题:
,且反应会放出大量的热。实验装置如图(夹持仪器已省略)请回答下列问题:___________ 、___________ 。
(2)装置戊上方分液漏斗中最好选用___________(填字母)。
(3)装置乙和丁盛放的试剂均是___________ 。
(4) 和水反应的化学方程式为
和水反应的化学方程式为___________ 。
(5)装置丙放置在冰水浴中的原因是___________ 。
(6)选用下面的装置探究酸性: ,溶液均足量。
,溶液均足量。___________ (填序号)
①ACF
②ACBF
③ACBEDF
④ABCEDF
能证明 的酸性强于
的酸性强于 的实验现象为
的实验现象为___________ 。
 和
和 反应合成硫酰氯
反应合成硫酰氯 ,并对
,并对 和
和 的酸性强弱进行探究。已知:①
的酸性强弱进行探究。已知:① 的熔点为
的熔点为 ,沸点为
,沸点为 ,在空气中遇水蒸气发生剧烈反应,并产生大量
,在空气中遇水蒸气发生剧烈反应,并产生大量 白雾,
白雾,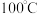 以上分解生成
以上分解生成 和
和 ;②实验室合成
;②实验室合成 的原理:
的原理: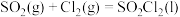 ,且反应会放出大量的热。实验装置如图(夹持仪器已省略)请回答下列问题:
,且反应会放出大量的热。实验装置如图(夹持仪器已省略)请回答下列问题:
(2)装置戊上方分液漏斗中最好选用___________(填字母)。
| A.蒸馏水 |
| B.浓氢氧化钠溶液 |
| C.饱和食盐水 |
D. 盐酸 盐酸 |
(3)装置乙和丁盛放的试剂均是
(4)
 和水反应的化学方程式为
和水反应的化学方程式为(5)装置丙放置在冰水浴中的原因是
(6)选用下面的装置探究酸性:
 ,溶液均足量。
,溶液均足量。
①ACF
②ACBF
③ACBEDF
④ABCEDF
能证明
 的酸性强于
的酸性强于 的实验现象为
的实验现象为
您最近一年使用:0次




