河南省荥阳市京城高中2023-2024学年高一下学期3月月考化学试题
河南
高一
阶段练习
2024-05-26
43次
整体难度:
容易
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、认识化学科学、物质结构与性质、化学实验基础
河南省荥阳市京城高中2023-2024学年高一下学期3月月考化学试题
河南
高一
阶段练习
2024-05-26
43次
整体难度:
容易
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、认识化学科学、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
解题方法
1. 我国高铁技术飞速发展,被视为中国“新四大发明”之一、下列说法正确的是
| A.高铁轨道与地基之间填隙减震材料聚氨酯属于有机高分子材料 |
| B.高铁上的信息传输系统使用了光导纤维,其主要成分是硅 |
| C.高铁车厢采用铝合金材料制作,是因为常温下铝耐腐蚀不与氧气反应 |
| D.高铁车厢连接处使用的增强聚四氟乙烯板,可通过四氟乙烯单体缩聚而成 |
【知识点】 二氧化硅的用途解读 加聚物的单体、链节及聚合度的确定解读 高分子材料
您最近一年使用:0次
单选题
|
容易(0.94)
名校
解题方法
2. 下列化学用语或说法正确的是
A.中子数为35的溴原子: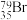 | B.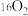 、 、 、 、 互称同位素 互称同位素 |
C. 的结构示意图: 的结构示意图: | D.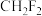 的电子式: 的电子式: |
【知识点】 有关粒子结构的化学用语 元素、核素、同位素解读
您最近一年使用:0次
2022-09-06更新
|
318次组卷
|
4卷引用:山东省泰安市2021-2022学年高一下学期期末考试化学试题
单选题
|
较易(0.85)
3. 下图分别表示元素的某种性质与核电荷数的变化趋势,下列说法错误的是
A.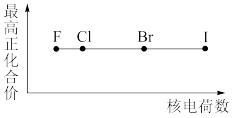 | B.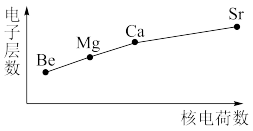 |
C. | D.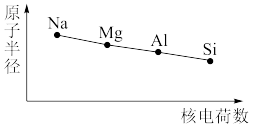 |
您最近一年使用:0次
2024-02-03更新
|
84次组卷
|
2卷引用:贵州贵阳市2023-2024学年高一上学期期末考试化学试卷
单选题
|
适中(0.65)
名校
4. 根据元素周期律,对下列事实进行推测,其中推测不合理的是
| 选项 | 事实 | 推测 |
| A |  与水反应缓慢, 与水反应缓慢, 与水反应较快 与水反应较快 |  (第 (第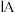 族元素的单质)与水反应更剧烈 族元素的单质)与水反应更剧烈 |
| B |  是强酸, 是强酸, 也是强酸 也是强酸 |  属于强酸 属于强酸 |
| C |  的沸点为 的沸点为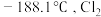 的沸点为 的沸点为 |  的沸点大于 的沸点大于 |
| D |  与 与 在暗处剧烈化合, 在暗处剧烈化合, 与 与 光照或点燃时反应 光照或点燃时反应 |  与 与 反应需要加热到一定温度 反应需要加热到一定温度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-26更新
|
186次组卷
|
4卷引用:河北郑口中学2023-2024学年高一上学期1月期末测试 化学试题
单选题
|
较易(0.85)
名校
5. “分类法”是一种常见的学习和研究化学的方法,下列关于电解质、非电解质、离子化合物、共价化合物的分类正确的是
| 选项 | 电解质 | 非电解质 | 离子化合物 | 共价化合物 |
| A | 铁 | 干冰 | 氧化镁 | 二氧化硫 |
| B | 蒸馏水 | 乙醇 | 硝酸铵 | 硫酸 |
| C | 纯碱 | 硫酸钡 | 氯化钙 | 过氧化氢 |
| D | 明矾 | 二氧化氮 | 碳酸氢钠 | 氢气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-07更新
|
65次组卷
|
2卷引用:湖南省长沙市湖南师范大学附属中学2023-2024学年高一下学期入学考试化学试卷
单选题
|
适中(0.65)
6. 氮化硅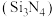 陶瓷材料可用于原子反应堆。氮化硅可由如下反应制得:
陶瓷材料可用于原子反应堆。氮化硅可由如下反应制得: 。下列说法正确的是
。下列说法正确的是
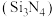 陶瓷材料可用于原子反应堆。氮化硅可由如下反应制得:
陶瓷材料可用于原子反应堆。氮化硅可由如下反应制得: 。下列说法正确的是
。下列说法正确的是A.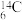 中电子数为8 中电子数为8 | B. 的电子式为 的电子式为 |
C. 属于离子化合物 属于离子化合物 | D.生成 转移 转移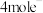 |
您最近一年使用:0次
2024-03-04更新
|
126次组卷
|
2卷引用:江西省部分学校2023-2024学年高一下学期开学考化学试题
单选题
|
适中(0.65)
解题方法
7. 已知X、Y、Z为原子序数依次增大的短周期元素,其中Z的非金属性是主族元素中最大的,这三种元素能形成化合物的结构如图所示。下列说法正确的是

| A.非金属性由大到小的顺序为:Z>X>Y |
| B.X原子最外层电子数为4 |
| C.Y元素的某种氢化物可作火箭的燃料 |
| D.Z元素的气态氢化物是同族元素中酸性最强的 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
8. mg某金属M溶于盐酸中,放出的气体在标准状况下的体积为nL,并生成氯化物MCl2,则金属M的相对原子质量是( )
| A.n/m | B.2m/n | C.m/22.4n | D.22.4m/n |
您最近一年使用:0次
2016-12-09更新
|
779次组卷
|
4卷引用:2012届高三上学期化学一轮复习《化学家眼中的物质世界》专题综合测试(苏教版)
(已下线)2012届高三上学期化学一轮复习《化学家眼中的物质世界》专题综合测试(苏教版)山西省朔州市怀仁市第一中学2018-2019学年高一上学期期中考试化学试题海南省农垦中学2023-2024学年高三上学期期末考试化学试题(A卷)河南省荥阳市京城高中2023-2024学年高一下学期3月月考化学试题
单选题
|
容易(0.94)
名校
解题方法
9. 下列各组物质性质比较的表示中,不正确的是
A.还原性: |
B.稳定性: |
C.氧化性: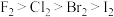 |
D.与水反应由易到难: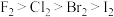 |
您最近一年使用:0次
2024-03-04更新
|
159次组卷
|
2卷引用:黑龙江省实验中学2023-2024学年高一下学期开学测试化学试题
单选题
|
较易(0.85)
10. 高纯硅可以采用下列方法制备.下列说法正确的是

| A.晶体Si导电性介于导体和绝缘体之间,常用于制造光导纤维 |
B.可以通过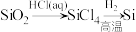 实现粗硅的制备 实现粗硅的制备 |
C.步骤①的反应为 ,不能说明碳的非金属性比硅强 ,不能说明碳的非金属性比硅强 |
D.已知电负性: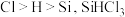 遇水会剧烈反应,化学方程式为 遇水会剧烈反应,化学方程式为 |
您最近一年使用:0次
2024-03-01更新
|
378次组卷
|
2卷引用:山东省部分学校2023-2024学年高三下学期2月份大联考(开学)质量检测化学试题
单选题
|
较易(0.85)
名校
11. 下表是元素周期表的一部分,下列说法正确的是
| Si | P | S | Cl | Ar |
| Ge | As | Se | Br | Kr |
| Sn | Sb | Te | I | Xe |
| Pb | Bi | Po | Al | Rn |
A.原子半径: | B.稳定性: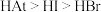 |
C.酸性: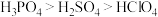 | D.上表中,元素Pb的金属性最强 |
您最近一年使用:0次
2023-07-16更新
|
342次组卷
|
3卷引用:北京市中国人民大学附属中学2022-2023学年高一下学期期末考试化学试题
单选题
|
适中(0.65)
名校
12. 元素周期表中蕴含着丰富的元素信息。下列说法正确的是
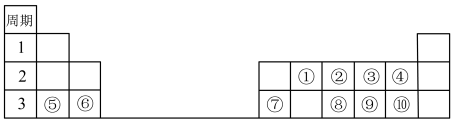
| A.单质的还原性:⑤<⑥<⑦ |
| B.简单离子的还原性:④>⑩ |
| C.氢元素与③形成的化合物中一定不含非极性键 |
| D.⑤的最高价氧化物对应的水化物的溶液可以和⑦的常见氧化物反应 |
您最近一年使用:0次
2024-03-07更新
|
115次组卷
|
2卷引用:湖南省长沙市湖南师范大学附属中学2023-2024学年高一下学期入学考试化学试卷
单选题
|
适中(0.65)
解题方法
13. 镁及其合金是用途很广的金属材料。某兴趣小组按如下步骤从海水中提取镁:

| A.操作①为过滤,试剂X可以选用NaOH溶液 |
| B.试剂Y为盐酸,相应离子方程式为Mg(OH)2+2H+=Mg2++2H2O |
| C.操作②在获得MgCl2晶体后需要进一步在空气中加热脱去结晶水 |
| D.与电解MgO相比,电解熔融MgCl2的方式冶炼金属镁具有节能优势 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
14. 从干海带中提取碘的实验流程如下:
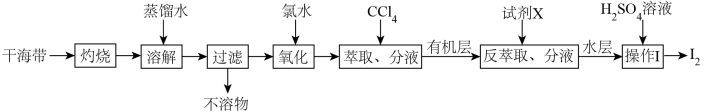
| A.氧化步骤中氯水可用过氧化氢代替 |
B.试剂X可以为 ,反萃取的离子方程式为: ,反萃取的离子方程式为: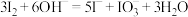 |
C. 可循环利用以有效提高干海带提碘的产率 可循环利用以有效提高干海带提碘的产率 |
| D.操作Ⅰ要用到普通漏斗、烧杯和玻璃棒 |
您最近一年使用:0次
2024-01-28更新
|
592次组卷
|
6卷引用:辽宁省五校联考2023-2024学年高三上学期期末考试化学试题
二、解答题 添加题型下试题
解答题-结构与性质
|
适中(0.65)
名校
解题方法
15. I、①碘的升华 ②烧碱熔化 ③氯化钠溶于水 ④氯化氢溶于水 ⑤氧气溶于水
⑥氯化铵受热分解。
未发生化学键破坏的是___________ ;仅发生离子键破坏的是___________ ;仅发生共价键破坏的是___________ ;既发生离子键又发生共价键破坏的是___________ ;
II、下列8种化学符号: O2、
O2、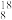 O2、
O2、 H、
H、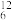 C、
C、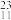 Na、
Na、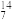 N、
N、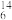 C、
C、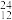 Mg。
Mg。
(1)表示核素的符号共___________ 种。
(2)互为同位素的是___________ 。
(3)质量相同的H216O和D216O所含中子数之比为___________ 。
根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:
(4)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式:___________ 。
(5)Be(OH)2与Mg(OH)2可用___________ 试剂鉴别。
⑥氯化铵受热分解。
未发生化学键破坏的是
II、下列8种化学符号:
 O2、
O2、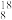 O2、
O2、 H、
H、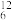 C、
C、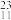 Na、
Na、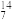 N、
N、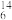 C、
C、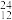 Mg。
Mg。(1)表示核素的符号共
(2)互为同位素的是
(3)质量相同的H216O和D216O所含中子数之比为
根据周期表对角线规则,金属Be与Al单质及其化合物性质相似。试回答下列问题:
(4)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式:
(5)Be(OH)2与Mg(OH)2可用
您最近一年使用:0次
2021-05-24更新
|
229次组卷
|
2卷引用:四川省内江市威远中学2020-2021学年高一下学期第一次月考化学试题
三、填空题 添加题型下试题
填空题
|
适中(0.65)
解题方法
16. 元素周期表可以用于探寻各种元素间的内在联系。
(1)下列关于元素周期表的说法错误的是______ 。
a.门捷列夫按照原子的核电荷数由小到大排列制出了第一张元素周期表
b.元素周期表由三个短周期,四个长周期构成
c.在金属和非金属的分界线处寻找半导体材料
d.元素周期表中含有主族、副族、第VⅢ族、0族等十八个族
(2)利用元素在周期表中的位置、结构、性质的关系,得出的结论正确的是______ 。
a.原子半径:Li>Na>K b.酸性:H3PO4>H2SO4>HClO4
c.稳定性:H2Se>H2S>H2O d.碱性:NaOH>Mg(OH)2>Al(OH)3
(3)碳族元素包括:C、Si、Ge、Sn、Pb、Fl(放射性元素)
①请完成CO2和KOH溶液恰好反应生成正盐的离子方程式_______ 。
②写出Si在元素周期表中的位置_______ 。由碳族元素结构特点,可推测Pb3O4中Pb的化合价为_____ 。
(4)卤族元素包括:F、Cl、Br、I、At(放射性元素)
①Br与F的原子序数的差值为______ 。
②已知某溶液中只含有Fe2+、Cl﹣、Br﹣、I﹣,且c(Cl﹣):c(Br﹣):c(I﹣)=1:1:2,则c(Fe2+):c(Br﹣)=____ 。向其中通入一定量的氯气发生反应,当c(Fe2+):c(Cl﹣)=1:4时,离子方程式为_____ 。
(1)下列关于元素周期表的说法错误的是
a.门捷列夫按照原子的核电荷数由小到大排列制出了第一张元素周期表
b.元素周期表由三个短周期,四个长周期构成
c.在金属和非金属的分界线处寻找半导体材料
d.元素周期表中含有主族、副族、第VⅢ族、0族等十八个族
(2)利用元素在周期表中的位置、结构、性质的关系,得出的结论正确的是
a.原子半径:Li>Na>K b.酸性:H3PO4>H2SO4>HClO4
c.稳定性:H2Se>H2S>H2O d.碱性:NaOH>Mg(OH)2>Al(OH)3
(3)碳族元素包括:C、Si、Ge、Sn、Pb、Fl(放射性元素)
①请完成CO2和KOH溶液恰好反应生成正盐的离子方程式
②写出Si在元素周期表中的位置
(4)卤族元素包括:F、Cl、Br、I、At(放射性元素)
①Br与F的原子序数的差值为
②已知某溶液中只含有Fe2+、Cl﹣、Br﹣、I﹣,且c(Cl﹣):c(Br﹣):c(I﹣)=1:1:2,则c(Fe2+):c(Br﹣)=
您最近一年使用:0次
四、解答题 添加题型下试题
解答题-无机推断题
|
适中(0.65)
解题方法
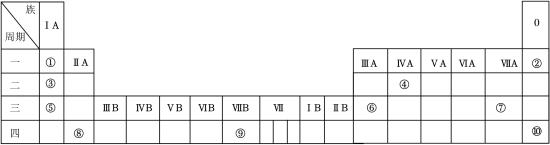
17. 下表列出了①~⑩十种元素在元素周期表中的位置。
(1)⑦的单质和⑤的最高价氧化物对应的水化物反应的方程式:________ 。
(2)⑧的固态氢化物CaH2与H2O反应生成Ca(OH)2和一种可燃性气体单质____ 。(填化学式)
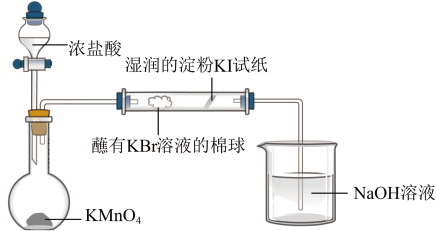
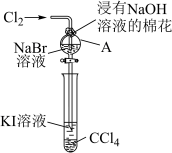
(3)某小组同学设计实验比较VIIA族元素的非金属性:Cl>Br>I。
甲同学设计实验如下:打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有KBr溶液的棉球变为橙黄色,湿润的淀粉KI试纸变蓝,已知:常温下浓盐酸与高锰酸钾反应生成氯气。____ 。
②除了利用卤素单质间的置换反应,下列可作为卤族元素非金属性递变规律的判断依据有____ 。(填字母)
A.Cl2、Br2、I2的熔点逐渐升高 B.HCl、HBr、HI的稳定性逐渐减弱
C.HCl、HBr、HI水溶液的酸性逐渐增强 D.Cl﹣、Br﹣、I﹣的还原性逐渐增强
③写出圆底烧瓶中发生的化学反应方程式____ 。
(1)⑦的单质和⑤的最高价氧化物对应的水化物反应的方程式:
(2)⑧的固态氢化物CaH2与H2O反应生成Ca(OH)2和一种可燃性气体单质
(3)某小组同学设计实验比较VIIA族元素的非金属性:Cl>Br>I。
甲同学设计实验如下:打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有KBr溶液的棉球变为橙黄色,湿润的淀粉KI试纸变蓝,已知:常温下浓盐酸与高锰酸钾反应生成氯气。
②除了利用卤素单质间的置换反应,下列可作为卤族元素非金属性递变规律的判断依据有
A.Cl2、Br2、I2的熔点逐渐升高 B.HCl、HBr、HI的稳定性逐渐减弱
C.HCl、HBr、HI水溶液的酸性逐渐增强 D.Cl﹣、Br﹣、I﹣的还原性逐渐增强
③写出圆底烧瓶中发生的化学反应方程式
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
18. 海水的综合利用是当今的热点话题之一。
Ⅰ.利用海水可以解决煤燃烧过程中排放的 造成的环境问题。其工艺流程如图所示:
造成的环境问题。其工艺流程如图所示: 吸收含硫的烟气后,会溶有
吸收含硫的烟气后,会溶有 、
、 等分子或离子,需要用氧气进行氧化处理,写出
等分子或离子,需要用氧气进行氧化处理,写出 参加反应的离子方程式
参加反应的离子方程式___________ 。
(2)氧化后的海水需用大量天然海水与之混合后才能排放。该操作的主要目的是___________ 。
Ⅱ.从海水中提取粗盐后的母液中含有 、
、 和
和 等阳离子。对母液进行一系列的加工可制得金属镁。
等阳离子。对母液进行一系列的加工可制得金属镁。
(3)从离子反应的角度思考,在母液中加入石灰乳的作用是___________ 。
(4)电解熔融无水氯化镁所得镁蒸气在特定环境中冷却后即为固体镁。下列物质中可以用作镁蒸气的冷却剂的是___________(填字母)。
Ⅲ.海带中含有碘元素。从海带中提取碘的实验过程如下图:___________ 。步骤③的分离操作为___________ 。
(6)写出步骤④反应的离子方程式___________ 。
Ⅰ.利用海水可以解决煤燃烧过程中排放的
 造成的环境问题。其工艺流程如图所示:
造成的环境问题。其工艺流程如图所示: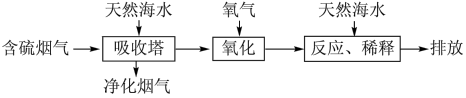
 吸收含硫的烟气后,会溶有
吸收含硫的烟气后,会溶有 、
、 等分子或离子,需要用氧气进行氧化处理,写出
等分子或离子,需要用氧气进行氧化处理,写出 参加反应的离子方程式
参加反应的离子方程式(2)氧化后的海水需用大量天然海水与之混合后才能排放。该操作的主要目的是
Ⅱ.从海水中提取粗盐后的母液中含有
 、
、 和
和 等阳离子。对母液进行一系列的加工可制得金属镁。
等阳离子。对母液进行一系列的加工可制得金属镁。(3)从离子反应的角度思考,在母液中加入石灰乳的作用是
(4)电解熔融无水氯化镁所得镁蒸气在特定环境中冷却后即为固体镁。下列物质中可以用作镁蒸气的冷却剂的是___________(填字母)。
A. | B. | C.Ar | D.水蒸气 |
Ⅲ.海带中含有碘元素。从海带中提取碘的实验过程如下图:

(6)写出步骤④反应的离子方程式
您最近一年使用:0次
2023-07-05更新
|
138次组卷
|
2卷引用:安徽省芜湖市2022-2023学年高一下学期7月考试化学试题
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、有机化学基础、化学与STSE、认识化学科学、物质结构与性质、化学实验基础
试卷题型(共 18题)
题型
数量
单选题
14
解答题
3
填空题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 二氧化硅的用途 加聚物的单体、链节及聚合度的确定 高分子材料 | |
| 2 | 0.94 | 有关粒子结构的化学用语 元素、核素、同位素 | |
| 3 | 0.85 | 同主族元素性质递变规律理解及应用 微粒半径大小的比较方法 | |
| 4 | 0.65 | 同主族元素性质递变规律 同主族元素性质递变规律理解及应用 | |
| 5 | 0.85 | 酸、碱、盐、氧化物 电解质、非电解质概念 非电解质、电解质物质类别判断 | |
| 6 | 0.65 | 电子式的书写与判断 元素、核素、同位素 电子转移计算 | |
| 7 | 0.65 | 元素非金属性强弱的比较方法 根据原子结构进行元素种类推断 | |
| 8 | 0.85 | 物质的量有关计算 根据n=m/M的相关计算 根据N=m·NA/M的相关推算 | |
| 9 | 0.94 | 同主族元素性质递变规律理解及应用 元素非金属性强弱的比较方法 | |
| 10 | 0.85 | 硅的制备 二氧化硅的化学性质 元素非金属性强弱的比较方法 元素性质与电负性的关系 | |
| 11 | 0.85 | 同周期元素性质递变规律 同主族元素性质递变规律理解及应用 元素非金属性强弱的比较方法 微粒半径大小的比较方法 | |
| 12 | 0.65 | 元素非金属性强弱的比较方法 “位构性”关系理解及应用 化学键与物质类别关系的判断 | |
| 13 | 0.65 | 常见金属的冶炼 海水提取镁 | |
| 14 | 0.65 | 氧化还原反应方程式的书写与配平 萃取和分液 过滤 海带中碘的提取及检验 | |
| 二、解答题 | |||
| 15 | 0.65 | 预测元素的性质 原子中相关数值及其之间的相互关系 元素、核素、同位素 化学键概念理解及判断 | 结构与性质 |
| 17 | 0.65 | 氧化还原反应方程式的书写与配平 氯气的实验室制法 元素非金属性强弱的比较方法 | 无机推断题 |
| 18 | 0.65 | 离子方程式的书写 仪器使用与实验安全 化学实验方案的设计与评价 海带中碘的提取及检验 | 工业流程题 |
| 三、填空题 | |||
| 16 | 0.65 | 氧化还原反应方程式的书写与配平 同主族元素性质递变规律 元素非金属性强弱的比较方法 微粒半径大小的比较方法 | |



