名校
1 . 周期表中前20号几种元素,其相关信息如下(铍的原子半径为0.089nm);F原子中无中子,G在地壳中含量居第二位,H元素焰色反应呈紫色。根据题意请回答下列问题:
(1)B的原子结构示意图为___________ 。
(2)F2C和F2E两种化合物中,沸点较高的是____ (填化学式)。
(3)用电子式表示化合物H2E的形成过程_______________________________ 。
(4)某同学设计了以G同族的短周期元素的最低价氢化物为燃料的电池,电解质为KOH。 则该电池的负极的电极反应式为__________________________________ 。
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.075 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +5,—3 | +3 | +6,—2 | —1 | —2 |
(2)F2C和F2E两种化合物中,沸点较高的是
(3)用电子式表示化合物H2E的形成过程
(4)某同学设计了以G同族的短周期元素的最低价氢化物为燃料的电池,电解质为KOH。 则该电池的负极的电极反应式为
您最近一年使用:0次
名校
解题方法
2 . 某溶液中只含有Ba2+ Mg2+ Ag+三种阳离子,现用适量的NaOH溶液、稀盐酸和Na2SO4溶液将这三种离子逐一沉淀分离,其流程如图所示:
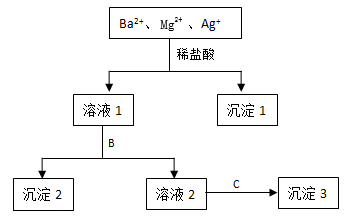
(1)沉淀1的化学式为_________ ,生成该沉淀的离子方程式为______________ 。
(2)若试剂B为Na2SO4溶液,则沉淀2化学式为______________ 。
(3)若试剂B为NaOH溶液,则生成沉淀2的离子方程式为______________ 。
(4)如果原溶液中Ba2+ Mg2+ Ag+的浓度均为0.1 mol·L-1,且溶液中含有的阴离子只有NO3-,则溶液中NO3- 浓度为_______ mol·L-1。

(1)沉淀1的化学式为
(2)若试剂B为Na2SO4溶液,则沉淀2化学式为
(3)若试剂B为NaOH溶液,则生成沉淀2的离子方程式为
(4)如果原溶液中Ba2+ Mg2+ Ag+的浓度均为0.1 mol·L-1,且溶液中含有的阴离子只有NO3-,则溶液中NO3- 浓度为
您最近一年使用:0次
2017-02-17更新
|
895次组卷
|
6卷引用:贵州省兴义中学2017-2018学年高一上学期期中考试化学试题
3 . A、B、C、D、E、F六种短周期主族元素,其原子序数依次增大,其中B与C同周期,D与E和F周周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D所在周期原子半径最大的主族元素,又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)元素F在周期表中的位置_______________________ ;
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)____________ ;
(3)由A、B、C三种元素以原子个数比4:2:3形成化合物X,X中所含化学键类型有_________ ;检验该化合物中的阳离子的方法是____________________ (用离子方程式表示及文字描述表示)。
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出D元素的最高价氧化物对应的水化物与E的最高价氧化物反应的离子方程式:_______________________ ;若E是非金属元素,其单质在电子工业中有重要应用,请写出其单质溶于强碱溶液的离子方程式:_______________________ 。
(1)元素F在周期表中的位置
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)
(3)由A、B、C三种元素以原子个数比4:2:3形成化合物X,X中所含化学键类型有
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出D元素的最高价氧化物对应的水化物与E的最高价氧化物反应的离子方程式:
您最近一年使用:0次
14-15高三上·云南昆明·期末
解题方法
4 . 如图是一个制取氯气并以氯气为原料进行特定反应的装置。

(l)A是氯气发生装置,写出其中的化学反应方程式___________ 。
(2)a仪器的名称为___________ 。
(3)实验开始时,先点燃A处的酒精灯,打开活塞K,让氯气充满整个装置,再点燃D处酒精灯,连接上E装置。D装置的硬质玻璃管内盛有炭粉,反应产物为CO2和HCl。写出D中反应的化学方程式_________ ,装置C的作用是__________ 。
(4)在E处,若漏斗内气体带有黄绿色,则紫色石蕊试液的颜色变化为_______ 。
(5)若将E处烧杯中溶液改为澄清石灰水,反应过程中现象为___________ (填序号)。
①有白色沉淀生成;②无白色沉淀生成;③先生成白色沉淀,而后白色沉淀消失。
(6)D处反应完毕后,关闭活塞K,移去酒精灯,由于余热的作用,A处仍有Cl2产生,则装置B中的现象是________ ;若发现装置B中该现象不明显,可能的原因是________ ;查找原因时可用肥皂水或湿润的碘化钾淀粉试纸等,若用蘸有浓氨水的玻璃棒检查时观察到有白烟产生,写出该氧化还原反应的化学方程式_________________________ 。

(l)A是氯气发生装置,写出其中的化学反应方程式
(2)a仪器的名称为
(3)实验开始时,先点燃A处的酒精灯,打开活塞K,让氯气充满整个装置,再点燃D处酒精灯,连接上E装置。D装置的硬质玻璃管内盛有炭粉,反应产物为CO2和HCl。写出D中反应的化学方程式
(4)在E处,若漏斗内气体带有黄绿色,则紫色石蕊试液的颜色变化为
(5)若将E处烧杯中溶液改为澄清石灰水,反应过程中现象为
①有白色沉淀生成;②无白色沉淀生成;③先生成白色沉淀,而后白色沉淀消失。
(6)D处反应完毕后,关闭活塞K,移去酒精灯,由于余热的作用,A处仍有Cl2产生,则装置B中的现象是
您最近一年使用:0次
10-11高三上·河北唐山·期中
名校
5 . 下面是用98%的浓硫酸(ρ=1.84 g·cm-3)配制500 mL 0.5 mol·L-1稀硫酸的操作,请按要求填空:
(1)所需浓硫酸的体积为__________ 。
(2)如果实验室有15 mL、20 mL、50 mL量筒,应选用________ mL量筒最好。量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将________ (填“偏高”“偏低”或“无影响”)。
(3)将量取的浓硫酸沿烧杯内壁慢慢注入盛有约100 mL水的____________ 里,并不断搅拌,目的是______ 。
(4)将____________ 的上述溶液沿__________ 注入__________ 中,并用50 mL蒸馏水洗涤烧杯2~3次,洗涤液要__________ 中,并摇匀。
(5)加水至距刻度线__________ 处,改用____________ 加水,使溶液的凹液面正好跟刻度线相平。
(1)所需浓硫酸的体积为
(2)如果实验室有15 mL、20 mL、50 mL量筒,应选用
(3)将量取的浓硫酸沿烧杯内壁慢慢注入盛有约100 mL水的
(4)将
(5)加水至距刻度线
您最近一年使用:0次
2016-12-09更新
|
987次组卷
|
8卷引用:贵州省黔西县一中2018-2019学年高一第一学期12月考试化学试题
贵州省黔西县一中2018-2019学年高一第一学期12月考试化学试题(已下线)2010年河北省唐山一中高三上学期期中考试化学卷(已下线)2011-2012学年河南省郑州市智林学校高一上学期期中考试化学试卷2015-2016学年上海市同济中学高一下学期期中考试化学试卷广西壮族自治区田阳高中2018-2019学年高一上学期12月月考化学试题鲁教版高中化学必修1第一章《认识化学科学》测试卷1河南省长葛市第一高级中学2021届高三上学期10月阶段性测试化学试题山东省菏泽市曹县第一中学2022-2023学年高一上学期期中教学质量检测化学试题
11-12高二下·浙江宁波·期中
6 . 亚甲基蓝(Methylnene Blue)在碱性条件下与葡萄糖作用生成亚甲基白(Methylene White),亚甲基蓝的结构简式: 。著名的蓝瓶子实验操作步骤如下:
。著名的蓝瓶子实验操作步骤如下:
①如图示在250mL锥形瓶中,依次加入2g NaOH、100mL H2O和3g葡萄糖,搅拌溶解后,再加入3滴~5滴0.2%的亚甲基蓝溶液,振荡混合液呈现蓝色;
②塞紧橡皮塞(活塞a、b关闭),将溶液静置,溶液变为无色;
③再打开瓶塞,振荡,溶液又变为蓝色;
④再塞紧橡皮塞,将溶液静置,溶液又变为无色,以上③、④可重复多次。
试回答下列问题:

(1)某学生将起初配得的蓝色溶液分装在A,B两支试管中(如上图,A试管充满溶液,B中有少量溶液),塞上橡皮塞静置片刻,两溶液均显无色,若再同时振荡A,B试管,能显蓝色的是_________ (填“A”或“B”);
(2)若塞紧锥形瓶塞并打开活塞a、b,通入足量氢气后,再关闭活塞a、b并振荡,溶液能否由无色变为蓝色_________ (填“能”或“不能”);若塞紧锥形瓶塞并打开a、b通入足量氧气,溶液能否由无色变为蓝色_________ (填“能”或“不能”);
(3)上述转化过程中,葡萄糖的作用是_________ ,亚甲基蓝的作用是_________ ;
(4)上述实验中葡萄糖也可用鲜橙汁(其中含丰富维生素C)代替,这是因为维生素C具有_____ ;
(5)该实验中③、④操作能否无限次重复进行_________ (填“能”或“不能”),理由是_____ 。
 。著名的蓝瓶子实验操作步骤如下:
。著名的蓝瓶子实验操作步骤如下:①如图示在250mL锥形瓶中,依次加入2g NaOH、100mL H2O和3g葡萄糖,搅拌溶解后,再加入3滴~5滴0.2%的亚甲基蓝溶液,振荡混合液呈现蓝色;
②塞紧橡皮塞(活塞a、b关闭),将溶液静置,溶液变为无色;
③再打开瓶塞,振荡,溶液又变为蓝色;
④再塞紧橡皮塞,将溶液静置,溶液又变为无色,以上③、④可重复多次。
试回答下列问题:

(1)某学生将起初配得的蓝色溶液分装在A,B两支试管中(如上图,A试管充满溶液,B中有少量溶液),塞上橡皮塞静置片刻,两溶液均显无色,若再同时振荡A,B试管,能显蓝色的是
(2)若塞紧锥形瓶塞并打开活塞a、b,通入足量氢气后,再关闭活塞a、b并振荡,溶液能否由无色变为蓝色
(3)上述转化过程中,葡萄糖的作用是
(4)上述实验中葡萄糖也可用鲜橙汁(其中含丰富维生素C)代替,这是因为维生素C具有
(5)该实验中③、④操作能否无限次重复进行
您最近一年使用:0次
2016-12-09更新
|
930次组卷
|
12卷引用:贵州省贞丰县第二中学2019-2020学年高二上学期期末考试化学试题
贵州省贞丰县第二中学2019-2020学年高二上学期期末考试化学试题(已下线)2011-2012学年浙江省北仑中学高二下学期期中考试化学试卷(已下线)2012年人教版高中化学选修6 1.1实验化学起步练习卷云南省广南二中2018-2019学年高二6月考试化学试题云南省盈江县第一高级中学2019-2020学年高二上学期期末考试化学试题云南省西双版纳傣族自治州勐腊县第一中学2019-2020学年高二上学期期末考试化学试题云南省丽江市永胜县第二中学2019—2020学年高二上学期期末考试化学试题贵州省三都水族自治县高级中学2019-2020学年高二上学期期末考试化学试题云南省曲靖市马龙区第二中学2019-2020学年高二上学期期末考试化学试题云南省曲靖市罗平县第三中学2019-2020学年高二上学期期末考试化学试题云南省寻甸县第五中学2019-2020学年高二上学期期末考试化学试题云南省勐腊县第二中学2019-2020学年高二上学期期末考试化学试题
11-12高一上·广西百色·阶段练习
7 . 按如图所示操作,充分反应后:

(1) I中铁丝上观察到的现象是______ ;反应的化学方程式为______ ;
(2) II中发生反应的化学方程式为______ ;
(3)结合I、II实验现象可知,Fe、Cu、Ag的还原性顺序为______ 。

(1) I中铁丝上观察到的现象是
(2) II中发生反应的化学方程式为
(3)结合I、II实验现象可知,Fe、Cu、Ag的还原性顺序为
您最近一年使用:0次




