名校
1 . 下列实验方案能计算出最终结果的是
| A.a g碳酸钠和碳酸氢钠混合物加热,充分反应后,剩余b g固体,计算碳酸钠的质量分数 |
B.1 L  的浓盐酸与足量 的浓盐酸与足量 充分反应,计算产生氯气的物质的量 充分反应,计算产生氯气的物质的量 |
| C.a g硝酸钠和氯化钠溶于水后加入足量硝酸银溶液,产生b g干燥的白色沉淀,计算硝酸钠的质量分数 |
| D.a g碳酸钠和氯化钠混合物完全溶于足量盐酸,将产生的气体通过碱石灰,碱石灰增重b g,计算碳酸钠的质量分数 |
您最近一年使用:0次
2022-11-29更新
|
115次组卷
|
2卷引用:河南省名校联盟2022-2023学年高一上学期期中考试化学试题
2 . 1.52g铜镁合金完全溶解于50mL密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法正确的是
| A.该浓硝酸中HNO3的物质的量浓度为14mol/L |
| B.该合金中铜与镁的物质的量之比为1:2 |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.得到2.54 g沉淀时,加入NaOH溶液的体积是600mL |
您最近一年使用:0次
2022-08-21更新
|
942次组卷
|
3卷引用:河南省信阳高级中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
3 . 下列实验操作分析或记录正确的是
| A.质量分数为98%的浓硫酸与等体积水混合后,硫酸的质量分数大于49% |
| B.用量筒测得排水法收集制得的氢气体积为50.28 mL |
| C.将11.7gNaCl固体溶于2 L水中,所得NaCl溶液物质的量浓度为0.1mol/L |
| D.配制480mL 0.2mol/LNaOH溶液,需称量NaOH固体的质量为4.0 g |
您最近一年使用:0次
2022-01-19更新
|
161次组卷
|
3卷引用:河南省周口恒大中学2023-2024学年高三上学期11月期中考试化学试题
名校
4 . 在一定条件下,使12g CO和 的混合气体充分反应,所得混合物在常温下跟足量的
的混合气体充分反应,所得混合物在常温下跟足量的 固体反应,结果固体增重7g,则原混合气体中
固体反应,结果固体增重7g,则原混合气体中 的质量分数可能是
的质量分数可能是
 的混合气体充分反应,所得混合物在常温下跟足量的
的混合气体充分反应,所得混合物在常温下跟足量的 固体反应,结果固体增重7g,则原混合气体中
固体反应,结果固体增重7g,则原混合气体中 的质量分数可能是
的质量分数可能是| A.33.3% | B.41.7% | C.58.3% | D.66.7% |
您最近一年使用:0次
2021-12-21更新
|
161次组卷
|
2卷引用:河南省南阳市2023-2024学年高一上学期10月月考化学试题
名校
解题方法
5 . 短周期主族元素a、b、c、d,原子序数依次增大,a与氢元素形成的一种二元化合物是常用的绿色氧化剂,c元素在地壳中含量排第三位,d最外层电子数是K层电子数的3倍。下列叙述不正确的是
| A.a和b形成的二元化合物只含离子键 | B.b不一定是金属元素 |
| C.c的最高价氧化物对应的水化物是强碱 | D.简单阴离子的还原性a<d |
您最近一年使用:0次
2023-03-20更新
|
143次组卷
|
4卷引用:河南省周口市太康县第一高级中学2023-2024学年高一上学期1月月考化学试题
6 . 某化学小组欲通过测定混合气体中 的含量来计算
的含量来计算 已变质的
已变质的 样品中
样品中 的含量。实验装置如下图(Q为弹性良好的气囊)。
的含量。实验装置如下图(Q为弹性良好的气囊)。
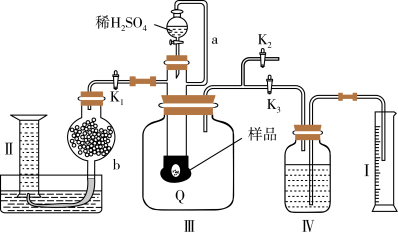
已知:①过氧化钠与硫酸反应的总化学方程式: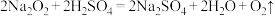 ;②忽略气体在II和IV中的溶解。
;②忽略气体在II和IV中的溶解。
下列分析错误的是
 的含量来计算
的含量来计算 已变质的
已变质的 样品中
样品中 的含量。实验装置如下图(Q为弹性良好的气囊)。
的含量。实验装置如下图(Q为弹性良好的气囊)。
已知:①过氧化钠与硫酸反应的总化学方程式:
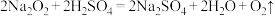 ;②忽略气体在II和IV中的溶解。
;②忽略气体在II和IV中的溶解。下列分析错误的是
A.b的作用是为了除去气体中的 ,故b中应装有碱石灰 ,故b中应装有碱石灰 |
B.测定气体总体积必须关闭 ,打开 ,打开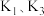 |
| C.量筒I用于测量产生气体的总体积,量筒II用于测量产生氧气的体积 |
D.若量筒II中产生的气体经过换算后为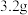 ,则 ,则 已变质的 已变质的 样品中 样品中 的质量为 的质量为 |
您最近一年使用:0次
解题方法
7 . X、Y、Z、M是原子序数依次增大的短周期主族元素,Y的最外层电子数是内层电子数的3倍,Y与Z形成的化合物Z2Y3中,元素质量比m(Y):m(Z)=8:9;X原子的最外层电子数为M原子和Z原子最外层电子数的和的一半。下列说法正确的是
| A.X的最高价氧化物对应的水化物一定为强酸 | B.气态氢化物的沸点:Y>M |
| C.Z是地壳中含量最多的元素 | D.原子半径:Z>M>X>Y |
您最近一年使用:0次
2020-07-16更新
|
121次组卷
|
2卷引用:河南省南阳市2022-2023学年高一下学期期末考试化学试题



