名校
1 . 已知: ,若
,若 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 ,若
,若 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.10g质量分数为28%的NaOH溶液中含氢原子数目为 |
B.0.1 mol/L NaCN溶液中含阴离子总数大于 |
C.当生成1 mol NaSCN消耗11.2 L  |
D.相同温度下,相同体积的两个容器中,加入等质量的 和 和 ,则两个容器内的压强之比为3:2 ,则两个容器内的压强之比为3:2 |
您最近一年使用:0次
名校
2 . 标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为w,物质的量浓度为cmol/L,则下列关系中错误的是
A.ρ=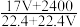 | B.w=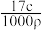 |
C.w=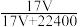 | D.w=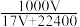 |
您最近一年使用:0次
2023-11-12更新
|
257次组卷
|
2卷引用:上海市上海中学2023-2024学年高一上学期10月月考化学试题
3 . 石灰氮是由Ca、N、C等三种元素组成的盐,其含钙、碳的质量分数分别为50%、l5%。①石灰氮完全水解的产物是A和B,其中B可方便地制成一种氮肥;②A在高温下分解生成C和D,通常状况下,C为气体;③B的催化氧化产物为E和F;④E遇到D生成唯一产物G,G与C反应重新生成A和E;⑤F再被氧气氧化后的产物遇到E可制备常用的一种强酸H;⑥B、C、E混合反应生成一种常用的氮肥I。以下有关叙述中正确的是
| A.石灰氮是化学式为Ca(CN)2 |
| B.②、⑤、⑥为有关工业生产过程的反应原理 |
| C.1molB经过催化氧化生成E和F的过程中有3mol电子发生转移 |
| D.足量B和C与饱和氯化钠溶液反应可以制得发酵粉的一种主要成分 |
您最近一年使用:0次
4 . 已知A、B、C、D、E、F、G是七种原子序数依次增大的短周期元素,它们的原子结构特征或有关物质的性质等如下表所示。
(1)这七种元素中,金属元素的有
(2)上表的A、B、C三种元素中,正确的说法是
(3)上表的D、E、F、G中,正确的说法是
| 元素 | 原子结构特征或有关物质的性质 |
| A | 原子的最外层电子数是其内层电子数的2倍 |
| B | 其单质是空气中含量最多的物质 |
| C | 原子的最外层电子数是其电子层数的4倍 |
| D | 位于第ⅡA族,其原子半径比E的大 |
| E | 是金属元素,其氧化物和氢氧化物都有两性,且与D在同一周期 |
| F | 原子序数16,其单质在通常状况下为固体 |
| G | 原子的最外层电子数比其次外层电子数少1个 |
| A.1种 | B.2种 | C.3种 | D.4种 |
| A.元素A的原子半径小于元素B |
| B.元素C的性质最稳定 |
| C.元素A的非金属性比元素B强 |
| D.其中某元素的化合价为+6 |
| A.原子半径最小的是G |
| B.G的氧化物对应水化物的酸性比F的强 |
| C.与相同浓度的盐酸反应时,D比E更剧烈 |
| D.D的最高价氧化物对应的水化物易溶于水 |
您最近一年使用:0次
2010·上海·零模
解题方法
5 . 某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等)( )
则下列分析推理中不正确的是 ( )
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
| m(混合物) | 9.2 g | 15.7 g | 27.6 g |
| V(CO2)(标况) | 2.24 L | 3.36 L | 3.36 L |
则下列分析推理中不正确的是 ( )
| A.根据表中数据不能计算出混合物中NaHCO3的质量分数 |
| B.加入混合物9.2 g时盐酸过量质量分数 |
| C.盐酸的物质的量浓度为3.0 mol·L-1 |
| D.15.7 g混合物恰好与盐酸完全反应 |
您最近一年使用:0次
12-13高三上·上海徐汇·期末
解题方法
6 . 有a克Na2CO3和NaHCO3混合物,下列实验方案中可测定其中Na2CO3质量分数的是
| A.将混合物与足量稀盐酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| B.将混合物充分加热,减重b克 |
| C.将混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
| D.将混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
您最近一年使用:0次
解题方法
7 . 为了测定某镁铝合金的成分,取14.7 g合金完全溶于500 mL 3 mol/L的硫酸中,再加入400 mL 8 mol/L的氢氧化钠溶液充分反应,最后只产生一种沉淀。则关于该合金的测定过程的描述正确的是
| A.该合金中含有铝的质量至少为5.4 g |
| B.合金中镁的质量分数为63.3%≤Mg%<100% |
| C.在产生沉淀后的溶液中一定含有0.2 mol NaAlO2 |
| D.在产生沉淀后的溶液中有1.5 mol Na2SO4 |
您最近一年使用:0次
10-11高三上·上海嘉定·期末
解题方法
8 . 在t℃将ag NH3完全溶于水,得到V mL溶液,假如该溶液的密度为dg/cm3,质量分数为w,其中含NH4+的物质的量为b mol。下列叙述正确的是
A.溶质的质量分数为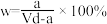 |
| B.溶质的物质的量浓度为1000a/17V mol·L-1 |
C.溶液中c(OH-)=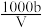 mol·L-1 + c(H+) mol·L-1 + c(H+) |
| D.上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5w |
您最近一年使用:0次
解题方法
9 . NO、NO2可被氨水溶液吸收(6NO+ 4NH3→5N2+6H2O;6NO2+ 8NH3→7N2+12H2O)。现有NO与NO2(不含N2O4)混合气体90mol被30%的氨水4.45×103g完全吸收,产生78mol氮气。吸收后氨水密度为0.980 g/cm3。则
| A.原混合气体的平均组成为NO1.1 | B.原氨水的浓度约为17.3mol/L |
| C.吸收后氨水的浓度约为2.4mol/L | D.吸收后氨水的质量分数约为0.5 |
您最近一年使用:0次
解题方法
10 . 能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的实验方案是
| A.取a克混合物充分加热至质量不变,减重b克 |
| B.取a克混合物与足量稀硝酸充分反应,加热、蒸干、灼烧至熔化,冷却得b克固体 |
| C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰完全吸收,增重b克 |
| D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
您最近一年使用:0次
2020-03-21更新
|
87次组卷
|
2卷引用:上海市普陀区2016届高三上学期12月教学质量调研化学试题



