名校
1 . 下列有关物质的性质与用途具有对应关系的是
A.镁可以和 反应,可用于制造信号弹和焰火 反应,可用于制造信号弹和焰火 |
B.纳米 能与酸反应,可用作铁磁性材料 能与酸反应,可用作铁磁性材料 |
| C.锂单质较钠活泼,可用于制造锂离子电池 |
D.无水 呈蓝色,吸水后为粉红色[ 呈蓝色,吸水后为粉红色[ ],可用于制造变色硅胶(干燥剂) ],可用于制造变色硅胶(干燥剂) |
您最近一年使用:0次
2022-08-08更新
|
1136次组卷
|
4卷引用:江西省南昌市第十九中学2022-2023学年高三上学期(10月)第三次月考化学试卷
江西省南昌市第十九中学2022-2023学年高三上学期(10月)第三次月考化学试卷广东省六校2023届高三第一次联考化学试题广东省广州市六校2023届高三上学期8月第一次联考化学试题(已下线)专题六 金属元素及其化合物-实战高考·二轮复习核心突破
2 . 亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
(1)从物质分类角度来看, 是
是___________ (填序号)。
a.酸 b.盐 c.碱 d.非电解质 e.电解质
(2)由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下,配平该化学方程式:
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下,配平该化学方程式:___________

(3)用上述反应来处理 并不是最佳方法,其原因是
并不是最佳方法,其原因是___________ 。
(4)误食 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出
表现出___________ (填“氧化性”或“还原性”)。
(5)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:___________ 。
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。(1)从物质分类角度来看,
 是
是a.酸 b.盐 c.碱 d.非电解质 e.电解质
(2)由于
 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下,配平该化学方程式:
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下,配平该化学方程式:
(3)用上述反应来处理
 并不是最佳方法,其原因是
并不是最佳方法,其原因是(4)误食
 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出
表现出(5)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:
您最近一年使用:0次
3 . 钠和氯的化合物与生活密切相关,下列物质与其用途不符合的是
| A.小苏打用作制作馒头和面包的膨松剂 |
| B.漂白粉用作洪水过后环境的消毒剂 |
| C.次氯酸用作棉、麻和纸张的漂白剂 |
| D.纯碱用于治疗胃酸过多 |
您最近一年使用:0次
2023-10-05更新
|
34次组卷
|
2卷引用:江西省南昌市第一中学2022-2023学年高一上学期11月期中考试化学试题
解题方法
4 . 下表中物质的用途与所对应性质相符的是
| 选项 | 物质 | 用途 | 性质 |
| A | 铁、铬(18%)、镍(8%)合金 | 制作医疗器材、厨具 | 不易生锈 |
| B | FeCl3 | 可用于腐蚀印刷电路板上的Cu | FeCl3溶液具有酸性 |
| C | SiO2 | 可用于制备光导纤维 | SiO2硬度大 |
| D | Al(OH)3 | 可用于中和过多的胃酸 | 氢氧化铝受热分解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 三氯化碘(ICl3)在药物合成中用途非常广泛,其熔点为33℃,沸点为73℃,氯气与单质碘需在温度稍低于70℃下反应制备ICl3,实验室制备如图所示。下列说法正确的是

| A.装置A可选用的药品为高锰酸钾与浓盐酸 |
| B.装置B的作用是除杂,也作安全瓶,在本实验中可以和装置C互换位置 |
| C.装置C中的硅胶可用浓硫酸代替 |
| D.装置D最恰当的加热方式是用酒精灯先预热再集中加热 |
您最近一年使用:0次
2022-05-24更新
|
968次组卷
|
7卷引用:江西省南昌市第十九中学2022-2023学年高三上学期(11月)第四次月考化学试卷
江西省南昌市第十九中学2022-2023学年高三上学期(11月)第四次月考化学试卷 广东省汕头市2022届高三下学期第三次模拟考试化学试题(已下线)专题11 化学实验基础-2022年高考真题模拟题分项汇编(已下线)第12讲 富集在海水中的元素——卤素(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)2022年江苏卷高考真题变式题1-13广东省仲元中学2023-2024学年高三上学期模拟测试(一)化学试题重庆市荣昌中学校2023-2024学年高三下学期开学考试化学试题
6 . 在生产生活中,卤族元素(F、Cl、Br、I)的单质及化合物用途广泛。
(1)氯元素在周期表中的位置为_______ 。
(2)下列说法中正确的是_______
(3)已知:ICl(氯化碘)是红棕色液体,易水解。ICl 的水解反应方程式是_______ 。
(4)工业氢溴酸常带有淡淡的黄色,可能的原因是:①含 Fe3+,②含 Br2,③含 Fe3+和 Br2,只用下列一种试剂就能分析产生淡黄色的原因,该试剂是 _______(填写字母)。
(1)氯元素在周期表中的位置为
(2)下列说法中正确的是_______
| A.XeF2 分子中各原子最外层均满足 8e-结构 |
| B.食用碘盐中添加了 KIO3 |
| C.氟元素的非金属性强于氯元素,故氢氟酸的酸性强于盐酸 |
| D.还原性:Br->I- |
(4)工业氢溴酸常带有淡淡的黄色,可能的原因是:①含 Fe3+,②含 Br2,③含 Fe3+和 Br2,只用下列一种试剂就能分析产生淡黄色的原因,该试剂是 _______(填写字母)。
| A.KMnO4 溶液 | B.KSCN 溶液 | C.淀粉 KI 溶液 | D.CCl4 |
您最近一年使用:0次
名校
解题方法
7 . 铁元素是人体中含量最高的生命必需微量元素,承担着极其重要的生理功能.在日常生活中,常见的食品抗氧化剂主要活性成分为铁粉,脱氧过程中的一步主要反应为4Fe(OH)2+O2+2H2O=4Fe(OH)3(红褐色固体)。工业上高铁酸盐在能源、环保等方面有着广泛的用途,湿法制备高铁酸盐的原理为3ClO-+10OH-+2Fe3+=2FeO +3Cl-+5H2O。根据以上信息,回答以下问题:
+3Cl-+5H2O。根据以上信息,回答以下问题:
(1)高铁酸根离子(FeO )中铁元素的化合价为
)中铁元素的化合价为____ ;湿法制备高铁酸盐的反应中,氧化剂是___ ,被氧化的元素是____ (填元素名称)。消耗1mol还原剂转移电子的物质的量为___ 。
(2)某化学小组用食品抗氧化剂(成分为铁粉、活性炭、氯化钠)进行以下实验。
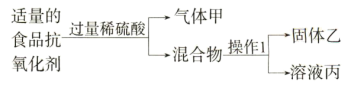
①操作1名称是____ ,溶液丙中一定含有的金属阳离子是____ 。
将乙烘干后,用乙的氧化物进行以下实验,物质之间的转化关系如图所示:(反应条件及部分产物略去)
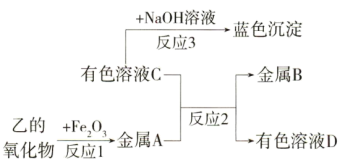
②写出反应1的化学方程式,并用单线桥标出电子转移的方向及数目:____ 。
③反应3的离子方程式为_____ 。
 +3Cl-+5H2O。根据以上信息,回答以下问题:
+3Cl-+5H2O。根据以上信息,回答以下问题:(1)高铁酸根离子(FeO
 )中铁元素的化合价为
)中铁元素的化合价为(2)某化学小组用食品抗氧化剂(成分为铁粉、活性炭、氯化钠)进行以下实验。

①操作1名称是
将乙烘干后,用乙的氧化物进行以下实验,物质之间的转化关系如图所示:(反应条件及部分产物略去)

②写出反应1的化学方程式,并用单线桥标出电子转移的方向及数目:
③反应3的离子方程式为
您最近一年使用:0次
2022-08-17更新
|
500次组卷
|
4卷引用:江西省南昌市豫章中学20212-2022学年高一下学期第一次月考化学试题



