1 . 某校化学兴趣小组为研究 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
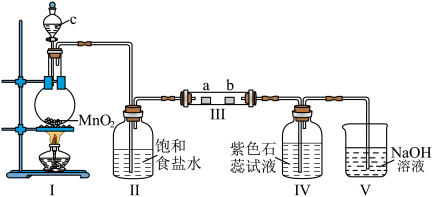
(1)装置Ⅰ中仪器c的名称是___________ ,实验室以二氧化锰和浓盐酸制备氯气的离子方程式为___________ 。
(2)装置Ⅱ中的试剂为___________ ,作用是___________ 。
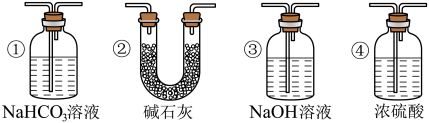
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加下图中的___________ (填序号)。
(4)若产生 足量,实验过程中装置Ⅳ中的实验现象为
足量,实验过程中装置Ⅳ中的实验现象为___________ 。
(5)写出装置Ⅴ中发生的离子方程式___________ 。
 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ中的试剂为
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加下图中的

(4)若产生
 足量,实验过程中装置Ⅳ中的实验现象为
足量,实验过程中装置Ⅳ中的实验现象为(5)写出装置Ⅴ中发生的离子方程式
您最近一年使用:0次
2 . 实验表明,在如图装置中,带负电荷的胶粒向Pt(铂)极迁移,带正电荷的胶粒向石墨(C)极迁移,这种现象叫“电泳现象”。某小组制备AgI胶体并探究其性质,有关信息如表所示(注明:AgI胶体呈黄色)

下列推断正确的是

| 操作 | 化学反应现象 | 电泳实验现象 |
 | 产生黄色液体 | 石墨极附近颜色变深,铂极附近颜色变浅 |
 | 产生黄色液体 | 铂极附近颜色变深,石墨极附近颜色变浅 |
| A.用丁达尔效应可以确定①、②试管里的液体是否是胶体 |
| B.①和②试管中都发生了氧化还原反应 |
| C.①试管制备的碘化银胶体带正电荷 |
| D.碘化银胶粒带电性与加入试剂顺序有关 |
您最近一年使用:0次
2023-02-08更新
|
229次组卷
|
4卷引用:江西省南昌市2022-2023学年高一上学期11月期中化学试题
3 . 下列实验方案不能完成“实验目的”的是
| 选项 | 实验目的 | 实验方案 |
| A | 确认 胶体是否制备成功 胶体是否制备成功 | 用可见光束照射 |
| B | 确认金属活泼性:Na>Cu | 将金属钠投入 溶液中 溶液中 |
| C | 证明非金属性:N>C | 向碳酸钙中滴加稀硝酸 |
| D | 证明 具有还原性 具有还原性 | 向NaI淀粉溶液中滴入少量氯水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 用下列实验装置进行相应实验,能达到实验目的的是
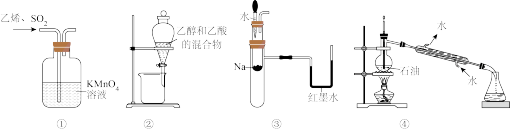

| A.用装置①除去C2H4中少量SO2 | B.用装置②分离乙醇和乙酸的混合物 |
| C.用装置③验证Na和水反应为放热反应 | D.用装置④分馏石油并收集60~ 150℃馏分 |
您最近一年使用:0次
2020-07-18更新
|
380次组卷
|
6卷引用:江西省南昌市八一中学2021-2022学年高一下学期复学摸底考试化学试题
名校
解题方法
5 . 如图所示是一个制取 并以
并以 为原料进行特定反应的装置,多余的
为原料进行特定反应的装置,多余的 可以贮存在
可以贮存在 瓶中,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(淀粉-KI溶液)、D(水)、F(紫色石蕊试液)。
瓶中,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(淀粉-KI溶液)、D(水)、F(紫色石蕊试液)。 烧瓶中的固体为
烧瓶中的固体为 ,液体为浓盐酸,则其发生反应的化学方程式为
,液体为浓盐酸,则其发生反应的化学方程式为___________
(2) 中的现象为
中的现象为___________ ,发生反应的离子方程式___________ 。
(3)装置 中硬质玻璃管内盛有炭粉,若
中硬质玻璃管内盛有炭粉,若 中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出
中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出 中反应的化学方程式:
中反应的化学方程式:___________ 。
(4)D中溶液的存在微粒有___________ (填化学式)。
(5)在F中紫色石蕊试液的颜色变化是___________ 。
(6)G中应盛放___________ 溶液。
 并以
并以 为原料进行特定反应的装置,多余的
为原料进行特定反应的装置,多余的 可以贮存在
可以贮存在 瓶中,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(淀粉-KI溶液)、D(水)、F(紫色石蕊试液)。
瓶中,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(淀粉-KI溶液)、D(水)、F(紫色石蕊试液)。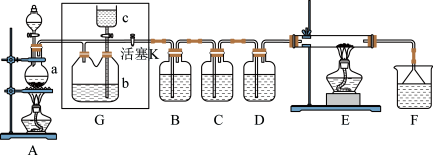
 烧瓶中的固体为
烧瓶中的固体为 ,液体为浓盐酸,则其发生反应的化学方程式为
,液体为浓盐酸,则其发生反应的化学方程式为(2)
 中的现象为
中的现象为(3)装置
 中硬质玻璃管内盛有炭粉,若
中硬质玻璃管内盛有炭粉,若 中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出
中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出 中反应的化学方程式:
中反应的化学方程式:(4)D中溶液的存在微粒有
(5)在F中紫色石蕊试液的颜色变化是
(6)G中应盛放
您最近一年使用:0次
名校
解题方法
6 . 化学兴趣小组在学习钠盐时,查阅到了以下学习资料,
资料一:金属钠在工业上可用电解熔融氯化钠法制备:2NaCl(熔融) 2Na+Cl2↑
2Na+Cl2↑
资料二:铋(Bi)元素价态为+3时较稳定,铋酸钠(NaBiO3)溶液呈无色。取一定量的硫酸锰(MnSO4)溶液,向其中依次滴加下列溶液,对应的现象如下表所示:
根据该兴趣小组提供的资料分析,下列说法正确的是
资料一:金属钠在工业上可用电解熔融氯化钠法制备:2NaCl(熔融)
 2Na+Cl2↑
2Na+Cl2↑资料二:铋(Bi)元素价态为+3时较稳定,铋酸钠(NaBiO3)溶液呈无色。取一定量的硫酸锰(MnSO4)溶液,向其中依次滴加下列溶液,对应的现象如下表所示:
| 加入溶液 | ①适量铋酸钠溶液 | ②过量的双氧水(H2O2) | ③适量KI-淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 得到蓝色溶液 |
| A.由资料一可得氧化性Na+>Cl2 |
| B.实验②中双氧水做氧化剂 |
| C.NaBiO3不能使KI-淀粉溶液变成蓝色 |
| D.氧化性:NaBiO3>KMnO4>H2O2 |
您最近一年使用:0次
2023-09-22更新
|
126次组卷
|
2卷引用:江西省南昌第二中学2022-2023学年高一上学期第一次月考化学试题
7 . 氯及其化合物既是重要化工原料,又是高效、广谱消毒剂。
(1)氯气是一种色的气体,氯气与水反应的离子方程式为___________ 。
(2)漂白粉是常见的消毒剂,写出工业制取漂白粉的化学方程式:___________ 。
(3)二氧化氯( )是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂。制备
)是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂。制备 的方法是用
的方法是用 通入
通入 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为___________ ; 在杀菌消毒过程中会产生副产物亚氯酸盐(
在杀菌消毒过程中会产生副产物亚氯酸盐( ),需将其转化为
),需将其转化为 除去。下列试剂中,可将
除去。下列试剂中,可将 转化为
转化为 的是
的是___________ (填序号)。
a. b.
b. c.
c. d.
d.
(4)某同学设计实验探究84消毒液的漂白性。
Ⅰ.在2mL 84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL 84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。
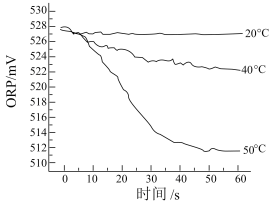
已知:ORP表示水溶液中物质的氧化性或还原性强弱。ORP值越大,氧化性越强。
①实验Ⅰ、Ⅱ现象不同的原因是___________ 。
②实验Ⅲ中,随时间的变化ORP值不同的原因可能是___________ 。
③针对不同物品的消毒,需将84消毒液稀释到不同的浓度。已知某品牌84消毒液中次氯酸钠的质量分数为12.6%,若取该消毒液100g,加水稀释为8%的溶液,则需加水的质量为___________ g。
(1)氯气是一种色的气体,氯气与水反应的离子方程式为
(2)漂白粉是常见的消毒剂,写出工业制取漂白粉的化学方程式:
(3)二氧化氯(
 )是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂。制备
)是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂。制备 的方法是用
的方法是用 通入
通入 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为 在杀菌消毒过程中会产生副产物亚氯酸盐(
在杀菌消毒过程中会产生副产物亚氯酸盐( ),需将其转化为
),需将其转化为 除去。下列试剂中,可将
除去。下列试剂中,可将 转化为
转化为 的是
的是a.
 b.
b. c.
c. d.
d.
(4)某同学设计实验探究84消毒液的漂白性。
Ⅰ.在2mL 84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL 84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。

已知:ORP表示水溶液中物质的氧化性或还原性强弱。ORP值越大,氧化性越强。
①实验Ⅰ、Ⅱ现象不同的原因是
②实验Ⅲ中,随时间的变化ORP值不同的原因可能是
③针对不同物品的消毒,需将84消毒液稀释到不同的浓度。已知某品牌84消毒液中次氯酸钠的质量分数为12.6%,若取该消毒液100g,加水稀释为8%的溶液,则需加水的质量为
您最近一年使用:0次
解题方法
8 . 已知FeCl3固体易升华,其蒸气为黄色。某学习小组通过下列装置探究MnO2与 FeCl3能否反应产生Cl2,实验装置如图。
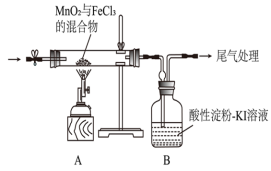
回答下列问题:
(1)装置A中产生黄色气体不能说明一定产生Cl2,原因为 _______ 。
(2)除了生成的Cl2可使B中溶液变蓝外,推测还有两种可能。
①推测一:装置A中产生的另一种黄色气体也可使B中溶液变蓝,发生反应的离子方程式为_______ 。为排除该气体的影响,可将装置进行改进,改进的措施为_______ 。
②推测二:在酸性条件下,装置中的空气可使B中溶液变蓝,发生反应的离子方程式为_______ 。为排除空气的影响,可在开始加热A装置前,_______ 。
(3)按照上述方法改进再进行实验,观察到装置A中产生黄色气体,装置B中溶液变蓝,则A中发生反应的化学方程式为_______ 。

回答下列问题:
| 实验操作 | 现象 |
| 点燃酒精喷灯,加热 | 加热一段时间后,装置A中产生黄色气体,装置B中溶液变蓝 |
(2)除了生成的Cl2可使B中溶液变蓝外,推测还有两种可能。
①推测一:装置A中产生的另一种黄色气体也可使B中溶液变蓝,发生反应的离子方程式为
②推测二:在酸性条件下,装置中的空气可使B中溶液变蓝,发生反应的离子方程式为
(3)按照上述方法改进再进行实验,观察到装置A中产生黄色气体,装置B中溶液变蓝,则A中发生反应的化学方程式为
您最近一年使用:0次
9 . 某研究小组利用如下浓盐酸仪器,用氯气与NaOH溶液冰水浴制备NaClO溶液。请回答下列问题:

(1)①中产生氯气的离子方程式为___________ 。
(2)②的作用___________ 。
(3)制备NaClO溶液,仪器的连接顺序为a___________ (填字母),化学方程式为___________ 。
(4)取③中溶液滴加品红试剂发现褪色,设计实验探究溶液褪色的原因。
i.a=___________ 。
ii.由实验Ⅱ得出的结论是___________ 。
iii.由上述实验得出的结论是:随NaOH溶液增多,NaClO___________ 。

(1)①中产生氯气的离子方程式为
(2)②的作用
(3)制备NaClO溶液,仪器的连接顺序为a
(4)取③中溶液滴加品红试剂发现褪色,设计实验探究溶液褪色的原因。
| 序号 | 0.1 mol/LNaClO溶液/mL | 0.1 mol/LNaCl溶液/mL | 0.1 mol/LNaOH溶液/mL | H2O/mL | 品红溶液 | 现象 |
| Ⅰ | 5.0 | 0 | 0 | 5.0 | 3滴 | 较快褪色 |
| Ⅱ | 0 | 5.0 | a | 0 | 3滴 | 不褪色 |
| Ⅲ | 5.0 | 0 | 5.0 | 0 | 3滴 | 缓慢褪色 |
ii.由实验Ⅱ得出的结论是
iii.由上述实验得出的结论是:随NaOH溶液增多,NaClO
您最近一年使用:0次
名校
解题方法
10 . 实验室以锈蚀程度很大的废铁屑为原料制备 晶体的流程如下:
晶体的流程如下: 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀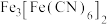 。回答下列问题:
。回答下列问题:
(1)“酸溶”过程中发生的主要反应有:① ;
;
②___________ (用离子方程式表示)
③___________ (用离子方程式表示)
(2)“酸溶”需控制温度在 左右,最佳的加热方式为
左右,最佳的加热方式为___________ 。
(3)“过滤”需要的玻璃仪器除烧杯外还有___________ 。
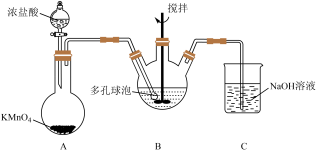
(4)“氧化”过程可在下图所示装置中进行。___________ 。
②装置 中发生的反应离子方程式为
中发生的反应离子方程式为___________ 。
③B中使用多孔球泡的作用是___________ 。
④证明装置 溶液中
溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是___________ 。
 晶体的流程如下:
晶体的流程如下:
 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀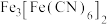 。回答下列问题:
。回答下列问题:(1)“酸溶”过程中发生的主要反应有:①
 ;
;②
③
(2)“酸溶”需控制温度在
 左右,最佳的加热方式为
左右,最佳的加热方式为(3)“过滤”需要的玻璃仪器除烧杯外还有
(4)“氧化”过程可在下图所示装置中进行。
②装置
 中发生的反应离子方程式为
中发生的反应离子方程式为③B中使用多孔球泡的作用是
④证明装置
 溶液中
溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是
您最近一年使用:0次



