名校
解题方法
1 . 实验室中用质量分数98%、密度为1.84g/mL的浓硫酸配制0.2mol•L-1的稀硫酸溶液950mL,下列说法不正确的是
| A.所用容量瓶的规格和用量筒量取浓硫酸的体积分别为:1000mL;10.87mL |
| B.量取浓硫酸时俯视量筒刻度线会使配制溶液的浓度偏低 |
| C.应先在容量瓶中加入一定量蒸馏水再将量取的浓硫酸缓慢加入容量瓶 |
| D.除容量瓶外还需15mL量筒、玻璃棒、烧杯、胶头滴管即可完成配制 |
您最近一年使用:0次
名校
2 . 回答下列问题。
Ⅰ.新型冠状病毒肺炎疫情在全球多地爆发,“84消毒液”是大规模环境消毒剂。已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
(1)该“84消毒液”的物质的量浓度约为___________  。(保留一位小数)
。(保留一位小数)
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。回答下列问题。
①配制一定物质的量浓度的上述消毒液需要选用如图所示的部分仪器,还需要的玻璃仪器是___________ (填仪器名称)

②若需配置质量分数为20%的NaClO消毒液,除需要托盘天平、药匙、玻璃棒、烧杯、胶头滴管外,还缺少的仪器是___________ 。
(3)请将下列各操作按正确的顺序将字母代号填写在横线上___________ 。
A.用托盘天平称取NaClO固体
B.塞好瓶塞,反复颠倒摇匀,装瓶,贴标签
C.加蒸馏水至离容量瓶瓶颈刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至刻度线
D.用适量蒸馏水洗涤烧杯、玻璃棒2~3次,洗涤液一并转入容量瓶,并轻摇容量瓶使其混匀
E.待溶液冷却至室温,再将溶液转入容量瓶
F.将已称量的NaClO固体置于烧杯中,加适量蒸馏水溶解完全
(4)若所配制的次氯酸钠溶液的物质的量浓度偏小,则下列可能的原因分析中正确的是___________。
(5)某工厂将氯气通入到40%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1000kg该溶液需消耗氯气的质量为___________ kg(保留整数)。
Ⅰ.新型冠状病毒肺炎疫情在全球多地爆发,“84消毒液”是大规模环境消毒剂。已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
| 84消毒液 (有效成分)NaClO (规格)1000mL (质量分数)25% (密度) 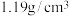 |
 。(保留一位小数)
。(保留一位小数)(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。回答下列问题。
①配制一定物质的量浓度的上述消毒液需要选用如图所示的部分仪器,还需要的玻璃仪器是

②若需配置质量分数为20%的NaClO消毒液,除需要托盘天平、药匙、玻璃棒、烧杯、胶头滴管外,还缺少的仪器是
(3)请将下列各操作按正确的顺序将字母代号填写在横线上
A.用托盘天平称取NaClO固体
B.塞好瓶塞,反复颠倒摇匀,装瓶,贴标签
C.加蒸馏水至离容量瓶瓶颈刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至刻度线
D.用适量蒸馏水洗涤烧杯、玻璃棒2~3次,洗涤液一并转入容量瓶,并轻摇容量瓶使其混匀
E.待溶液冷却至室温,再将溶液转入容量瓶
F.将已称量的NaClO固体置于烧杯中,加适量蒸馏水溶解完全
(4)若所配制的次氯酸钠溶液的物质的量浓度偏小,则下列可能的原因分析中正确的是___________。
| A.配制前,容量瓶中有少量蒸馏水 | B.洗涤液未转移到容量瓶中 |
| C.未经冷却立即转液 | D.定容时,仰视溶液的凹液面 |
您最近一年使用:0次
3 . 氯及其化合物既是重要化工原料,又是高效、广谱消毒剂。
(1)氯气是一种色的气体,氯气与水反应的离子方程式为___________ 。
(2)漂白粉是常见的消毒剂,写出工业制取漂白粉的化学方程式:___________ 。
(3)二氧化氯( )是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂。制备
)是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂。制备 的方法是用
的方法是用 通入
通入 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为___________ ; 在杀菌消毒过程中会产生副产物亚氯酸盐(
在杀菌消毒过程中会产生副产物亚氯酸盐( ),需将其转化为
),需将其转化为 除去。下列试剂中,可将
除去。下列试剂中,可将 转化为
转化为 的是
的是___________ (填序号)。
a. b.
b. c.
c. d.
d.
(4)某同学设计实验探究84消毒液的漂白性。
Ⅰ.在2mL 84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL 84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。
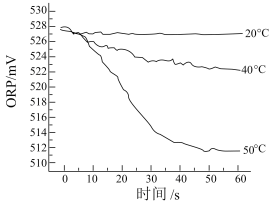
已知:ORP表示水溶液中物质的氧化性或还原性强弱。ORP值越大,氧化性越强。
①实验Ⅰ、Ⅱ现象不同的原因是___________ 。
②实验Ⅲ中,随时间的变化ORP值不同的原因可能是___________ 。
③针对不同物品的消毒,需将84消毒液稀释到不同的浓度。已知某品牌84消毒液中次氯酸钠的质量分数为12.6%,若取该消毒液100g,加水稀释为8%的溶液,则需加水的质量为___________ g。
(1)氯气是一种色的气体,氯气与水反应的离子方程式为
(2)漂白粉是常见的消毒剂,写出工业制取漂白粉的化学方程式:
(3)二氧化氯(
 )是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂。制备
)是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂。制备 的方法是用
的方法是用 通入
通入 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为 在杀菌消毒过程中会产生副产物亚氯酸盐(
在杀菌消毒过程中会产生副产物亚氯酸盐( ),需将其转化为
),需将其转化为 除去。下列试剂中,可将
除去。下列试剂中,可将 转化为
转化为 的是
的是a.
 b.
b. c.
c. d.
d.
(4)某同学设计实验探究84消毒液的漂白性。
Ⅰ.在2mL 84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.在2mL 84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。

已知:ORP表示水溶液中物质的氧化性或还原性强弱。ORP值越大,氧化性越强。
①实验Ⅰ、Ⅱ现象不同的原因是
②实验Ⅲ中,随时间的变化ORP值不同的原因可能是
③针对不同物品的消毒,需将84消毒液稀释到不同的浓度。已知某品牌84消毒液中次氯酸钠的质量分数为12.6%,若取该消毒液100g,加水稀释为8%的溶液,则需加水的质量为
您最近一年使用:0次
名校
解题方法
4 . Co(OH)2在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,取400℃时的产物(其中Co的化合价为+2,+3),用500mL5.1mol·L-1盐酸将其恰好完全溶解,得到CoCl2溶液和4.48L(标准状况)黄绿色气体。下列说法错误的是
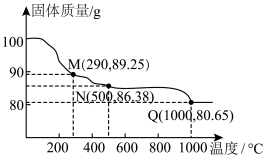

A.290℃时,固体的成分仅有 |
B.400℃时,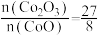 |
| C.500℃时,固体中氧元素总质量分数约为26.6% |
| D.生成的黄绿色气体可用于工业上生产“84”消毒液 |
您最近一年使用:0次
2022-07-03更新
|
549次组卷
|
4卷引用:江西省南昌市第二中学2022-2023学年高三上学期第三次考试化学试题
江西省南昌市第二中学2022-2023学年高三上学期第三次考试化学试题河北省保定市2021-2022学年高二下学期期末考试化学试题山西省长治市2021-2022学年高二下学期期末联考化学试题(已下线)2022年福建省高考真题变式题(选择题6-10)
名校
解题方法
5 . 下列实验基本操作正确的是
| A.用苯萃取碘水中的碘单质,分液时应先放出有机相,再放出无机相 |
| B.提取海带中碘元素时,为保证I-完全氧化为I2,加入的氯水应过量 |
| C.配制质量分数10%的CuSO4溶液:称取5.0 g 胆矾,加入27.0 g水,搅拌溶解 |
| D.蒸馏开始时先开冷凝水,再开加热器;结束时先关冷凝水,再关加热器 |
您最近一年使用:0次
2022-08-20更新
|
635次组卷
|
2卷引用:江西省南昌市第十九中学2022-2023学年高三上学期(10月)第三次月考化学试卷
名校
6 . 氮元素在海洋中的循环,是整个海洋生态系统的基础和关键,海洋中无机氮的循环过程可用下图表示。下列关于海洋氮循环的说法不正确的是
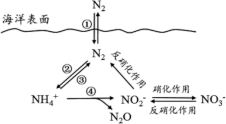
| A.海洋中的氮循环起始于氮的氧化 |
| B.氮循环中涉及氮的固定 |
C.向海洋排放含NO 的废水会影响海洋中NH 的废水会影响海洋中NH 的含量 的含量 |
| D.“硝化作用”可能有氧气的参与 |
您最近一年使用:0次
名校
解题方法
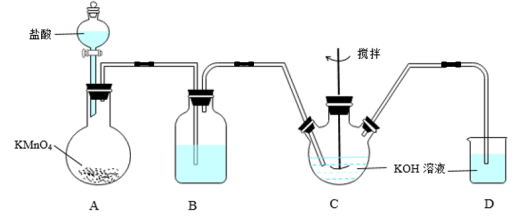
7 . 高铁酸钾(K2FeO4)是一种新型,高效、多功能绿色水处理剂,可通过KClO溶液与Fe(NO3)3溶液的反应制备。已知:①KClO在较高温度下发生歧化反应生成KClO3。②K2FeO4具有下列性质:可溶于水、微溶于浓KOH溶液;在强碱性溶液中比较稳定;在Fe3+催化作用下发生分解,在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2,如图所示是实验室模拟工业制备KClO溶液装置。______ ;
(2)反应时需将C装置置于冷水浴中,其原因为______ ;
(3)制备K2FeO4时,不能将碱性的KClO溶液滴加到Fe(NO3)3饱和溶液中,其原因是______ ,制备K2FeO4的离子方程式______ ;
(4)工业上常用废铁屑为原料制备Fe(NO3)3溶液,检验Fe3+所需试剂名称______ ,其反应原理为______ (用离子方程式表示);
(5)向反应后的三颈瓶中加入饱和KOH溶液,析出K2FeO4固体,过滤、洗涤、干燥。洗涤操作所用最佳试剂为______ ;
A.水 B.无水乙醇 C.稀KOH溶液
(6)工业上用“间接碘量法”测定高铁酸钾的纯度:用碱性KI溶液溶解1.00g K2FeO4样品,调节pH使高铁酸根全部被还原成亚铁离子,再调节pH为3~4,用1.0mol/L的Na2S2O3标准溶液作为滴定剂进行滴定(2Na2S2O3+I2=Na2S4O6+2NaI),淀粉作指示剂,装有Na2S2O3标准溶液的滴定管起始和终点读数如如图所示:______ mL。
②原样品中高铁酸钾的质量分数为______ 。[M(K2FeO4)=198g/mol]
③若在配制Na2S2O3标准溶液的过程中定容时俯视刻度线,则导致所测高铁酸钾的质量分数______ (填“偏高”、“偏低”或“无影响”)。
(2)反应时需将C装置置于冷水浴中,其原因为
(3)制备K2FeO4时,不能将碱性的KClO溶液滴加到Fe(NO3)3饱和溶液中,其原因是
(4)工业上常用废铁屑为原料制备Fe(NO3)3溶液,检验Fe3+所需试剂名称
(5)向反应后的三颈瓶中加入饱和KOH溶液,析出K2FeO4固体,过滤、洗涤、干燥。洗涤操作所用最佳试剂为
A.水 B.无水乙醇 C.稀KOH溶液
(6)工业上用“间接碘量法”测定高铁酸钾的纯度:用碱性KI溶液溶解1.00g K2FeO4样品,调节pH使高铁酸根全部被还原成亚铁离子,再调节pH为3~4,用1.0mol/L的Na2S2O3标准溶液作为滴定剂进行滴定(2Na2S2O3+I2=Na2S4O6+2NaI),淀粉作指示剂,装有Na2S2O3标准溶液的滴定管起始和终点读数如如图所示:
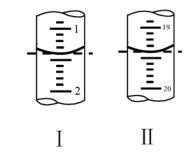
②原样品中高铁酸钾的质量分数为
③若在配制Na2S2O3标准溶液的过程中定容时俯视刻度线,则导致所测高铁酸钾的质量分数
您最近一年使用:0次
2021-02-02更新
|
109次组卷
|
2卷引用:江西省南昌市第十九中学2022-2023学年高三上学期(11月)第四次月考化学试卷
名校
解题方法
8 . 铁元素是人体中含量最高的生命必需微量元素,承担着极其重要的生理功能.在日常生活中,常见的食品抗氧化剂主要活性成分为铁粉,脱氧过程中的一步主要反应为4Fe(OH)2+O2+2H2O=4Fe(OH)3(红褐色固体)。工业上高铁酸盐在能源、环保等方面有着广泛的用途,湿法制备高铁酸盐的原理为3ClO-+10OH-+2Fe3+=2FeO +3Cl-+5H2O。根据以上信息,回答以下问题:
+3Cl-+5H2O。根据以上信息,回答以下问题:
(1)高铁酸根离子(FeO )中铁元素的化合价为
)中铁元素的化合价为____ ;湿法制备高铁酸盐的反应中,氧化剂是___ ,被氧化的元素是____ (填元素名称)。消耗1mol还原剂转移电子的物质的量为___ 。
(2)某化学小组用食品抗氧化剂(成分为铁粉、活性炭、氯化钠)进行以下实验。
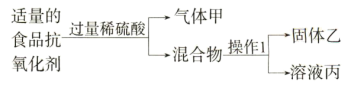
①操作1名称是____ ,溶液丙中一定含有的金属阳离子是____ 。
将乙烘干后,用乙的氧化物进行以下实验,物质之间的转化关系如图所示:(反应条件及部分产物略去)
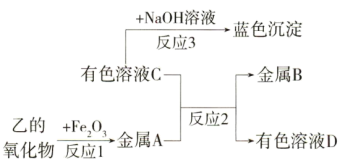
②写出反应1的化学方程式,并用单线桥标出电子转移的方向及数目:____ 。
③反应3的离子方程式为_____ 。
 +3Cl-+5H2O。根据以上信息,回答以下问题:
+3Cl-+5H2O。根据以上信息,回答以下问题:(1)高铁酸根离子(FeO
 )中铁元素的化合价为
)中铁元素的化合价为(2)某化学小组用食品抗氧化剂(成分为铁粉、活性炭、氯化钠)进行以下实验。

①操作1名称是
将乙烘干后,用乙的氧化物进行以下实验,物质之间的转化关系如图所示:(反应条件及部分产物略去)

②写出反应1的化学方程式,并用单线桥标出电子转移的方向及数目:
③反应3的离子方程式为
您最近一年使用:0次
2022-08-17更新
|
500次组卷
|
4卷引用:江西省南昌市豫章中学20212-2022学年高一下学期第一次月考化学试题
20-21高一上·全国·期中
名校
9 . 某结晶水合物的化学式为R·nH2O,其相对分子质量为m,在25°C时, ag晶体溶于bg水中即达饱和,形成VmL密度为 的溶液,下列表达式中不正确的是
的溶液,下列表达式中不正确的是
 的溶液,下列表达式中不正确的是
的溶液,下列表达式中不正确的是A.饱和溶液中R的质量分数为 |
B.25°C时,R的溶解度为 g g |
C.饱和溶液R的质量分数为 |
D.饱和溶液的物质的量浓度为 |
您最近一年使用:0次
2020-04-18更新
|
636次组卷
|
4卷引用:江西省南昌市八一中学2021-2022学年高二下学期化学期末考试试题
名校
10 . Ⅰ.实验室要配制500 mL 0.2 mol/L NaOH溶液,请回答下列问题:
(1)配制过程中不需要使用的化学仪器有________ (填字母)。
A 烧杯 B 500 mL容量瓶 C 漏斗 D 胶头滴管 E 玻璃棒
(2)用托盘天平称取氢氧化钠,其质量为________ g。
(3)下列主要操作步骤的正确顺序是________ (填序号)。
①称取一定质量的氢氧化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶瓶颈刻度线下1~2 cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③待冷却至室温后,将溶液转移到500 mL容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会使配制出的NaOH溶液浓度_______ (填“偏高、偏低”或“不变”)。
Ⅱ.如图实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为______ mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是______ 。
A 溶液中HCl的物质的量 B 溶液的浓度
C 溶液中Cl-的数目 D 溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol/L的稀盐酸。该学生需要量取______ mL上述浓盐酸进行配制。
Ⅲ.现有0.27kg质量分数为10%的CuCl2溶液,则溶液中CuCl2的物质的量为___________
(1)配制过程中不需要使用的化学仪器有
A 烧杯 B 500 mL容量瓶 C 漏斗 D 胶头滴管 E 玻璃棒
(2)用托盘天平称取氢氧化钠,其质量为
(3)下列主要操作步骤的正确顺序是
①称取一定质量的氢氧化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶瓶颈刻度线下1~2 cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③待冷却至室温后,将溶液转移到500 mL容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会使配制出的NaOH溶液浓度
Ⅱ.如图实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19g/cm3 HCl的质量分数:36.5% |
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是
A 溶液中HCl的物质的量 B 溶液的浓度
C 溶液中Cl-的数目 D 溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol/L的稀盐酸。该学生需要量取
Ⅲ.现有0.27kg质量分数为10%的CuCl2溶液,则溶液中CuCl2的物质的量为
您最近一年使用:0次
2019-11-27更新
|
1002次组卷
|
6卷引用:江西省南昌市八一中学2021-2022学年高二下学期化学期末考试试题
江西省南昌市八一中学2021-2022学年高二下学期化学期末考试试题河南省洛阳市宜阳县第一高级中学2022-2023学年高一上学期第四次能力达标测试化学试题黑龙江省绥化市青冈县第一中学2019-2020学年高一上学期期中考试(B班)化学试题河北省邯郸市魏县2021-2022学年高一上学期11月联考化学试题江苏省南京市第五高级中学2022-2023学年高一上学期学情自测卷化学试题(已下线)押题卷02-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(江苏专用)



