名校
1 . NA为阿伏加德罗常数的值,下列说法正确的是
| A.常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA |
B.含0.5molCr2O 的酸性溶液与足量H2O2反应生成 的酸性溶液与足量H2O2反应生成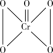 ,转移电子数4NA ,转移电子数4NA |
| C.1molXeF4中氙的价层电子对数为4NA |
| D.标准状况下,22.4LCH4和44.8LCl2在光照下充分反应后的分子数为3NA |
您最近一年使用:0次
名校
解题方法
2 . 亚硝酸钙 可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应
可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应 利用如下装置制备亚硝酸钙(加热及夹持装置略)。
利用如下装置制备亚硝酸钙(加热及夹持装置略)。 溶液能将NO氧化为
溶液能将NO氧化为 。
。
回答下列问题:
(1)检查装置气密性,加入相应的试剂。先通 ,其目的是
,其目的是________ 。通 后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开
后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开 ,使稀硝酸滴入三颈烧瓶中;(iv)关闭
,使稀硝酸滴入三颈烧瓶中;(iv)关闭 ,打开
,打开 ,通入
,通入 。操作(ii)是
。操作(ii)是________ 。
(2)仪器a的名称为________ ,装置D中盛装的试剂是________ (填名称),装置E的作用是________ 。
(3)制备的产品 样品中含有杂质
样品中含有杂质 ,通过下列方法可测定产品的纯度:称量mg样品溶于水,加
,通过下列方法可测定产品的纯度:称量mg样品溶于水,加 固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作:
固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作: ;“还原
;“还原 ”时加入
”时加入 的
的 标准液,“滴定剩余
标准液,“滴定剩余 ”时消耗
”时消耗 的
的 标准溶液VmL。“滴定剩余
标准溶液VmL。“滴定剩余 ”过程中发生反应的离子方程式为
”过程中发生反应的离子方程式为________ ,样品中 的纯度为
的纯度为________ (用含m、V的式子表示)。
 可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应
可用作化学合成反应中的催化剂、氧化剂、中间体等。实验室根据反应 利用如下装置制备亚硝酸钙(加热及夹持装置略)。
利用如下装置制备亚硝酸钙(加热及夹持装置略)。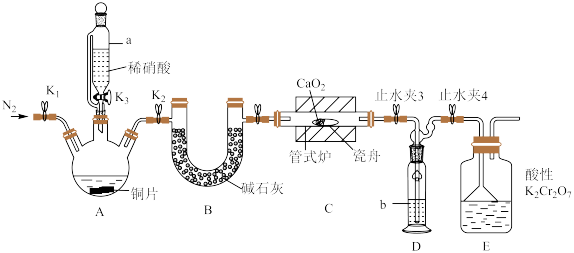
 溶液能将NO氧化为
溶液能将NO氧化为 。
。回答下列问题:
(1)检查装置气密性,加入相应的试剂。先通
 ,其目的是
,其目的是 后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开
后进行的操作为(i)打开管式炉,对瓷舟进行加热;(ii)……;(iii)打开 ,使稀硝酸滴入三颈烧瓶中;(iv)关闭
,使稀硝酸滴入三颈烧瓶中;(iv)关闭 ,打开
,打开 ,通入
,通入 。操作(ii)是
。操作(ii)是(2)仪器a的名称为
(3)制备的产品
 样品中含有杂质
样品中含有杂质 ,通过下列方法可测定产品的纯度:称量mg样品溶于水,加
,通过下列方法可测定产品的纯度:称量mg样品溶于水,加 固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作:
固体,充分振荡,过滤后将溶液转移到250mL容量瓶,配制溶液,取25mL溶液进行以下操作: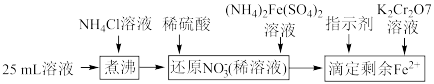
 ;“还原
;“还原 ”时加入
”时加入 的
的 标准液,“滴定剩余
标准液,“滴定剩余 ”时消耗
”时消耗 的
的 标准溶液VmL。“滴定剩余
标准溶液VmL。“滴定剩余 ”过程中发生反应的离子方程式为
”过程中发生反应的离子方程式为 的纯度为
的纯度为
您最近一年使用:0次
2024-06-01更新
|
292次组卷
|
7卷引用:江西省南昌市八一中学2024届高三下学期三模测试化学试题
名校
解题方法
3 . 下列反应的离子方程式正确的是
A.向FeI2溶液中通入一定量氯气,测得有50%的Fe2+被氧化: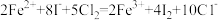 |
| B.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
C.CuO溶于 溶液: 溶液: |
D.向有AgCl沉淀的溶液中滴加氨水,沉淀消失: |
您最近一年使用:0次
4 . 二氧化碳的捕集和转化是科学研究中的热点问题,我国科研人员提出了由 和
和 转化为
转化为 和
和 的反应历程如图,下列说法正确的是
的反应历程如图,下列说法正确的是
 和
和 转化为
转化为 和
和 的反应历程如图,下列说法正确的是
的反应历程如图,下列说法正确的是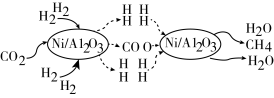
A.该反应的化学方程式为: |
B.反应中使用的催化剂为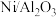 ,Al和 ,Al和 是同周期元素 是同周期元素 |
C. 分子的电子式为: 分子的电子式为: |
D.上述反应中捕集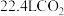 ,转移电子数为 ,转移电子数为 |
您最近一年使用:0次
解题方法
5 . 纳米磁性 在生物靶向材料、微波吸收材料及静电复印显影剂等方面都有极其广泛的用途。一种利用废旧镀锌铁皮制备纳米磁性
在生物靶向材料、微波吸收材料及静电复印显影剂等方面都有极其广泛的用途。一种利用废旧镀锌铁皮制备纳米磁性 的工艺流程如下:
的工艺流程如下: 溶于强碱时生成
溶于强碱时生成 。
。
(1)“碱洗”废旧镀锌铁皮的目的是___________(填字母)。
(2)“酸溶”后的溶液中阳离子主要有___________ 。
(3)“氧化”时发生的总反应离子方程式为___________ 。在酸性条件下, 很容易发生反应:
很容易发生反应: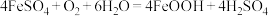 。为避免生成
。为避免生成 影响产品纯度,则“氧化”时应选择的加料方式为
影响产品纯度,则“氧化”时应选择的加料方式为___________ 。
(4)“氧化”后溶液中 的物质的量之比是1∶2,检验其中
的物质的量之比是1∶2,检验其中 可选用的试剂是___________。
可选用的试剂是___________。
(5)“分离”时 纳米粒子不能采用过滤法实现固液分离,理由是
纳米粒子不能采用过滤法实现固液分离,理由是___________ 。
(6)用重铬酸钾法(一种氧化还原滴定法)可测定产物 中的二价铁含量。若需配制浓度为
中的二价铁含量。若需配制浓度为 的
的 标准溶液
标准溶液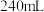 ,应准确称取
,应准确称取___________ g (保留4位有效数字,已知
(保留4位有效数字,已知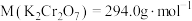 )。
)。
 在生物靶向材料、微波吸收材料及静电复印显影剂等方面都有极其广泛的用途。一种利用废旧镀锌铁皮制备纳米磁性
在生物靶向材料、微波吸收材料及静电复印显影剂等方面都有极其广泛的用途。一种利用废旧镀锌铁皮制备纳米磁性 的工艺流程如下:
的工艺流程如下:
 溶于强碱时生成
溶于强碱时生成 。
。(1)“碱洗”废旧镀锌铁皮的目的是___________(填字母)。
| A.去除油污 | B.溶解镀锌层 | C.去除铁锈 | D.钝化铁皮 |
(2)“酸溶”后的溶液中阳离子主要有
(3)“氧化”时发生的总反应离子方程式为
 很容易发生反应:
很容易发生反应: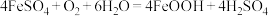 。为避免生成
。为避免生成 影响产品纯度,则“氧化”时应选择的加料方式为
影响产品纯度,则“氧化”时应选择的加料方式为(4)“氧化”后溶液中
 的物质的量之比是1∶2,检验其中
的物质的量之比是1∶2,检验其中 可选用的试剂是___________。
可选用的试剂是___________。A. 溶液 溶液 | B. 溶液 溶液 | C.酸性 溶液 溶液 | D. |
(5)“分离”时
 纳米粒子不能采用过滤法实现固液分离,理由是
纳米粒子不能采用过滤法实现固液分离,理由是(6)用重铬酸钾法(一种氧化还原滴定法)可测定产物
 中的二价铁含量。若需配制浓度为
中的二价铁含量。若需配制浓度为 的
的 标准溶液
标准溶液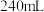 ,应准确称取
,应准确称取 (保留4位有效数字,已知
(保留4位有效数字,已知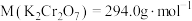 )。
)。
您最近一年使用:0次
解题方法
6 .  在化工生产中有重要作用,实验小组用下图装置制备
在化工生产中有重要作用,实验小组用下图装置制备 。请回答下列问题。
。请回答下列问题。 ,
, ,
, 。
。
②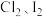 易溶于正己烷(分子式:
易溶于正己烷(分子式: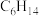 ,沸点:69℃)。
,沸点:69℃)。
③ 的正己烷溶液呈橙红色,
的正己烷溶液呈橙红色,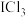 的正己烷溶液呈黄色。
的正己烷溶液呈黄色。
(1)装置A中反应的化学方程式为___________ 。
(2)仪器 的名称为
的名称为___________ ,该装置的作用是___________ 。
(3)从 中选择合适的装置制备
中选择合适的装置制备 ,装置正确的连接顺序为
,装置正确的连接顺序为
___________ 。
(4)制备 时,反应温度控制在30~40℃,采用的加热方法是
时,反应温度控制在30~40℃,采用的加热方法是___________ ,当观察到C中的颜色变为___________ 色时,停止加热A装置。
(5)制备 时,
时,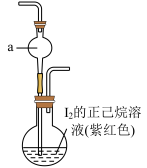 优于
优于 (加热装置已略)的原因有
(加热装置已略)的原因有___________ (答一条即可)。
(6)由于氯气会与自来水中的有机物发生反应生成对人体有害的物质,人们尝试研究并使用新的自来水消毒剂,如 气体就是一种新型高效含氯消毒剂。一种制备
气体就是一种新型高效含氯消毒剂。一种制备 的方法是用
的方法是用 通入硫酸酸化的
通入硫酸酸化的 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为___________ 。
 在化工生产中有重要作用,实验小组用下图装置制备
在化工生产中有重要作用,实验小组用下图装置制备 。请回答下列问题。
。请回答下列问题。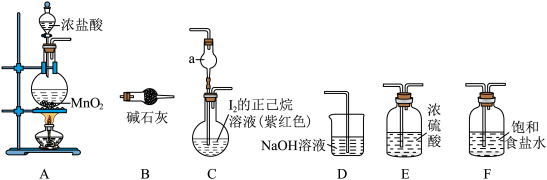
 ,
, ,
, 。
。②
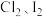 易溶于正己烷(分子式:
易溶于正己烷(分子式: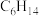 ,沸点:69℃)。
,沸点:69℃)。③
 的正己烷溶液呈橙红色,
的正己烷溶液呈橙红色,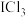 的正己烷溶液呈黄色。
的正己烷溶液呈黄色。(1)装置A中反应的化学方程式为
(2)仪器
 的名称为
的名称为(3)从
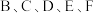 中选择合适的装置制备
中选择合适的装置制备 ,装置正确的连接顺序为
,装置正确的连接顺序为
(4)制备
 时,反应温度控制在30~40℃,采用的加热方法是
时,反应温度控制在30~40℃,采用的加热方法是(5)制备
 时,
时, 优于
优于 (加热装置已略)的原因有
(加热装置已略)的原因有(6)由于氯气会与自来水中的有机物发生反应生成对人体有害的物质,人们尝试研究并使用新的自来水消毒剂,如
 气体就是一种新型高效含氯消毒剂。一种制备
气体就是一种新型高效含氯消毒剂。一种制备 的方法是用
的方法是用 通入硫酸酸化的
通入硫酸酸化的 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为
您最近一年使用:0次
解题方法
7 . 价类二维图是我们学习元素及其化合物相关知识的重要模型和工具。如图是钠的价类二维图: 中氢元素的化合价为
中氢元素的化合价为___________ , 能与水剧烈反应:
能与水剧烈反应: ,该反应中氧化剂和还原剂的物质的量之比是
,该反应中氧化剂和还原剂的物质的量之比是___________ 。
(2)某同学欲进行钠在空气中燃烧的实验,可将钠放入___________ (填字母)中进行加热。
A.蒸发皿 B.坩埚
(3)若①是一种淡黄色固体,其在呼吸面具中作供氧剂的原理是___________ (用化学方程式表示,写一个即可)。
(4)检验上图中物质所含钠元素的方法___________ 。
(5)某纯碱样品中含杂质 ,取质量为
,取质量为 的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到
的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到 固体物质,则此样品中
固体物质,则此样品中 的质量分数为
的质量分数为___________ 。
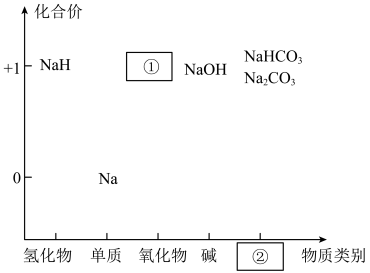
 中氢元素的化合价为
中氢元素的化合价为 能与水剧烈反应:
能与水剧烈反应: ,该反应中氧化剂和还原剂的物质的量之比是
,该反应中氧化剂和还原剂的物质的量之比是(2)某同学欲进行钠在空气中燃烧的实验,可将钠放入
A.蒸发皿 B.坩埚
(3)若①是一种淡黄色固体,其在呼吸面具中作供氧剂的原理是
(4)检验上图中物质所含钠元素的方法
(5)某纯碱样品中含杂质
 ,取质量为
,取质量为 的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到
的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到 固体物质,则此样品中
固体物质,则此样品中 的质量分数为
的质量分数为
您最近一年使用:0次
解题方法
8 . 我国嫦娥五号探测器带回的月土中含有原子序数依次增大的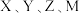 四种短周期主族元素。
四种短周期主族元素。 有杀菌消毒作用:
有杀菌消毒作用: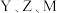 为同周期相邻元素,且其中只有一种是非金属元素。下列说法中正确的是
为同周期相邻元素,且其中只有一种是非金属元素。下列说法中正确的是
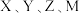 四种短周期主族元素。
四种短周期主族元素。 有杀菌消毒作用:
有杀菌消毒作用: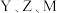 为同周期相邻元素,且其中只有一种是非金属元素。下列说法中正确的是
为同周期相邻元素,且其中只有一种是非金属元素。下列说法中正确的是A. 元素的最高正价为 元素的最高正价为 价 价 | B.Z单质的导电性能弱于 单质 单质 |
C. 与 与 形成的化合物能与强碱反应 形成的化合物能与强碱反应 | D.原子半径由大到小的顺序为 |
您最近一年使用:0次
解题方法
9 . 2023年国庆节,南昌以天空为幕,以烟花为笔,举办了一场盛大的“风景这边独好”国庆烟花晚会。璀敁的焰火点亮了南昌的夜空,惊艳了无数国人。这与高中化学中“焰色试验”知识相关,下列说法中正确的是
| A.焰色试验是化学变化 | B.利用焰色试验可区分 与 与 固体 固体 |
| C.焰色试验均应透过蓝色钴玻璃观察 | D.用稀盐酸清洗做焰色试验的铂丝 |
您最近一年使用:0次
解题方法
10 . 下列方程式书写正确的是
A. 溶液中: 溶液中: |
B.小苏打与盐酸反应: |
C.往硫酸氢钠溶液中逐滴加入氢氧化钡溶液至呈中性: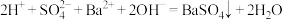 |
D.钠投入硫酸铜溶液中: |
您最近一年使用:0次



