1 . 每年10月23日上午6:02到晚上6:02被誉为“摩尔日”(MoleDay),这个时间的美式写法为6:0210/23。外观与阿伏加德罗常数相似。
(1)分子数为 个
个 的物质的量约为
的物质的量约为___________ mol。
(2)标准状况下,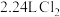 的质量为
的质量为___________ g。
(3)同温同压下,等体积的NO气体和 气体中氧原子的个数之比为
气体中氧原子的个数之比为___________ 。
(4)等质量的CO和 中氧原子的个数之比为
中氧原子的个数之比为___________ 。
(5) 中含有b个氧原子,则阿伏加德罗常数的表达式为
中含有b个氧原子,则阿伏加德罗常数的表达式为_________________  。(用含a、b的式子表示)
。(用含a、b的式子表示)
(6)已知a g的A和b g的B恰好完全反应生成0.2mol的C和d g的D,则C的摩尔质量为_____________  。(用含a、b、d的式子表示)
。(用含a、b、d的式子表示)
(1)分子数为
 个
个 的物质的量约为
的物质的量约为(2)标准状况下,
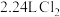 的质量为
的质量为(3)同温同压下,等体积的NO气体和
 气体中氧原子的个数之比为
气体中氧原子的个数之比为(4)等质量的CO和
 中氧原子的个数之比为
中氧原子的个数之比为(5)
 中含有b个氧原子,则阿伏加德罗常数的表达式为
中含有b个氧原子,则阿伏加德罗常数的表达式为 。(用含a、b的式子表示)
。(用含a、b的式子表示)(6)已知a g的A和b g的B恰好完全反应生成0.2mol的C和d g的D,则C的摩尔质量为
 。(用含a、b、d的式子表示)
。(用含a、b、d的式子表示)
您最近一年使用:0次
解题方法
2 . 有以下物质:①钠;② ;③NaOH;④
;③NaOH;④ ;⑤液氯;⑥氯水;⑦次氯酸钙;⑧氯化铁溶液;⑨澄清的石灰水;⑩稀盐酸。根据问题,请完成以下填空:
;⑤液氯;⑥氯水;⑦次氯酸钙;⑧氯化铁溶液;⑨澄清的石灰水;⑩稀盐酸。根据问题,请完成以下填空:
(1)以上物质中属于电解质的是
(2)以下两种物质溶于水,书写出相应的电离方程式。
 :
:
次氯酸钙:
(3)①与⑧反应,书写出该反应的总的离子方程式
(4)②与⑩反应,书写出相应的化学方程式
(5)④与少量的⑨反应,书写出相应的离子方程式
您最近一年使用:0次
解题方法
3 .  的制取工艺及综合实验探究。
的制取工艺及综合实验探究。
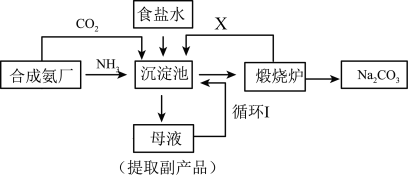
(1)我国化学家侯德榜改革国外的纯碱生产工艺,其生产流程可简要表示如下:
①往饱和食盐水中通入足量的 、足量的
、足量的 的先后顺序是
的先后顺序是___________________ 。
②沉淀池中和煅烧炉中所发生反应的化学方程式为____________________________________ ;____________________________________ 。
③从生产流程图可知,可循环利用的物质是________________ 。(写化学式)
(2)测定所得产品的组成和纯度
①检验纯碱样品中是否混有 :将样品溶于水,逐滴加入盐酸,产生气体的体积
:将样品溶于水,逐滴加入盐酸,产生气体的体积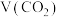 与加入盐酸的体积
与加入盐酸的体积 的关系如图所示(不计
的关系如图所示(不计 溶解)。回答以下问题:
溶解)。回答以下问题:
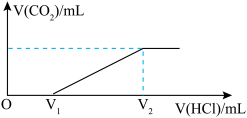
经测定,消耗盐酸的体积
____________ 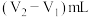 (填“>”、“<”、“=”),可以说明纯碱样品中确实混有
(填“>”、“<”、“=”),可以说明纯碱样品中确实混有 ;其中消耗盐酸的体积
;其中消耗盐酸的体积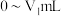 的过程中,所发生反应的离子方程式为
的过程中,所发生反应的离子方程式为______________________________ 。
②测定该纯碱样品的纯度:称取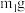 样品,置于小烧杯中,加水溶解,滴加足量
样品,置于小烧杯中,加水溶解,滴加足量 溶液。将反应混合物过滤、洗涤、干燥、称量,得到固体的质量为
溶液。将反应混合物过滤、洗涤、干燥、称量,得到固体的质量为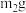 。则该纯碱样品的纯度(以
。则该纯碱样品的纯度(以 的质量分数进行计算)为
的质量分数进行计算)为_______________ 。(用含%的式子表示)
 的制取工艺及综合实验探究。
的制取工艺及综合实验探究。
(1)我国化学家侯德榜改革国外的纯碱生产工艺,其生产流程可简要表示如下:
①往饱和食盐水中通入足量的
 、足量的
、足量的 的先后顺序是
的先后顺序是②沉淀池中和煅烧炉中所发生反应的化学方程式为
③从生产流程图可知,可循环利用的物质是
(2)测定所得产品的组成和纯度
①检验纯碱样品中是否混有
 :将样品溶于水,逐滴加入盐酸,产生气体的体积
:将样品溶于水,逐滴加入盐酸,产生气体的体积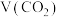 与加入盐酸的体积
与加入盐酸的体积 的关系如图所示(不计
的关系如图所示(不计 溶解)。回答以下问题:
溶解)。回答以下问题:
经测定,消耗盐酸的体积

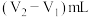 (填“>”、“<”、“=”),可以说明纯碱样品中确实混有
(填“>”、“<”、“=”),可以说明纯碱样品中确实混有 ;其中消耗盐酸的体积
;其中消耗盐酸的体积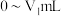 的过程中,所发生反应的离子方程式为
的过程中,所发生反应的离子方程式为②测定该纯碱样品的纯度:称取
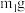 样品,置于小烧杯中,加水溶解,滴加足量
样品,置于小烧杯中,加水溶解,滴加足量 溶液。将反应混合物过滤、洗涤、干燥、称量,得到固体的质量为
溶液。将反应混合物过滤、洗涤、干燥、称量,得到固体的质量为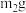 。则该纯碱样品的纯度(以
。则该纯碱样品的纯度(以 的质量分数进行计算)为
的质量分数进行计算)为
您最近一年使用:0次
4 . 化学实验兴趣小组为了探究在实验室制备 的过程中有水蒸气挥发出来,同时验证
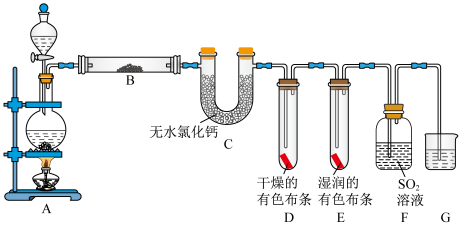
的过程中有水蒸气挥发出来,同时验证 的某些性质。甲同学设计了如图所示的实验装置(部分夹持装置省略)。回答下列问题:
的某些性质。甲同学设计了如图所示的实验装置(部分夹持装置省略)。回答下列问题:
(1)实验室制备 的反应原理中,从氧化还原的角度分析,
的反应原理中,从氧化还原的角度分析, 属于
属于___________ 产物。
(2)在标准状况下,若用含0.2mol HCl的浓盐酸与足量的 反应制取
反应制取 ,制得
,制得 体积
体积____________ (填“>”、“<”、“=”)1.12L。
(3)装置B中盛放无水 ,若出现的现象为
,若出现的现象为____________________________________ ,说明生成 含有水蒸气。
含有水蒸气。
(4)实验时装置D和E中出现了不同的现象,说明装置E中氯气与水发生反应的化学方程式为____________________________________ 。
(5)当装置F中通入 ,发生反应的离子方程式为
,发生反应的离子方程式为________________________________ 。
(6)装置G中应放入____________ ,吸收多余 ,防止污染环境。
,防止污染环境。
(7)某温度下,将氯气通入 溶液中,反应得到
溶液中,反应得到 、
、 和
和 的混合溶液,经测定
的混合溶液,经测定 与
与 的个数比为3:1。则氯气与
的个数比为3:1。则氯气与 反应时,被还原的氯原子和被氧化的氯原子的个数比为
反应时,被还原的氯原子和被氧化的氯原子的个数比为____________ 。
 的过程中有水蒸气挥发出来,同时验证
的过程中有水蒸气挥发出来,同时验证 的某些性质。甲同学设计了如图所示的实验装置(部分夹持装置省略)。回答下列问题:
的某些性质。甲同学设计了如图所示的实验装置(部分夹持装置省略)。回答下列问题:
(1)实验室制备
 的反应原理中,从氧化还原的角度分析,
的反应原理中,从氧化还原的角度分析, 属于
属于(2)在标准状况下,若用含0.2mol HCl的浓盐酸与足量的
 反应制取
反应制取 ,制得
,制得 体积
体积(3)装置B中盛放无水
 ,若出现的现象为
,若出现的现象为 含有水蒸气。
含有水蒸气。(4)实验时装置D和E中出现了不同的现象,说明装置E中氯气与水发生反应的化学方程式为
(5)当装置F中通入
 ,发生反应的离子方程式为
,发生反应的离子方程式为(6)装置G中应放入
 ,防止污染环境。
,防止污染环境。(7)某温度下,将氯气通入
 溶液中,反应得到
溶液中,反应得到 、
、 和
和 的混合溶液,经测定
的混合溶液,经测定 与
与 的个数比为3:1。则氯气与
的个数比为3:1。则氯气与 反应时,被还原的氯原子和被氧化的氯原子的个数比为
反应时,被还原的氯原子和被氧化的氯原子的个数比为
您最近一年使用:0次
解题方法
5 . 硫化氢的转化是资源利用和环境保护的重要研究课题。 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收S,其转化关系如图所示(CuS不溶于水)。下列说法中不正确的是
的混合溶液中回收S,其转化关系如图所示(CuS不溶于水)。下列说法中不正确的是

 和空气的混合气体通入
和空气的混合气体通入 、
、 和
和 的混合溶液中回收S,其转化关系如图所示(CuS不溶于水)。下列说法中不正确的是
的混合溶液中回收S,其转化关系如图所示(CuS不溶于水)。下列说法中不正确的是
A.过程中①中生成CuS的反应为: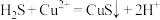 |
B.由图示的转化可得出氧化性的强弱顺序: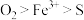 |
| C.在转化过程中化合价不变的元素只有:Cu和Cl |
D.回收S的总反应为: |
您最近一年使用:0次
6 . 某固体可能含有 、
、 、
、 、
、 、
、 、
、 中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
(1)一份固体溶于水得无色透明溶液,加入足量 溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。
溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。
(2)另一份固体与过量NaOH固体混合后充分加热,产生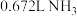 (标准状况)。
(标准状况)。
(已知: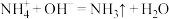 )
)
下列说法正确的是
 、
、 、
、 、
、 、
、 、
、 中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);(1)一份固体溶于水得无色透明溶液,加入足量
 溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。
溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。(2)另一份固体与过量NaOH固体混合后充分加热,产生
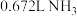 (标准状况)。
(标准状况)。(已知:
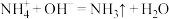 )
)下列说法正确的是
A.该固体中一定含有 、 、 、 、 、 、 |
B.该固体中一定没有 、 、 、 、 |
C.该固体中只含有 、 、 、 、 、 、 |
D.根据以上实验,无法确定该固体中有 |
您最近一年使用:0次
7 .  表示阿伏加德罗常数的值。下列叙述中正确的是
表示阿伏加德罗常数的值。下列叙述中正确的是
 表示阿伏加德罗常数的值。下列叙述中正确的是
表示阿伏加德罗常数的值。下列叙述中正确的是A.常温常压下, 固体中含有的离子数目为 固体中含有的离子数目为 |
B.常温常压下, 个 个 的质量是62g 的质量是62g |
C.标准状况下,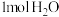 所占的体积约为22.4L 所占的体积约为22.4L |
D.标准状况下, 含有的原子数目为 含有的原子数目为 |
您最近一年使用:0次
解题方法
8 . 用下列装置制备并检验 的性质,下列有关装置和叙述都正确的是
的性质,下列有关装置和叙述都正确的是

 的性质,下列有关装置和叙述都正确的是
的性质,下列有关装置和叙述都正确的是
A.Ⅰ图中:如果 过量,浓盐酸就可以全部反应完 过量,浓盐酸就可以全部反应完 |
B.Ⅱ图中:利用排气法收集 ,并将多余的 ,并将多余的 进行尾气吸收 进行尾气吸收 |
| C.Ⅲ图中:如果光照充分,量筒内的水面会逐渐上升直到全部充满 |
D.Ⅳ图中:干燥的有色布条不褪色,湿润的有色布条能褪色,说明 有漂白性 有漂白性 |
您最近一年使用:0次
解题方法
9 . 在给定条件下,下列选项中所示物质之间转化均能实现的是
A. |
B.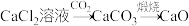 |
C.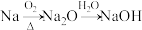 |
D.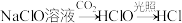 |
您最近一年使用:0次
解题方法
10 . 2023年10月26日,神舟十七号载人飞船于当天11时13分59秒点火发射,并顺利进入预定轨道,发射取得圆满成功。神舟飞船以肼( )和四氧化二氮(
)和四氧化二氮( )为动力源,发生的反应:
)为动力源,发生的反应: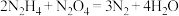 ,反应温度可高达2700℃,对于该反应,下列说法中正确的是
,反应温度可高达2700℃,对于该反应,下列说法中正确的是

 )和四氧化二氮(
)和四氧化二氮( )为动力源,发生的反应:
)为动力源,发生的反应: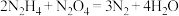 ,反应温度可高达2700℃,对于该反应,下列说法中正确的是
,反应温度可高达2700℃,对于该反应,下列说法中正确的是
A. 是氧化剂 是氧化剂 |
B. 发生了氧化反应 发生了氧化反应 |
| C.氧化产物和还原产物的物质的量之比为2:1 |
D.每消耗 ,反应中转移的电子数为 ,反应中转移的电子数为 |
您最近一年使用:0次



