1 . a.有下列物质:①氢氧化钡 ②KHSO4 ③液态HCl ④稀硫酸 ⑤二氧化碳 ⑥铜 ⑦碳酸钠 ⑧蔗糖
请回答下列问题:
(1)属于电解质的有___________ (填序号)
(2)属于非电解质的有___________ (填序号)
b.某同学用如下实验探究 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:
(3)在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为___________ 。FeCl3溶液,加入1滴___________ 溶液,溶液变___________ 。
(4)FeCl2溶液与氯水反应的化学方程式为___________ 。
(5)某同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程___________ 。
c.请回答下列问题:
(6)0.5 mol H2O含有H的物质的量___________ mol。含有O数目___________ 。
(7)100 mL 0.2 mol/L Na2SO4溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(8)标准状况下11.2 L的CO2的物质的量是___________ mol。
请回答下列问题:
(1)属于电解质的有
(2)属于非电解质的有
b.某同学用如下实验探究
 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:(3)在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为
(4)FeCl2溶液与氯水反应的化学方程式为
(5)某同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程
c.请回答下列问题:
(6)0.5 mol H2O含有H的物质的量
(7)100 mL 0.2 mol/L Na2SO4溶液中
 的物质的量浓度为
的物质的量浓度为(8)标准状况下11.2 L的CO2的物质的量是
您最近一年使用:0次
解题方法
2 . 下列离子的检验方法中合理的是
A.向某溶液中滴入H2O2溶液产生气泡,说明不含 |
B.用酸性KMnO4溶液检验FeSO4溶液中是否含有 |
C.向某溶液中加入NaOH溶液,直接得到红褐色沉淀,说明溶液中含有 |
D.向某溶液中加入NaOH溶液得到白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中只含有 ,不含有 ,不含有 |
您最近一年使用:0次
名校
3 . 电子工业中,人们常用FeCl3溶液腐蚀附在绝缘板上的铜箔,制造印刷电路板。
(1)请用化学方程式表示制造印刷电路板的反应原理_________________ 。
为了从腐蚀废液中回收铜并重新获得FeCl3溶液,可采用以下步骤:
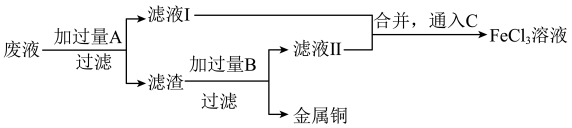
(2)写出回收铜并重新获得FeCl3溶液的过程中加入的有关物质的化学式:
A________ ,B________ ,C________ 。
(3)滤液Ⅰ中的阳离子既有氧化性又有还原性,判断的依据是_________________ 。为检验该金属阳离子,可设计的实验操作及实验现象为_________________ (可选择的试剂为“锌片”、KSCN溶液、“酸性H2O2”、“酸性KMnO4溶液”或“NaOH溶液”),且该过程发生的氧化还原反应离子方程式为_______________ 。
(4)上述步骤中,通入C发生反应的离子方程式为___________________ 。
(1)请用化学方程式表示制造印刷电路板的反应原理
为了从腐蚀废液中回收铜并重新获得FeCl3溶液,可采用以下步骤:

(2)写出回收铜并重新获得FeCl3溶液的过程中加入的有关物质的化学式:
A
(3)滤液Ⅰ中的阳离子既有氧化性又有还原性,判断的依据是
(4)上述步骤中,通入C发生反应的离子方程式为
您最近一年使用:0次
2024-01-09更新
|
67次组卷
|
2卷引用:新疆乌鲁木齐市实验学校2023-2024学年高一上学期1月期末化学试题
名校
解题方法
4 . 如图所示是铁及其化合物的“价类”二维图:

(1)X、Y分别代表_________ 、__________ ;(各1分)Z在空气中转化为W的化学方程式为__________ ,现象_________________________
(2)某小组研究 性质,预测
性质,预测 能与
能与___________ 发生氧化还原反应(填序号)
① 溶液 ②氯水 ③稀盐酸 ④酸性
溶液 ②氯水 ③稀盐酸 ④酸性 溶液 ⑤
溶液 ⑤ 溶液 ⑥碳酸钠
溶液 ⑥碳酸钠
(3)铁盐溶液可用于金属刻蚀,如何检验某溶液中存在
_________________________________ (写出两种检验手段);如用 溶液刻蚀铜制电路板,
溶液刻蚀铜制电路板, 被
被_________ (填“还原”或“氧化”)为 ,该反应的离子方程式为
,该反应的离子方程式为_____________________________ 。

(1)X、Y分别代表
(2)某小组研究
 性质,预测
性质,预测 能与
能与①
 溶液 ②氯水 ③稀盐酸 ④酸性
溶液 ②氯水 ③稀盐酸 ④酸性 溶液 ⑤
溶液 ⑤ 溶液 ⑥碳酸钠
溶液 ⑥碳酸钠(3)铁盐溶液可用于金属刻蚀,如何检验某溶液中存在

 溶液刻蚀铜制电路板,
溶液刻蚀铜制电路板, 被
被 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
名校
5 . 为了检验某长期放置的FeCl2溶液是否完全变质,可选用的试剂是
| A.氨水 | B.酸性高锰酸钾溶液 | C.KSCN | D.淀粉 |
您最近一年使用:0次
2023-12-03更新
|
246次组卷
|
2卷引用:新疆喀什地区十四校2023-2024学年高一上学期期末质量检测化学试卷
名校
6 . 下列关于离子检验的说法正确的是
| A.检验溶液中是否含有Ba2+;取少量待测液,向其中加入少量稀硫酸,若有白色沉淀产生,则溶液中含有Ba2+ |
| B.检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可选用的试剂是酸性KMnO4溶液 |
C.检验溶液中是否含有CO :取少量待测液,向其中加入适量稀盐酸,观察是否有大量气泡产生 :取少量待测液,向其中加入适量稀盐酸,观察是否有大量气泡产生 |
| D.在未知溶液中滴加稀盐酸出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液有Ag+ |
您最近一年使用:0次
名校
7 . 下列实验操作与实验现象及结论对应且正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向某溶液逐滴加入NaOH溶液 | 先有白色胶状沉淀产生,后来沉淀逐渐消失 | 溶液中可能含有 |
| B | 向某溶液中滴加氯水,然后再滴加KSCN溶液 | 溶液显红色 | 溶液中含有 |
| C | SO2分别通入酸性KMnO4和品红溶液 | 溶液均褪色 | SO2均表现漂白性 |
| D | 向Fe(NO3)2溶液中滴入2滴浓H2SO4 | 溶液变为黄色 | 氧化性:浓H2SO4>Fe3+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 下列离子方程式书写正确的是
A.向碳酸氢铵溶液中加入过量的 溶液: 溶液: |
B.过量铁粉加入稀硝酸中: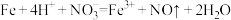 |
C.用过量氨水吸收工业尾气中的 : : |
D.氢氧化亚铁溶于过量稀硝酸: |
您最近一年使用:0次
解题方法
9 . 铁元素是人体内一种微量元素,主要以Fe2+的形式存在。请回答下列问题:
(1)下列微粒中,既有氧化性又有还原性的是______ (填字母)。
A.Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中______ 是还原剂
(3)某种麦片中含有微量的细小铁粉,食用该麦片后,铁粉与胃酸反应的离子方程式是___________ 。
(4)含硫酸亚铁的药片可治疗缺铁性贫血,其表面有糖衣,糖衣的作用是___________ 。可用___________ 溶液检验该硫酸亚铁药片是否变质。
(1)下列微粒中,既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中
(3)某种麦片中含有微量的细小铁粉,食用该麦片后,铁粉与胃酸反应的离子方程式是
(4)含硫酸亚铁的药片可治疗缺铁性贫血,其表面有糖衣,糖衣的作用是
您最近一年使用:0次
解题方法
10 . 化合价和物质类别是整理元素及化合物知识的两个要素,可表示为“价—类”二维图。铁元素的“价—类”二维图如图所示,下列说法正确的是

| A.工业上用CO还原Fe2O3炼铁,该反应为置换反应 |
| B.Fe3O4中铁元素为+4价 |
| C.要除去FeCl2溶液中少量的FeCl3,可加入适量铁粉并过滤 |
| D.Fe(OH)2浊液露置于空气中,由白色立即变为红褐色 |
您最近一年使用:0次



