1 . 下列关于Na2O和Na2O2的叙述正确的是
| A.将Na2O与Na2O2分别加入滴有酚酞的水中,二者现象相同 |
| B.在Na2O2与水的反应中,氧化产物与还原产物物质的量之比为1:4 |
| C.将Na2O2分别加入FeCl3和FeCl2溶液中最终所得沉淀颜色相同 |
| D.等质量的Na2O与Na2O2投入等量且足量水中充分反应后所得溶液物质的量浓度相等 |
您最近一年使用:0次
2023-06-20更新
|
424次组卷
|
3卷引用:河南省郑州外国语学校2020-2021学年高一上学期第二次月考化学试题
名校
解题方法
2 . 现有氧化还原反应: 。根据上述反应,判断下列结论正确的是:
。根据上述反应,判断下列结论正确的是:
 。根据上述反应,判断下列结论正确的是:
。根据上述反应,判断下列结论正确的是:A.还原性强弱顺序为 |
B.反应 中 中 是 是 的还原产物,反应 的还原产物,反应 中 中 是 是 的氧化产物 的氧化产物 |
C.若向酸性 溶液中加入 溶液中加入 溶液,可观察到溶液紫红色褪去 溶液,可观察到溶液紫红色褪去 |
D. 通入含 通入含 的溶液中,离子反应为: 的溶液中,离子反应为: |
您最近一年使用:0次
名校
解题方法
3 . 铋酸钠(NaBiO3)常用作Mn2+鉴定的强氧化剂,某研究小组用浮选过的辉铋矿(主要成分是Bi2S3,还含少量Bi2O3、SiO2等杂质)制备铋酸钠,其流程如图:

已知:①NaBiO3是一种难溶于水的物质②BiCl3极易水解生成不溶性的BiOCl沉淀。请回答下列问题:
(1)为了提高溶浸工序中原料的浸出率,可以采取的措施有______ (填标号)。
a.粉碎矿石 b.搅拌 c.加入足量的蒸馏水 d.降低温度
(2)滤渣A的主要成分为______ (填化学式),溶浸时通常加入FeCl3溶液和浓盐酸,加入的浓盐酸需过量的目的是______ 。
(3)通过反应③实现FeCl3的循环利用,写出该反应的离子方程式______ 。
(4)反应④的化学方程式为______ 。
(5)NaBiO3可在酸性介质中将Mn2+氧化为MnO ,故可用于Mn2+的鉴定。已知NaBiO3被还原为Bi3+,该反应的离子方程式为
,故可用于Mn2+的鉴定。已知NaBiO3被还原为Bi3+,该反应的离子方程式为______ 。
(6)实验室为了测定NaBiO3样品的纯度,需要配制250mL0.500mol/LFeSO4溶液,所需要的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要______ 。
(7)取上述NaBiO3样品10.0g,加入稀硫酸和MnSO4溶液使其完全溶解,稀释至100mL,取出20.00mL溶液,然后用新配制的0.500mol/LFeSO4溶液进行滴定,滴定完成后消耗24.80mLFeSO4溶液。则该样品中NaBiO3纯度为______ %(结果保留小数点后一位)。

已知:①NaBiO3是一种难溶于水的物质②BiCl3极易水解生成不溶性的BiOCl沉淀。请回答下列问题:
(1)为了提高溶浸工序中原料的浸出率,可以采取的措施有
a.粉碎矿石 b.搅拌 c.加入足量的蒸馏水 d.降低温度
(2)滤渣A的主要成分为
(3)通过反应③实现FeCl3的循环利用,写出该反应的离子方程式
(4)反应④的化学方程式为
(5)NaBiO3可在酸性介质中将Mn2+氧化为MnO
 ,故可用于Mn2+的鉴定。已知NaBiO3被还原为Bi3+,该反应的离子方程式为
,故可用于Mn2+的鉴定。已知NaBiO3被还原为Bi3+,该反应的离子方程式为(6)实验室为了测定NaBiO3样品的纯度,需要配制250mL0.500mol/LFeSO4溶液,所需要的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要
(7)取上述NaBiO3样品10.0g,加入稀硫酸和MnSO4溶液使其完全溶解,稀释至100mL,取出20.00mL溶液,然后用新配制的0.500mol/LFeSO4溶液进行滴定,滴定完成后消耗24.80mLFeSO4溶液。则该样品中NaBiO3纯度为
您最近一年使用:0次
4 . 以黄铁矿制硫酸产生的硫酸渣(含Fe2O3、Fe3O4、SiO2、Al2O3等)为原料制备纳米铁粉的部分工艺流程如下:
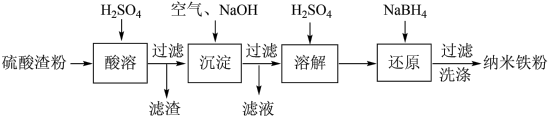
(1) “酸溶”过程中H2SO4过量的目的是____________ 。
(2) “沉淀”过程中空气参与反应的离子方程式为________ 。
(3) 为了确保纳米铁粉的纯度,“沉淀”过程需要调节溶液的pH的范围是3.2~3.5,其原因可能是________________ 。
(4) “还原”过程中加入NaBH4时,要同时通入氮气并不断搅拌,通入氮气的作用为___ 。
(5) 利用纳米铁粉可去除水体中的重金属Pb2+,中性条件下去除率最高,而酸性或碱性条件下去除率均有明显下降,如下图。

①酸性条件下,去除率下降的原因是____________ 。
②碱性条件下去除率下降的原因可能是____ (填字母)。
a. 纳米铁粉在碱性条件溶解
b. Pb2+在碱性条件生成沉淀
c. Pb2+在碱性条件生成的沉淀又被碱溶解

(1) “酸溶”过程中H2SO4过量的目的是
(2) “沉淀”过程中空气参与反应的离子方程式为
(3) 为了确保纳米铁粉的纯度,“沉淀”过程需要调节溶液的pH的范围是3.2~3.5,其原因可能是
(4) “还原”过程中加入NaBH4时,要同时通入氮气并不断搅拌,通入氮气的作用为
(5) 利用纳米铁粉可去除水体中的重金属Pb2+,中性条件下去除率最高,而酸性或碱性条件下去除率均有明显下降,如下图。

①酸性条件下,去除率下降的原因是
②碱性条件下去除率下降的原因可能是
a. 纳米铁粉在碱性条件溶解
b. Pb2+在碱性条件生成沉淀
c. Pb2+在碱性条件生成的沉淀又被碱溶解
您最近一年使用:0次
解题方法
5 . 铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。黑木耳中含有比较丰富的铁元素,某研究型学习小组同学测定某地黑木耳中铁的含量。
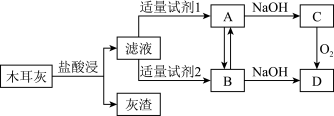
(1)称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。高温灼烧黑木耳,使之完全灰化。将木耳灰用上图流程处理,对滤液中的溶质进行研究。
①浸泡液检测不出铁元素的原因是_________ 。
②黑木耳放在______ (填仪器名称)中高温灼烧。
③滤液中铁元素的存在形式是Fe2+、_____ ;试剂l应该是_____ 。
(2)A转化为B可加入的试剂有_______ 。
a .酸性高锰酸钾 b .Cl2 c .H2O2 d .HNO3
(3)C生成D时的反应现象为___________ ,化学方程式为__________ ,当该反应转移8mol电子时,消耗标准状况下O2的体积为_______ L。
(4)若称取a g黑木耳全部烧成灰,将全部灰按照上面流程中加入试剂2的方法,全部转化为D,然后过滤、洗涤加热烘干、称得D质量为b g,_____ (填“能”或“不能”)准确测出该黑木耳铁元素的含量,理由是__________ 。

(1)称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。高温灼烧黑木耳,使之完全灰化。将木耳灰用上图流程处理,对滤液中的溶质进行研究。
①浸泡液检测不出铁元素的原因是
②黑木耳放在
③滤液中铁元素的存在形式是Fe2+、
(2)A转化为B可加入的试剂有
a .酸性高锰酸钾 b .Cl2 c .H2O2 d .HNO3
(3)C生成D时的反应现象为
(4)若称取a g黑木耳全部烧成灰,将全部灰按照上面流程中加入试剂2的方法,全部转化为D,然后过滤、洗涤加热烘干、称得D质量为b g,
您最近一年使用:0次
6 . 某同学用KSCN溶液和FeCl2溶液探究Fe2+的还原性时出现异常现象,实验如下:
下列说法错误的是( )
| ① | ② | ③ |
 | 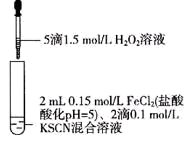 |  |
| 溶液变红,大约10秒左右红色褪去,有气体生成(经检验为O2)。取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀 | 溶液变红且不褪色,有气体生成(经检验为O2),经检验有丁达尔效应。 | 溶液变红且不褪色,滴加盐酸和BaCl2溶液,无白色沉淀,经检验无丁达尔效应。 |
| A.②中红色溶液中含有Fe(OH)3胶体 |
| B.实验②中发生的氧化还原反应只有两种 |
| C.对比①②③,可以判定酸性条件下H2O2可以氧化SCN- |
| D.③中发生的氧化还原反应为:4Fe2++O2+4H+=4Fe3++2H2O |
您最近一年使用:0次
2020-11-03更新
|
1833次组卷
|
15卷引用:山西省太原市第五中学2020届高三10月月考化学试题
山西省太原市第五中学2020届高三10月月考化学试题2020届高考化学知识点必练——氧化还原反应的本质及相关概念2020届高三化学化学二轮复习——高考常考题:情境下氧化还原反应方程式书写【精编选择26题】北京市延庆区2019届高三第一次模拟考试化学试题山东省师范大学附属中学2021届高三上学期第二次考试化学试题辽宁省大连市一〇三中学2021届高三一模考试化学试题黑龙江省哈尔滨市第六中学2020-2021学年高一12月月考化学试题(已下线)【浙江新东方】在线化学13江西省南昌市南昌县莲塘第一中学2021届高三上学期12月质量检测化学试题(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)山东省潍坊市实验中学2021-2022学年高三9月单元测试(入学考试)化学试题武汉市第一中学2021-2022学年高三上学期10月月考化学试题重庆市缙云教育联盟2023-2024学年高三下学期8月月考化学试题重庆市乌江新高考协作体2023-2024学年高一上学期11月期中化学试题
名校
解题方法
7 . 某溶液X中可能含有 、
、 、
、 、
、 、
、 、
、 和
和 中的几种,且所含阴离子的物质的量相等。为确定该溶液X的成分,某学习小组做了如下实验,下列说法错误的是
中的几种,且所含阴离子的物质的量相等。为确定该溶液X的成分,某学习小组做了如下实验,下列说法错误的是

 、
、 、
、 、
、 、
、 、
、 和
和 中的几种,且所含阴离子的物质的量相等。为确定该溶液X的成分,某学习小组做了如下实验,下列说法错误的是
中的几种,且所含阴离子的物质的量相等。为确定该溶液X的成分,某学习小组做了如下实验,下列说法错误的是
A.产生气体乙的方程式为: |
| B.气体甲能使湿润的红色石蕊试纸变蓝 |
C. 、 、 一定存在, 一定存在, 和 和 可能都存在 可能都存在 |
D.该溶液中只存在上述离子中的 、 、 、 、 、 、 四种离子 四种离子 |
您最近一年使用:0次
2020-10-26更新
|
685次组卷
|
3卷引用:吉林省东北师大附中2019-2020学年高三上学期第三次摸底考试化学试题
解题方法
8 . 下列能正确描述其反应的离子方程式的是( )
A.向(NH4)2Fe(SO4)2溶液中加入硝酸酸化的Ba(NO3)2:Ba2++SO =BaSO4↓ =BaSO4↓ |
B.向Ca(HCO3)2溶液中加入过量的NaOH:Ca2++HCO +OH-=CaCO3↓+H2O +OH-=CaCO3↓+H2O |
C.向KMnO4溶液中加入浓盐酸:2MnO +16H++10Cl-=2Mn2++5Cl2↑+8H2O +16H++10Cl-=2Mn2++5Cl2↑+8H2O |
D.向NaAlO2与NaOH的混合溶液中通入少量CO2:AlO +CO2+2H2O=Al(OH)3↓+HCO +CO2+2H2O=Al(OH)3↓+HCO |
您最近一年使用:0次
名校
解题方法
9 . 实验室以绿矾(FeSO4●7H2O)制备补血剂甘氨酸亚铁[(NH2CH2COO)2Fe],有关物质性质如下:
实验过程:
I.配制含0.10molFeSO4的绿矾溶液。
II.制备FeCO3:向配制好的绿矾溶液中,缓慢加入200mL1.1mol/LNH4HCO3溶液,边加边搅拌,反应结束后过滤并洗涤沉淀。
III.制备(NH2CH2COO)2Fe:实验装置如下图(夹持和加热仪器略去),将实验II得到的沉淀和含0.20mol甘氨酸的水溶液混合后加入C中,然后利用A中的反应将C中空气排净,接着滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品。
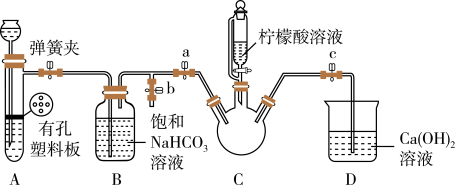
回答下列问题:
(1)实验I中:实验室配制绿矾溶液时,为防止FeSO4被氧化变质,应加入的试剂为________ (写化学式)。
(2)实验II中:生成沉淀的离子方程式为__________ 。
(3)实验III中:①C中盛柠檬酸溶液的仪器名称为__________ 。
②装置A中所盛放的试剂是________ (填字母)。
A.Na2CO3和稀H2SO4B.CaCO3和稀H2SO4C.CaCO3和稀盐酸
③确认C中空气排尽的实验现象是_________ 。
④加入柠檬酸溶液一方面可调节溶液的pH促进FeCO3溶解,另一个作用是_________ 。
⑤洗涤实验II中得到的沉淀,所选用的最佳洗涤试剂是________ 。(填字母)
A.热水B.乙醇溶液C.柠檬酸溶液
⑥若产品的质量为17.34g,则产率为__________ %。
| 甘氨酸(NH2CH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
| 易溶于水,微溶于乙醇,两性化合物 | 易溶于水和乙醇,有强酸性和还原性 | 易溶于水,难溶于乙醇 |
实验过程:
I.配制含0.10molFeSO4的绿矾溶液。
II.制备FeCO3:向配制好的绿矾溶液中,缓慢加入200mL1.1mol/LNH4HCO3溶液,边加边搅拌,反应结束后过滤并洗涤沉淀。
III.制备(NH2CH2COO)2Fe:实验装置如下图(夹持和加热仪器略去),将实验II得到的沉淀和含0.20mol甘氨酸的水溶液混合后加入C中,然后利用A中的反应将C中空气排净,接着滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品。

回答下列问题:
(1)实验I中:实验室配制绿矾溶液时,为防止FeSO4被氧化变质,应加入的试剂为
(2)实验II中:生成沉淀的离子方程式为
(3)实验III中:①C中盛柠檬酸溶液的仪器名称为
②装置A中所盛放的试剂是
A.Na2CO3和稀H2SO4B.CaCO3和稀H2SO4C.CaCO3和稀盐酸
③确认C中空气排尽的实验现象是
④加入柠檬酸溶液一方面可调节溶液的pH促进FeCO3溶解,另一个作用是
⑤洗涤实验II中得到的沉淀,所选用的最佳洗涤试剂是
A.热水B.乙醇溶液C.柠檬酸溶液
⑥若产品的质量为17.34g,则产率为
您最近一年使用:0次
解题方法
10 . 纳米铜是一种性能优质的超导材料,以辉铜矿(主要成分为Cu2S)为原料制备纳米铜粉的工艺流程如图所示。

资料:肼(N2H4)无色油状液体,溶于水生成水合肼N2H4·H2O(水合肼有强还原性,生成无污染物质,易挥发)
(1)①上述流程中可以加快反应速率的措施有______ 。
A.过滤和萃取 B.升高温度 C.增大压强 D.研磨矿石
②用FeCl3溶液浸取辉铜矿中铜元素的反应为:Cu2S+4FeCl3=2CuCl2+4FeCl2+S。浸取时,在有氧的环境下可维持Fe3+较高浓度,有关反应的离子方程式为_______ 。
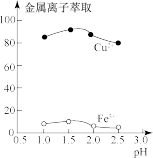
(2)“萃取”时,两种金属离子萃取率与pH的关系如图所示。当pH>1.7时,pH越大,金属离子萃取率越低,其中Fe3+萃取率降低的原因是______ 。
(3)“反萃取”得到的CuSO4溶液制备纳米铜粉时,Cu2+的还原率随pH和温度的变化如下表所示:
①该反应的离子方程式为_______ 。
②超过70℃时Cu2+的还原率降低的原因是______ 。
③以辉铜矿为原料制备纳米铜粉的工艺条件选择70℃、pH=10的理由是______ 。
(4)“水相1”中加入适量氨水,静置,再经过滤、_____ 、干燥、______ 等操作可得到Fe2O3。
(5)假设制得纳米铜的质量为akg,则最少投入肼的物质的量是______ 。

资料:肼(N2H4)无色油状液体,溶于水生成水合肼N2H4·H2O(水合肼有强还原性,生成无污染物质,易挥发)
(1)①上述流程中可以加快反应速率的措施有
A.过滤和萃取 B.升高温度 C.增大压强 D.研磨矿石
②用FeCl3溶液浸取辉铜矿中铜元素的反应为:Cu2S+4FeCl3=2CuCl2+4FeCl2+S。浸取时,在有氧的环境下可维持Fe3+较高浓度,有关反应的离子方程式为
(2)“萃取”时,两种金属离子萃取率与pH的关系如图所示。当pH>1.7时,pH越大,金属离子萃取率越低,其中Fe3+萃取率降低的原因是

(3)“反萃取”得到的CuSO4溶液制备纳米铜粉时,Cu2+的还原率随pH和温度的变化如下表所示:
| pH | 6 | 7 | 8 | 9 | 10 | 11 | 12 | |
| Cu2+还原率(%) | 34 | 60 | 90 | 92 | 95 | 92 | 90 | |
| 产物形态 | 砖红色Cu2O | 铜粉 | 紫黑色纳米铜 | |||||
| 温度 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | |
| Cu2+还原率(%) | 25 | 45 | 70 | 80 | 95 | 90 | 85 | |
| 产物形态 | 砖红色Cu2O | 铜粉 | 紫黑色纳米铜 | |||||
①该反应的离子方程式为
②超过70℃时Cu2+的还原率降低的原因是
③以辉铜矿为原料制备纳米铜粉的工艺条件选择70℃、pH=10的理由是
(4)“水相1”中加入适量氨水,静置,再经过滤、
(5)假设制得纳米铜的质量为akg,则最少投入肼的物质的量是
您最近一年使用:0次



