宁夏回族自治区银川市宁夏长庆高级中学2021届高三上学期第四次月考理综化学试题
宁夏
高三
阶段练习
2021-01-05
223次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、化学反应原理、化学实验基础、认识化学科学、物质结构与性质、有机化学基础
宁夏回族自治区银川市宁夏长庆高级中学2021届高三上学期第四次月考理综化学试题
宁夏
高三
阶段练习
2021-01-05
223次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、化学反应原理、化学实验基础、认识化学科学、物质结构与性质、有机化学基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
解题方法
1. 化学来源于生活,也服务于生活,下列有关生活中的化学叙述正确的是
| A.纤维素与合成纤维的成分相同 |
| B.在含硫的燃料中加入适量生石灰,以减少二氧化硫的排放量 |
| C.光导纤维中所用材料为晶体硅 |
| D.NOx、SO2、CO2、PM2.5颗粒都会导致酸雨 |
您最近一年使用:0次
2. 下列实验操作能达到实验目的的是


| A.用装置甲从碘水中萃取碘 |
| B.用装置乙验证SO2的漂白性 |
| C.用装置丙检验溶液中是否有K+ |
| D.用装置丁将MgCl2溶液蒸干制备MgCl2 |
您最近一年使用:0次
2020-12-28更新
|
177次组卷
|
2卷引用:宁夏回族自治区银川市宁夏长庆高级中学2021届高三上学期第四次月考理综化学试题
单选题
|
适中(0.65)
名校
解题方法
3. 下列离子方程式正确的是
A.向Na2SiO3溶液中通入过量CO2:Na2SiO3+2CO2+2H2O=H2SiO3↓+2HCO +2Na+ +2Na+ |
B.KClO碱性溶液与Fe(OH)3反应:3ClO−+2Fe(OH)3=2FeO +3Cl−+4H++H2O +3Cl−+4H++H2O |
| C.用KSCN溶液检验某溶液中含有Fe3+:Fe3++3SCN-=Fe(SCN)3↓ |
D.酸性介质中KMnO4氧化H2O2:2MnO +5H2O2+6H+=2Mn2++5O2↑+8H2O +5H2O2+6H+=2Mn2++5O2↑+8H2O |
【知识点】 离子方程式的正误判断解读
您最近一年使用:0次
2020-12-28更新
|
121次组卷
|
2卷引用:宁夏回族自治区银川市宁夏长庆高级中学2021届高三上学期第四次月考理综化学试题
单选题
|
适中(0.65)
名校
4. NA为阿伏加德罗常数的值。下列说法中正确的是
| A.1 mol SiO2与足量的焦炭高温下完全反应生成Si,转移2NA个电子 |
| B.将6 g H2与足量的N2混合,充分反应后生成NH3分子数为2NA |
| C.20gD216O中含有的中子数目为10NA |
| D.常温下,2.7 g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
5. 短周期主族元素W、X、Y、Z的原子序数依次增大,W原子的最外层电子数是内层电子总数的2倍,X、Z同主族且质子数之比为1:2,Y的最高价氧化物对应的水化物属于中强碱。下列说法正确的是
| A.简单离子半径:Z>X>Y |
| B.常温下,W的氢化物均为气体 |
| C.Z的氧化物的水化物一定是强酸 |
| D.工业上常用电解熔融YX的方法冶炼Y单质 |
您最近一年使用:0次
2020-12-28更新
|
195次组卷
|
3卷引用:宁夏回族自治区银川市宁夏长庆高级中学2021届高三上学期第四次月考理综化学试题
单选题
|
适中(0.65)
名校
6. 已知: 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是| A.异丙烯苯转化为异丙苯属于加成反应 |
| B.异丙苯能与溴水发生取代反应 |
| C.异丙烯苯分子中所有的碳原子可能共平面 |
| D.异丙苯的一氯代物有5种(不考虑立体异构) |
【知识点】 同分异构体的数目的确定解读 烯烃 有机分子中原子共面的判断解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
7. 某稀溶液中含有3.5 mol KNO3和2.2 mol H2SO4,向其中加入1.2 mol Fe,充分反应(已知NO 被还原为NO)。下列说法正确的是
被还原为NO)。下列说法正确的是
 被还原为NO)。下列说法正确的是
被还原为NO)。下列说法正确的是| A.反应过程中转移的电子数3NA |
| B.反应后生成NO的体积为24.64 L |
| C.所得溶液中c(Fe2+)∶c(Fe3+)=1∶3 |
| D.所得溶液中c(NO3-)=2.4 mol·L-1 |
您最近一年使用:0次
2019-11-06更新
|
186次组卷
|
5卷引用:宁夏银川一中2020届高三第三次月考理综化学试题
二、解答题 添加题型下试题
解答题-无机推断题
|
适中(0.65)
名校
8. A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A、E在元素周期表中的相对位置如图,A与氧元素能形成两种无色气体,C是地壳中含量最多的元素,D是地壳中含量最多的金属元素。
(1)C在元素周期表中的位置为______ ,其离子的结构示意图为______ 。
(2)AE2的电子式为______ 。
(3)元素B与氢元素能形成含有18个电子的分子,其中含有的化学键有______ 、______ 。
(4)A、B、C最简单氢化物的稳定性由强到弱的顺序是______ (填分子式)。
(5)实验室制取F2气体的离子方程式为______ 。
(6)在微电子工业中,B的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为______ 。
(7)DF3的水溶液可作净水剂,写出有关的离子方程式______ 。
| A | ||
| E |
(2)AE2的电子式为
(3)元素B与氢元素能形成含有18个电子的分子,其中含有的化学键有
(4)A、B、C最简单氢化物的稳定性由强到弱的顺序是
(5)实验室制取F2气体的离子方程式为
(6)在微电子工业中,B的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为
(7)DF3的水溶液可作净水剂,写出有关的离子方程式
您最近一年使用:0次
2020-12-28更新
|
270次组卷
|
4卷引用:宁夏回族自治区银川市宁夏长庆高级中学2021届高三上学期第四次月考理综化学试题
宁夏回族自治区银川市宁夏长庆高级中学2021届高三上学期第四次月考理综化学试题(已下线)解密05 物质结构元素周期律(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密05 物质结构元素周期律(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练宁夏青铜峡市宁朔中学2023-2024学年高三上学期第四次月考理科综合试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
9. 氨气在工农业生产中有重要应用。
(1)制取氨气并完成喷泉实验(图中夹持装置均已略去)。
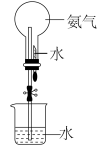
①写出实验室制取氨气的化学方程式______ 。要得到干燥的氨气可选用______ 做干燥剂。
②用上图装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是______ 。
(2)如图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。
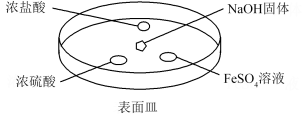
浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是______ 。(写化学式,一种即可)。
(3)氨气催化氧化可以生成NO,如图所示将相同条件下的m体积NO和n体积O2同时通入倒立于水槽中且盛满水的试管内,充分反应后,试管内残留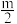 体积的气体,该气体与空气接触后立即变为红棕色。则m与n的比值为
体积的气体,该气体与空气接触后立即变为红棕色。则m与n的比值为______ 。

(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为______ ,若反应中有0.3mol电子发生转移,生成亚硝酸的质量为______ g(保留两位小数)。
(1)制取氨气并完成喷泉实验(图中夹持装置均已略去)。

①写出实验室制取氨气的化学方程式
②用上图装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操作是
(2)如图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是
(3)氨气催化氧化可以生成NO,如图所示将相同条件下的m体积NO和n体积O2同时通入倒立于水槽中且盛满水的试管内,充分反应后,试管内残留
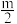 体积的气体,该气体与空气接触后立即变为红棕色。则m与n的比值为
体积的气体,该气体与空气接触后立即变为红棕色。则m与n的比值为
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
名校
解题方法
10. 铋酸钠(NaBiO3)常用作Mn2+鉴定的强氧化剂,某研究小组用浮选过的辉铋矿(主要成分是Bi2S3,还含少量Bi2O3、SiO2等杂质)制备铋酸钠,其流程如图:

已知:①NaBiO3是一种难溶于水的物质②BiCl3极易水解生成不溶性的BiOCl沉淀。请回答下列问题:
(1)为了提高溶浸工序中原料的浸出率,可以采取的措施有______ (填标号)。
a.粉碎矿石 b.搅拌 c.加入足量的蒸馏水 d.降低温度
(2)滤渣A的主要成分为______ (填化学式),溶浸时通常加入FeCl3溶液和浓盐酸,加入的浓盐酸需过量的目的是______ 。
(3)通过反应③实现FeCl3的循环利用,写出该反应的离子方程式______ 。
(4)反应④的化学方程式为______ 。
(5)NaBiO3可在酸性介质中将Mn2+氧化为MnO ,故可用于Mn2+的鉴定。已知NaBiO3被还原为Bi3+,该反应的离子方程式为
,故可用于Mn2+的鉴定。已知NaBiO3被还原为Bi3+,该反应的离子方程式为______ 。
(6)实验室为了测定NaBiO3样品的纯度,需要配制250mL0.500mol/LFeSO4溶液,所需要的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要______ 。
(7)取上述NaBiO3样品10.0g,加入稀硫酸和MnSO4溶液使其完全溶解,稀释至100mL,取出20.00mL溶液,然后用新配制的0.500mol/LFeSO4溶液进行滴定,滴定完成后消耗24.80mLFeSO4溶液。则该样品中NaBiO3纯度为______ %(结果保留小数点后一位)。

已知:①NaBiO3是一种难溶于水的物质②BiCl3极易水解生成不溶性的BiOCl沉淀。请回答下列问题:
(1)为了提高溶浸工序中原料的浸出率,可以采取的措施有
a.粉碎矿石 b.搅拌 c.加入足量的蒸馏水 d.降低温度
(2)滤渣A的主要成分为
(3)通过反应③实现FeCl3的循环利用,写出该反应的离子方程式
(4)反应④的化学方程式为
(5)NaBiO3可在酸性介质中将Mn2+氧化为MnO
 ,故可用于Mn2+的鉴定。已知NaBiO3被还原为Bi3+,该反应的离子方程式为
,故可用于Mn2+的鉴定。已知NaBiO3被还原为Bi3+,该反应的离子方程式为(6)实验室为了测定NaBiO3样品的纯度,需要配制250mL0.500mol/LFeSO4溶液,所需要的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要
(7)取上述NaBiO3样品10.0g,加入稀硫酸和MnSO4溶液使其完全溶解,稀释至100mL,取出20.00mL溶液,然后用新配制的0.500mol/LFeSO4溶液进行滴定,滴定完成后消耗24.80mLFeSO4溶液。则该样品中NaBiO3纯度为
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
名校
解题方法
11. 锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为______ ,有______ 个未成对电子。Ge在周期表中的位置______ 。
(2)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Ge、O两元素电负性由大至小的顺序是______ 。C、O两元素第一电离能由小到大的顺序是______ 。
(3)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为______ ,微粒之间存在的作用力是______ 。
(4)晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76 pm,其密度为______ g·cm-3(列出计算式即可,不必计算出具体数值)。

(1)基态Ge原子的核外电子排布式为
(2)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Ge、O两元素电负性由大至小的顺序是
(3)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(4)晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76 pm,其密度为

您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
名校
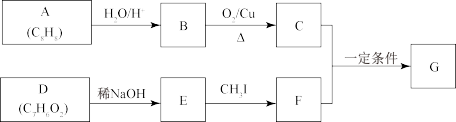
12. 查尔酮类化合物G是黄酮类药物的主要合成中间体,其中一种合成路线如下:
(1)A的结构简式为_____ ,D中含氧官能团的名称为______ 。
(2)由A生成B的反应类型为_______ 。
(3)由B生成C的化学方程式为__________ 。
(4)G的结构简式为________ 。
(5)写出化合物F同时符合下列条件的同分异构体的结构简式:________ 。
①苯环上有2个对位取代基 ②能发生银镜反应 ③能发生水解反应
②
③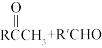

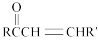 +H2O
+H2O
(1)A的结构简式为
(2)由A生成B的反应类型为
(3)由B生成C的化学方程式为
(4)G的结构简式为
(5)写出化合物F同时符合下列条件的同分异构体的结构简式:
①苯环上有2个对位取代基 ②能发生银镜反应 ③能发生水解反应
(6)以甲苯和丙酮( )为原料,设计制备有机物
)为原料,设计制备有机物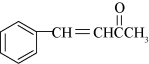 的合成路线:
的合成路线:
您最近一年使用:0次
2020-11-18更新
|
338次组卷
|
4卷引用:广东省汕头市金山中学2021届高三上学期期中考试化学试题
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、化学与STSE、化学反应原理、化学实验基础、认识化学科学、物质结构与性质、有机化学基础
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 硫、氮氧化物对人体、环境的危害 酸雨 化学科学对人类文明发展的意义 大气污染的治理原理及方法 光导纤维与硅芯片 | |
| 2 | 0.65 | 二氧化硫 制备与水解有关的物质 物质的分离、提纯 实验方案设计的基本要求 | |
| 3 | 0.65 | 离子方程式的正误判断 | |
| 4 | 0.65 | 阿伏加德罗常数的应用 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 可逆反应及反应限度 | |
| 5 | 0.65 | 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 | |
| 6 | 0.65 | 同分异构体的数目的确定 烯烃 有机分子中原子共面的判断 | |
| 7 | 0.65 | 硝酸盐的氧化性 | |
| 二、解答题 | |||
| 8 | 0.65 | 元素周期律、元素周期表的推断 同周期元素性质递变规律理解及应用 “位构性”关系理解及应用 共价键概念及判断 | 无机推断题 |
| 9 | 0.65 | 氨的喷泉实验 氨气的实验室制法 氮氧化物溶解于水的相关计算 物质性质的探究 | 实验探究题 |
| 10 | 0.4 | 基于氧化还原反应守恒规律的计算 Fe2+的还原性 常见无机物的制备 | 工业流程题 |
| 11 | 0.65 | 核外电子排布的表示形式 电离能变化规律 利用杂化轨道理论判断化学键杂化类型 晶胞的有关计算 | 结构与性质 |
| 12 | 0.65 | 有机物的推断 根据题给物质选择合适合成路线 有机合成综合考查 有机推断综合考查 | 有机推断题 |



