解题方法
1 . 与石墨结构相似的六方氮化硼(BN)晶体在高温高压下可以转化为立方氮化硼(BN),立方氮化硼的结构与金刚石相似,硬度与金刚石相当。下列关于该物质的分析中正确的是
| A.六方氮化硼转化为立方氮化硼是物理变化 |
B.立方氮化硼(BN)中氮元素的化合价为 |
C.和 键相比, 键相比, 键的键长更长 键的键长更长 |
| D.立方氮化硼比晶体硅的熔点更高,硬度更大 |
您最近一年使用:0次
2021-09-22更新
|
538次组卷
|
4卷引用:2021年湖北高考化学试题变式题1-10
2021年湖北高考化学试题变式题1-10福建泉州市第六中学2020-2021学年高二下学期期中考试化学试题3.2.2 共价晶体-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)(已下线)第3.2.2讲 共价晶体-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)
2 . 工业上常用反应 制备粗硅,若碳过量还会生成SiC,下列说法正确的是
制备粗硅,若碳过量还会生成SiC,下列说法正确的是
 制备粗硅,若碳过量还会生成SiC,下列说法正确的是
制备粗硅,若碳过量还会生成SiC,下列说法正确的是| A.相对分子质量:C60>SiO2>SiC,因此熔沸点:C60>SiO2>SiC |
| B.SiH4中Si的化合价为+4价,CH4中C的化合价为-4价,因此SiH4还原性小于CH4 |
| C.Si原子间难形成双键而C原子间可以,是因为Si的原子半径大于C,难形成p-pπ键 |
| D.键能:Si—H<C—H,Si—Si<C—C,因此硅烷的种类和数量远不如烷烃的多 |
您最近一年使用:0次
2021-08-04更新
|
483次组卷
|
2卷引用:2021年海南高考化学试题变式题11-19
真题
解题方法
3 . (1)已知3种原子晶体的熔点数据如下表:
金刚石熔点比晶体硅熔点高的原因是_______ 。
(2)提纯含有少量氯化钠的甘氨酸样品:将样品溶于水,调节溶液的pH使甘氨酸结晶析出,可实现甘氨酸的提纯。其理由是_______ 。
| 金刚石 | 碳化硅 | 晶体硅 | |
| 熔点/℃ | >3550 | 2600 | 1415 |
(2)提纯含有少量氯化钠的甘氨酸样品:将样品溶于水,调节溶液的pH使甘氨酸结晶析出,可实现甘氨酸的提纯。其理由是
您最近一年使用:0次
2021-06-15更新
|
3658次组卷
|
9卷引用:2021年6月浙江高考化学试题变式题26-31
(已下线)2021年6月浙江高考化学试题变式题26-312021年6月新高考浙江化学高考真题(已下线)考点08 分子间作用力 氢键-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点08 微粒间作用力-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题08.微粒间相互作用力-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)解密05 物质结构 元素周期律(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密05 物质结构 元素周期律(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)考点08 微粒间相互作用力-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点08 微粒间相互作用力(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
解题方法
4 . 下表为C、 形成的部分化学键的键能数据。下列说法错误的是
形成的部分化学键的键能数据。下列说法错误的是
 形成的部分化学键的键能数据。下列说法错误的是
形成的部分化学键的键能数据。下列说法错误的是| 化学键 |  |  | 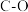 |  |  | 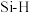 |  |
键能/( ) ) | 347 | 413 | 358 | 803 | 226 | 318 | 452 |
A.键能: ,因此硬度:金刚石 ,因此硬度:金刚石 晶体硅 晶体硅 |
B.键能 ,因此熔点: ,因此熔点: |
| C. CH4的热稳定性大于SiH4,且二者燃烧的产物中SiO2更容易形成 |
D. CH4与SiH4分子中所含元素的电负性: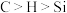 |
您最近一年使用:0次
2021-04-10更新
|
1019次组卷
|
6卷引用:山东省济南市2021届高三一模化学试题
山东省济南市2021届高三一模化学试题(已下线)第17讲 化学能与热能(精讲)-2022年一轮复习讲练测(已下线)专题13 物质结构与性质基础-备战2022年高考化学真题及地市好题专项集训【山东专用】辽宁省渤海大学附属高级中学2021-2022学年高二下学期阶段性考试化学试题(已下线)2020年山东卷化学高考真题变式题1-10(已下线)2022年山东省高考真题变式题(单选题)
解题方法
5 . 下列说法中错误的是


A. 和 和 的结构相似都属于原子(共价)晶体,熔点 的结构相似都属于原子(共价)晶体,熔点 |
B.B与 的单质性质差异很大,B单质不能与强碱水溶液反应 的单质性质差异很大,B单质不能与强碱水溶液反应 |
C.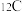 和 和 的价层电子排布相同 的价层电子排布相同 |
| D.如图所示银的晶胞中含有4个银原子 |
您最近一年使用:0次
名校
6 . B和Al为同族元素,下列说法错误的是
A. 和 和 都可以与 都可以与 形成配位键 形成配位键 |
B. 为三元酸, 为三元酸, 呈两性 呈两性 |
| C.共价键的方向性使晶体B有脆性,原子层的相对滑动使金属Al有延展性 |
| D.B和Al分别与N形成的共价晶体,均具有较高硬度和熔点 |
您最近一年使用:0次
2021-01-25更新
|
880次组卷
|
3卷引用:湖北省2021年普通高中学业水平选择考适应性测试化学试题
解题方法
7 . Al2O3可以从铝土矿中获得,铝土矿的主要成分为Al2O3,含Fe2O3、SiO2等杂质。经过“酸溶法”或“碱溶法”等都可以去掉杂质得到Al2O3。19世纪后期,美国的霍尔和法国的埃鲁先后独立发明了电解Al2O3法生产铝。2Al2O3 4Al+3O2↑[冰晶石(Na3AlF6)作助熔剂,降低氧化铝熔点]
4Al+3O2↑[冰晶石(Na3AlF6)作助熔剂,降低氧化铝熔点]
(1)上述涉及到Al、Na、O、F、Si、Fe六种元素中,不是主族元素的是___________ ,Al3+电子排布式___________ ,O原子的未成对电子数___________ 。
(2)制造“中国芯”芯片的核心元素Si位于元素周期表第___________ 周期第___________ 族。冰晶石(Na3AlF6)晶体中阴、阳离子各一种,阴离子符号___________ 。
(3)用“>”或“<”填空:
(4)用离子晶体的知识解释Al2O3比Na2O熔点高的原因_________ 。
(5)其实电解法生产铝有很多弊端,科技工作者不断创新。下面一种新型直接从铝土矿中提取铝的方法
I.Al2O3(s)+AlCl3(g)+3C(s) 3 AlCl(g)+ 3CO(g) -1486kJ
3 AlCl(g)+ 3CO(g) -1486kJ
II.3 AlCl(g) 2 Al(l)+ AlCl3(g) +140 kJ
2 Al(l)+ AlCl3(g) +140 kJ
①反应I中的还原产物是___________ ;若有0.6gC反应,电子转移数目为___________
②结合反应I、II分析,请说出这种提炼方法2条优点___________ ___________ 。
 4Al+3O2↑[冰晶石(Na3AlF6)作助熔剂,降低氧化铝熔点]
4Al+3O2↑[冰晶石(Na3AlF6)作助熔剂,降低氧化铝熔点](1)上述涉及到Al、Na、O、F、Si、Fe六种元素中,不是主族元素的是
(2)制造“中国芯”芯片的核心元素Si位于元素周期表第
(3)用“>”或“<”填空:
原子半径 | 非金属性 | 熔点 |
| Al | O | 二氧化硅 |
(4)用离子晶体的知识解释Al2O3比Na2O熔点高的原因
(5)其实电解法生产铝有很多弊端,科技工作者不断创新。下面一种新型直接从铝土矿中提取铝的方法
I.Al2O3(s)+AlCl3(g)+3C(s)
 3 AlCl(g)+ 3CO(g) -1486kJ
3 AlCl(g)+ 3CO(g) -1486kJII.3 AlCl(g)
 2 Al(l)+ AlCl3(g) +140 kJ
2 Al(l)+ AlCl3(g) +140 kJ①反应I中的还原产物是
②结合反应I、II分析,请说出这种提炼方法2条优点
您最近一年使用:0次



