解题方法
1 . 物质的结构决定物质的性质。下列性质差异与结构因素匹配正确的是
| 选项 | 性质差异 | 结构因素 |
| A | 键角:CH4(109°28′)大于NH3(107.3°) | 中心原子杂化方式 |
| B | 摩氏硬度:金刚石(10) 石英(7) 石英(7) | 晶体类型 |
| C | 酸性:CF3COOH(pKa=0.23)>CCl3COOH(pKa=0.65) | 羟基极性 |
| D | 苯酚的溶解度:高于65℃时(能与水互溶) 室温时(9.2g) 室温时(9.2g) | 电离程度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 如表所示为部分化学键的键能数据,由键能数据大小,不能解释下列事实的是
| 化学键 |  |  |  |  |  |  |  |  |
键能 | 413 | 348 | 745 | 326 | 318 | 226 | 452 | 347 |
A.硬度:金刚石 碳化硅 碳化硅 |
| B.熔、沸点:金刚石>CO2 |
| C.SiH4的稳定性小于CH4,更易生成氧化物 |
| D.硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多 |
您最近一年使用:0次
3 . 下列有关物质结构与性质的说法错误的是
A. 比 比 稳定,是由于 稳定,是由于 分子间存在氢键,而 分子间存在氢键,而 分子间不存在氢键 分子间不存在氢键 |
| B.Zn的第一电离能大于Ga,是由于Zn的价层电子排布是全充满的,比较稳定 |
C. 溶于氨水,是由于 溶于氨水,是由于 与 与 反应生成了可溶性配合物 反应生成了可溶性配合物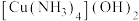 |
| D.金刚石可用作地质钻探钻头,是由于金刚石具有很高的硬度 |
您最近一年使用:0次
4 . 某长石矿物的化学式为 ,
,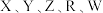 是原子序数依次增大的前20号主族元素。元素Z、W是常见的金属元素,元素R在地壳中的含量仅次于元素Y。下列说法错误的是
是原子序数依次增大的前20号主族元素。元素Z、W是常见的金属元素,元素R在地壳中的含量仅次于元素Y。下列说法错误的是
 ,
,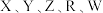 是原子序数依次增大的前20号主族元素。元素Z、W是常见的金属元素,元素R在地壳中的含量仅次于元素Y。下列说法错误的是
是原子序数依次增大的前20号主族元素。元素Z、W是常见的金属元素,元素R在地壳中的含量仅次于元素Y。下列说法错误的是| A.X、Y形成的二元化合物常温常压下呈液态 |
B.Z、W最高价氧化物对应水化物的碱性; |
| C.X、Y、Z、R四种元素形成的单质中,R熔点最高 |
| D.Z、R、W最高价氧化物对应的水化物之间均可发生反应 |
您最近一年使用:0次
5 . 化学和生活、科技、社会发展息息相关,下列说法错误的是
A.神舟系列飞船返回舱使用氮化硅耐高温材料, 属于共价晶体 属于共价晶体 |
| B.三星堆黄金面具出土时光亮且薄如纸,说明金不活泼和有良好的延展性 |
C.利用 合成了高级脂肪酸,实现了无机小分子向有机高分子的转变 合成了高级脂肪酸,实现了无机小分子向有机高分子的转变 |
D.高铁酸钾( )对饮用水有杀菌消毒和净化的作用 )对饮用水有杀菌消毒和净化的作用 |
您最近一年使用:0次
6 . 金刚石有重要的应用,科学家不断研究制备金刚石的方法。
方法Ⅰ:C(石墨) C(金刚石)
C(金刚石) 
方法Ⅱ: (金刚石)
(金刚石)
下列说法正确的是
方法Ⅰ:C(石墨)
 C(金刚石)
C(金刚石) 
方法Ⅱ:
 (金刚石)
(金刚石)下列说法正确的是
| A.金刚石和石墨互称为同位素 |
| B.金刚石和石墨中粒子间的作用力类型相同 |
| C.键长:Si-C键<C-C键(金刚石) |
| D.熔点:SiC<C(金刚石) |
您最近一年使用:0次
2024·黑龙江·模拟预测
解题方法
7 . 下列叙述中,事实与对应解释错误的是
| 事实 | 解释 | |
| A | 酸性:HCOOH > CH3COOH | H3C-是推电子基团,使羧基中羟基的极性减小 |
| B | 在水中的溶解度:乙醇 > 戊醇 | 乙醇分子结构与水具有相似性,而戊醇分子结构与水的相似性较小 |
| C | 硬度:金刚石>石墨 | 金刚石属于共价晶体只含共价键,石墨属于混合型晶体,既存在共价键又存在范德华力 |
| D | 热稳定性:H2O>H2S | 水分子间存在氢键作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 化学推动科技进步。下列说法不正确的是
| A.华为自主研发的“麒麟”芯片与太阳能电池感光板所用的主要材料均为晶体硅 |
| B.杭州亚运会场馆使用的“碲化镉”光伏发电系统将化学能转化为电能 |
C.“神舟十七号”发动机的耐高温结构材料 属于共价晶体 属于共价晶体 |
| D.“深海一号”母船海水浸泡区镶上铝基是利用了牺牲阳极的金属防腐原理 |
您最近一年使用:0次
解题方法
9 . 硼酸晶体有类似于石墨的片层状结构。下列说法不正确的是
| A.氧化铍熔点较高,可用作耐火材料 |
| B.电解熔融氯化铍制备铍单质 |
| C.用碳原子取代晶体硅中部分原子,硬度变大 |
D.不慎将碱液沾到皮肤上,立即用大量水冲洗,再涂上 的硼酸 的硼酸 |
您最近一年使用:0次
名校
解题方法
10 . 中医药学认为,雄黄(As4S4),外用可以治疗疥癣恶疮、蛇虫咬伤等;微量内服,可治惊痫、疮毒等症。雄黄遇热易氧化为As2O3(俗称砒霜),虽在古时常用做毒药,但科学家却发现它对治疗白血病有明显的作用。砷的其它化合物也在研究和生产中有着许多重要用途。____ ,核外电子占据的最高能级的电子云轮廓图形状为____ 。
(2)雄黄(As4S4)的结构如上图1所示,As原子的杂化形式为_____ 。
(3)Na3AsO4常用作杀虫剂、防腐剂,它含有的化学键类型包括____ ;AsO43-的空间构型为_____ 。
(4)砷化镓是优良的半导体材料,其晶胞结构如图2所示。立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是____ ;砷化镓密度为 ,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为
,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为 ,则砷化镓晶体的空间利用率为
,则砷化镓晶体的空间利用率为_____ 。
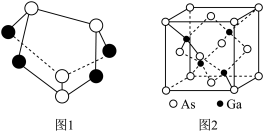
(2)雄黄(As4S4)的结构如上图1所示,As原子的杂化形式为
(3)Na3AsO4常用作杀虫剂、防腐剂,它含有的化学键类型包括
(4)砷化镓是优良的半导体材料,其晶胞结构如图2所示。立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是
 ,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为
,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为 ,则砷化镓晶体的空间利用率为
,则砷化镓晶体的空间利用率为
您最近一年使用:0次



