名校
1 . 药物阿兹夫定的有效成分的结构简式如图,下列说法中正确的是
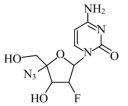
| A.含有3个手性碳原子 | B.阿兹夫定的分子式为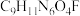 |
| C.五元环环上的原子共平面 | D.晶体的熔点高于 |
您最近一年使用:0次
名校
解题方法
2 . 下面排序不正确的是
A.晶体的熔点由高到低排列  |
B.熔点由高到低:  |
C.硬度由大到小:金刚石  碳化硅 碳化硅  晶体硅 晶体硅 |
D.熔点由高到低:  |
您最近一年使用:0次
名校
3 . 短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,W原子的核外电子数与X、Z原子的最外层电子数之和相等,Y的原子序数是Z原子最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所示。下列叙述正确的是

| A.简单离半径:X>Z | B.单质Y的熔点高于单质X |
| C.简单氢化物的热稳定性:Y>Z | D.Z的所有含氧酸均为强酸 |
您最近一年使用:0次
解题方法
4 . 下列关于物质的熔沸点高低顺序中,正确的是
| A.金刚石>晶体硅>金刚砂 | B.NaF>NaCl>NaBr |
| C.H2S>H2O | D.生铁>纯铁>钠 |
您最近一年使用:0次
解题方法
5 . 化合物 有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:
有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:
(1)Ca2+的焰色试验呈砖红色,金属元素能产生焰色试验的微观原因为____________ 。
(2)与Ni同周期且基态原子最外层电子数相同的Zn元素位于元素周期表的________ 区。
(3)Fe能与CO、 等形成配合物,如
等形成配合物,如 (结构如图1)、
(结构如图1)、 (结构如图2),其中1mol
(结构如图2),其中1mol  中含有
中含有________ mol配位原子, 中含有
中含有 键与
键与 键的数目之比为
键的数目之比为_________ 。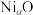 晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为
晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为 、
、 ,则晶体中
,则晶体中 与
与 的最简整数比为
的最简整数比为________ 。
(5)P与As同主族,磷化硼(BP,结构如图3)是一种超硬耐磨涂层材料,磷化硼晶体属于_________ (填“共价”“离子”或“分子”)晶体,_________ (填“是”或“否”)含有配位键,晶体中P原子的配位数为__________ 。 ,配位数为6的晶体有两种:X和Y。化学式为
,配位数为6的晶体有两种:X和Y。化学式为 的X呈绿色,定量实验表明,1mol X恰好与2mol
的X呈绿色,定量实验表明,1mol X恰好与2mol  反应生成沉淀。Y呈紫色,且1molY恰好与3mol
反应生成沉淀。Y呈紫色,且1molY恰好与3mol  反应生成沉淀,则Y的化学式为
反应生成沉淀,则Y的化学式为___________ 。
 有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:
有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:(1)Ca2+的焰色试验呈砖红色,金属元素能产生焰色试验的微观原因为
(2)与Ni同周期且基态原子最外层电子数相同的Zn元素位于元素周期表的
(3)Fe能与CO、
 等形成配合物,如
等形成配合物,如 (结构如图1)、
(结构如图1)、 (结构如图2),其中1mol
(结构如图2),其中1mol  中含有
中含有 中含有
中含有 键与
键与 键的数目之比为
键的数目之比为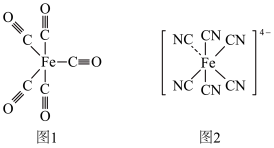
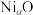 晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为
晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为 、
、 ,则晶体中
,则晶体中 与
与 的最简整数比为
的最简整数比为(5)P与As同主族,磷化硼(BP,结构如图3)是一种超硬耐磨涂层材料,磷化硼晶体属于

 ,配位数为6的晶体有两种:X和Y。化学式为
,配位数为6的晶体有两种:X和Y。化学式为 的X呈绿色,定量实验表明,1mol X恰好与2mol
的X呈绿色,定量实验表明,1mol X恰好与2mol  反应生成沉淀。Y呈紫色,且1molY恰好与3mol
反应生成沉淀。Y呈紫色,且1molY恰好与3mol  反应生成沉淀,则Y的化学式为
反应生成沉淀,则Y的化学式为
您最近一年使用:0次
名校
解题方法
6 . “结构决定性质”是化学学科的核心观念。下列有关性质的比较正确的是
A.在水中的溶解度:戊醇 乙醇 乙醇 | B.熔点: |
C.硬度:金刚石 碳化硅 碳化硅 硅 硅 | D.键角: |
您最近一年使用:0次
名校
7 . 下列关于物质的结构或性质以及解释均正确的是
| 选项 | 物质的结构与性质 | 解释 |
| A | 键角: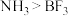 |  中 中 的孤电子对数比 的孤电子对数比 中 中 的孤电子对数多 的孤电子对数多 |
| B | 酸性: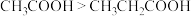 | 烃基(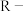 )越长推电子效应越大,使羧基中羟基的极性越小,羧酸的酸性越弱 )越长推电子效应越大,使羧基中羟基的极性越小,羧酸的酸性越弱 |
 |  的熔点比干冰高 的熔点比干冰高 |  比 比 相对分子量大,分子间作用力大 相对分子量大,分子间作用力大 |
 | 稳定性: |  分子间存在氢键 分子间存在氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 氮化硼、磷化硼均是受到高度关注的耐磨涂料。磷化硼的晶胞及某些原子的分数坐标如图所示,下列说法正确的是
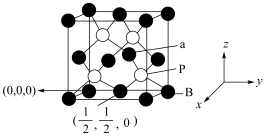
| A.磷化硼中P的价层电子对数为4 | B.熔点:BN<BP |
| C.磷化硼不溶于水,但可能溶于苯 | D.a原子的分数坐标为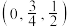 |
您最近一年使用:0次
名校
解题方法
9 . 我国科学家开发的 催化剂可实现
催化剂可实现 还原制
还原制 ,为资源回收利用提供新思路。请回答下列问题:
,为资源回收利用提供新思路。请回答下列问题:
(1)基态N原子的价层电子的轨道表示式为_______ 。
(2)题述物质所含的第二周期元素中,第一电离能由大到小的顺序为_______ (填元素符号,下同);电负性由小到大的顺序为_______ 。
(3)氨硼烷 是一种新型储氢材料。
是一种新型储氢材料。 分子中B原子的杂化方式为
分子中B原子的杂化方式为_______ 。
(4)已知: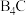 (碳化硼)、
(碳化硼)、 (氮化硼)的熔点依次为
(氮化硼)的熔点依次为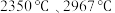 ,这两种物质的熔点存在差异的主要原因是
,这两种物质的熔点存在差异的主要原因是_______ 。
(5)已知 的晶胞结构如图1所示,该晶胞中含有的阳离子数为
的晶胞结构如图1所示,该晶胞中含有的阳离子数为_______ ,阳离子的配位数为_______ 。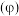 为
为_______ (用含π的式子表示);
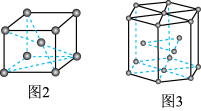
②图3中晶胞的空间利用率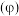 为
为_______ (用含%表示,保留2位有效数字,已知 =3.14,
=3.14, =1.414,
=1.414, =1.732);
=1.732);
③已知图3中晶胞底边长为 ,高为
,高为 ,
, 代表阿伏加德罗常数的值,则该晶胞的密度为
代表阿伏加德罗常数的值,则该晶胞的密度为_______  (用含
(用含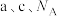 的式子表示)。
的式子表示)。
 催化剂可实现
催化剂可实现 还原制
还原制 ,为资源回收利用提供新思路。请回答下列问题:
,为资源回收利用提供新思路。请回答下列问题:(1)基态N原子的价层电子的轨道表示式为
(2)题述物质所含的第二周期元素中,第一电离能由大到小的顺序为
(3)氨硼烷
 是一种新型储氢材料。
是一种新型储氢材料。 分子中B原子的杂化方式为
分子中B原子的杂化方式为(4)已知:
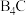 (碳化硼)、
(碳化硼)、 (氮化硼)的熔点依次为
(氮化硼)的熔点依次为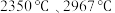 ,这两种物质的熔点存在差异的主要原因是
,这两种物质的熔点存在差异的主要原因是(5)已知
 的晶胞结构如图1所示,该晶胞中含有的阳离子数为
的晶胞结构如图1所示,该晶胞中含有的阳离子数为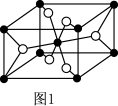
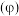 为
为②图3中晶胞的空间利用率
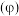 为
为 =3.14,
=3.14, =1.414,
=1.414, =1.732);
=1.732);③已知图3中晶胞底边长为
 ,高为
,高为 ,
, 代表阿伏加德罗常数的值,则该晶胞的密度为
代表阿伏加德罗常数的值,则该晶胞的密度为 (用含
(用含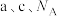 的式子表示)。
的式子表示)。
您最近一年使用:0次
名校
解题方法
10 . 硅微粒非常坚硬,比较晶体硅与碳化硅的熔点高低并解释说明___________ 。
您最近一年使用:0次



