名校
解题方法
1 . 碳、硅元素及其化合物在生产生活中应用广泛。请回答:
(1)基态硅原子核外电子排布式:_______ 。该基态原子占据最高能级的电子云轮廓图形状为_______ 。
(2)C60晶体采用面心立方堆积,C60晶体中存在的作用力有_______ (填字母)
A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键 F.金属键
(3)与碳的氢化物类似,硅元素的氢化物硅烷的通式为:SinH2n+2。下列有关说法不正确的是_______。
(4)硅酸盐是地壳中的主要成分。硅酸盐的最简单阴离子为SiO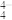 ,为硅氧四面体,结构如图1。SiO
,为硅氧四面体,结构如图1。SiO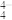 在溶液中形成的分子形态脱水易形成凝胶状的固体物质—硅胶。硅胶继续脱水,形成了共用氧原子的硅氧四面体骨架—SiO2(硅石)。联系相关信息,解释硅胶转变为硅石后,硬度变大的原因:
在溶液中形成的分子形态脱水易形成凝胶状的固体物质—硅胶。硅胶继续脱水,形成了共用氧原子的硅氧四面体骨架—SiO2(硅石)。联系相关信息,解释硅胶转变为硅石后,硬度变大的原因:_______ 。 ,KCx晶胞结构如图2(碳原子省略),如图3是晶胞沿y轴方向的投影。
,KCx晶胞结构如图2(碳原子省略),如图3是晶胞沿y轴方向的投影。_______ 。
②若石墨层内的大π键可表示为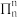 (上标表示电子总数,下标表示原子数),则平均每个KCx单元中的大π键可表示为
(上标表示电子总数,下标表示原子数),则平均每个KCx单元中的大π键可表示为_______ (用具体的数据表示)。
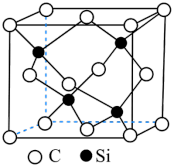
(6)已知 晶体的密度为ρg· cm-3,其晶胞结构如图所示。阿伏加德罗常数值为NA,则晶胞中两个
晶体的密度为ρg· cm-3,其晶胞结构如图所示。阿伏加德罗常数值为NA,则晶胞中两个 原子之间的距离为
原子之间的距离为_______  。
。
(1)基态硅原子核外电子排布式:
(2)C60晶体采用面心立方堆积,C60晶体中存在的作用力有
A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键 F.金属键
(3)与碳的氢化物类似,硅元素的氢化物硅烷的通式为:SinH2n+2。下列有关说法不正确的是_______。
| A.Si3H8没有同分异构体 |
| B.Si-Si键能比C-C键能小,故热稳定性:SinH2n+2>CnH2n+2 |
| C.SinH2n+2中Si原子杂化方式均为sp3 |
| D.SinH2n+2可与水反应生成氢气 |
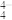 ,为硅氧四面体,结构如图1。SiO
,为硅氧四面体,结构如图1。SiO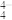 在溶液中形成的分子形态脱水易形成凝胶状的固体物质—硅胶。硅胶继续脱水,形成了共用氧原子的硅氧四面体骨架—SiO2(硅石)。联系相关信息,解释硅胶转变为硅石后,硬度变大的原因:
在溶液中形成的分子形态脱水易形成凝胶状的固体物质—硅胶。硅胶继续脱水,形成了共用氧原子的硅氧四面体骨架—SiO2(硅石)。联系相关信息,解释硅胶转变为硅石后,硬度变大的原因: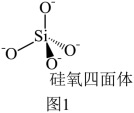
 ,KCx晶胞结构如图2(碳原子省略),如图3是晶胞沿y轴方向的投影。
,KCx晶胞结构如图2(碳原子省略),如图3是晶胞沿y轴方向的投影。
②若石墨层内的大π键可表示为
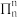 (上标表示电子总数,下标表示原子数),则平均每个KCx单元中的大π键可表示为
(上标表示电子总数,下标表示原子数),则平均每个KCx单元中的大π键可表示为(6)已知
 晶体的密度为ρg· cm-3,其晶胞结构如图所示。阿伏加德罗常数值为NA,则晶胞中两个
晶体的密度为ρg· cm-3,其晶胞结构如图所示。阿伏加德罗常数值为NA,则晶胞中两个 原子之间的距离为
原子之间的距离为 。
。
您最近一年使用:0次
名校
解题方法
2 . 中医药学认为,雄黄(As4S4),外用可以治疗疥癣恶疮、蛇虫咬伤等;微量内服,可治惊痫、疮毒等症。雄黄遇热易氧化为As2O3(俗称砒霜),虽在古时常用做毒药,但科学家却发现它对治疗白血病有明显的作用。砷的其它化合物也在研究和生产中有着许多重要用途。____ ,核外电子占据的最高能级的电子云轮廓图形状为____ 。
(2)雄黄(As4S4)的结构如上图1所示,As原子的杂化形式为_____ 。
(3)Na3AsO4常用作杀虫剂、防腐剂,它含有的化学键类型包括____ ;AsO43-的空间构型为_____ 。
(4)砷化镓是优良的半导体材料,其晶胞结构如图2所示。立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是____ ;砷化镓密度为 ,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为
,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为 ,则砷化镓晶体的空间利用率为
,则砷化镓晶体的空间利用率为_____ 。
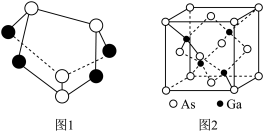
(2)雄黄(As4S4)的结构如上图1所示,As原子的杂化形式为
(3)Na3AsO4常用作杀虫剂、防腐剂,它含有的化学键类型包括
(4)砷化镓是优良的半导体材料,其晶胞结构如图2所示。立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是
 ,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为
,Ga和As原子半径分别为r1pm和r2pm,阿伏加德罗常数值为 ,则砷化镓晶体的空间利用率为
,则砷化镓晶体的空间利用率为
您最近一年使用:0次
解题方法
3 . 氮元素能与金属或者非金属元素形成种类繁多、应用广泛的化合物。
(1)基态N原子的价层电子轨道表示式是___________ 。
(2)与碳氢化合物类似,N、H两元素之间也可以形成氮烷、氮烯。
①在最简单的氮烯分子中,N的杂化方式是___________ 。
② 具有很强的还原性,是常用的火箭推进剂,它在常温常压下为无色液体。判断
具有很强的还原性,是常用的火箭推进剂,它在常温常压下为无色液体。判断 是否溶于水并说明理由
是否溶于水并说明理由___________ 。
(3)配合物 可用作广谱杀菌剂,其中Cu属于
可用作广谱杀菌剂,其中Cu属于___________ 区元素,该配合物中的配位原子是___________ ,配位数是___________ 。
(4) 的某种晶体结构中,原子间均以单键结合,其硬度比金刚石大,原因是
的某种晶体结构中,原子间均以单键结合,其硬度比金刚石大,原因是___________ 。
(5) 和
和 形成的化合物是一种重要的半导体材料。其某种晶胞形状为立方体,边长为
形成的化合物是一种重要的半导体材料。其某种晶胞形状为立方体,边长为 ,结构如图所示。
,结构如图所示。 最近的
最近的 有
有___________ 个。
②已知阿伏加德罗常数为 ,氮化镓(GaN)的摩尔质量为
,氮化镓(GaN)的摩尔质量为 ,该晶体的密度表达式为
,该晶体的密度表达式为___________  (
( )。
)。
(1)基态N原子的价层电子轨道表示式是
(2)与碳氢化合物类似,N、H两元素之间也可以形成氮烷、氮烯。
①在最简单的氮烯分子中,N的杂化方式是
②
 具有很强的还原性,是常用的火箭推进剂,它在常温常压下为无色液体。判断
具有很强的还原性,是常用的火箭推进剂,它在常温常压下为无色液体。判断 是否溶于水并说明理由
是否溶于水并说明理由(3)配合物
 可用作广谱杀菌剂,其中Cu属于
可用作广谱杀菌剂,其中Cu属于(4)
 的某种晶体结构中,原子间均以单键结合,其硬度比金刚石大,原因是
的某种晶体结构中,原子间均以单键结合,其硬度比金刚石大,原因是(5)
 和
和 形成的化合物是一种重要的半导体材料。其某种晶胞形状为立方体,边长为
形成的化合物是一种重要的半导体材料。其某种晶胞形状为立方体,边长为 ,结构如图所示。
,结构如图所示。
 最近的
最近的 有
有②已知阿伏加德罗常数为
 ,氮化镓(GaN)的摩尔质量为
,氮化镓(GaN)的摩尔质量为 ,该晶体的密度表达式为
,该晶体的密度表达式为 (
( )。
)。
您最近一年使用:0次
解题方法
4 . 氮化镓 是智能手机的快速充电器中使用的一种半导体材料,可通过单质与氨气在高温下反应可制得。镓在周期表中的位置如图。
是智能手机的快速充电器中使用的一种半导体材料,可通过单质与氨气在高温下反应可制得。镓在周期表中的位置如图。
(1)配平反应:___________ 
 ___________
___________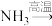 ___________
___________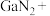 ___________
___________ ;其中氧化剂的电子式
;其中氧化剂的电子式___________ 。
(2)N原子的电子排布式为___________ 。Ga原子核外未成对电子数为___________ 个。
(3)氢化物的热稳定性:
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
Ga分别与N、P、 形成化合物的晶体结构与金刚石相似,其熔点如下表所示:
形成化合物的晶体结构与金刚石相似,其熔点如下表所示:
(4) 晶体中含有的化学键类型为
晶体中含有的化学键类型为___________ 。从结构的角度分析、推测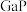 的熔点范围
的熔点范围___________ ,理由是___________ 。
 是智能手机的快速充电器中使用的一种半导体材料,可通过单质与氨气在高温下反应可制得。镓在周期表中的位置如图。
是智能手机的快速充电器中使用的一种半导体材料,可通过单质与氨气在高温下反应可制得。镓在周期表中的位置如图。| Al | P |
| Ga | As |
(1)配平反应:

 ___________
___________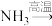 ___________
___________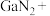 ___________
___________ ;其中氧化剂的电子式
;其中氧化剂的电子式(2)N原子的电子排布式为
(3)氢化物的热稳定性:

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。 Ga分别与N、P、
 形成化合物的晶体结构与金刚石相似,其熔点如下表所示:
形成化合物的晶体结构与金刚石相似,其熔点如下表所示:| 物质 |  | 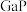 |  |
| 熔点/℃ | 1700 | x | 1238 |
 晶体中含有的化学键类型为
晶体中含有的化学键类型为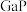 的熔点范围
的熔点范围
您最近一年使用:0次
2022-06-15更新
|
190次组卷
|
2卷引用:上海市黄浦区2022届高三6月学业等级考调研测试化学试题
5 . 镓 及其化合物在国防技术、航空航天技术等领域扮演着重要的角色。一种利用湿法提锌的浸出渣(主要含一定量
及其化合物在国防技术、航空航天技术等领域扮演着重要的角色。一种利用湿法提锌的浸出渣(主要含一定量 和
和 的化合物)为原料制备高纯镓的流程如图所示:
的化合物)为原料制备高纯镓的流程如图所示:
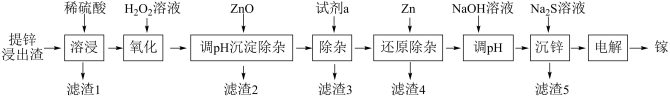
已知:①溶液中的 会对电解
会对电解 溶液造成影响
溶液造成影响
② 与
与 可以发生反应
可以发生反应
③本流程温度下,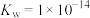 ;
; ;
;
请回答下列问题:
(1)滤渣1的主要成分为_______ (填化学式)。
(2)“氧化”过程中发生反应的离子方程式为_______ 。
(3)“调 沉淀除杂”过程需加入聚丙烯酰胺絮凝剂并加热的目的是
沉淀除杂”过程需加入聚丙烯酰胺絮凝剂并加热的目的是_______ 。
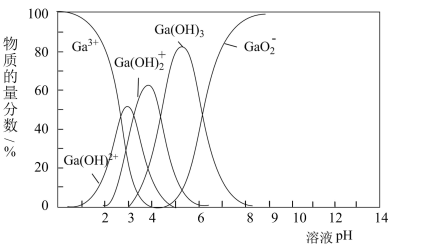
(4)溶液中 的各种形态粒子的物质的量分数随溶液
的各种形态粒子的物质的量分数随溶液 变化的关系如图所示,用
变化的关系如图所示,用 “调
“调 沉淀除杂”的理论范围为
沉淀除杂”的理论范围为_______ 。(溶液中剩余离子浓度小于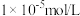 时沉淀完全)
时沉淀完全)
(5)试剂a的作用是_______ 。
(6)流程中可以循环利用的物质是_______ (填化学式)。
(7) 、
、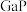 、
、 可用于制取第三代半导体材料,熔点如表所示,分析其变化原因:
可用于制取第三代半导体材料,熔点如表所示,分析其变化原因:_______ 。
 及其化合物在国防技术、航空航天技术等领域扮演着重要的角色。一种利用湿法提锌的浸出渣(主要含一定量
及其化合物在国防技术、航空航天技术等领域扮演着重要的角色。一种利用湿法提锌的浸出渣(主要含一定量 和
和 的化合物)为原料制备高纯镓的流程如图所示:
的化合物)为原料制备高纯镓的流程如图所示:
已知:①溶液中的
 会对电解
会对电解 溶液造成影响
溶液造成影响②
 与
与 可以发生反应
可以发生反应
③本流程温度下,
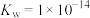 ;
; ;
;
请回答下列问题:
(1)滤渣1的主要成分为
(2)“氧化”过程中发生反应的离子方程式为
(3)“调
 沉淀除杂”过程需加入聚丙烯酰胺絮凝剂并加热的目的是
沉淀除杂”过程需加入聚丙烯酰胺絮凝剂并加热的目的是(4)溶液中
 的各种形态粒子的物质的量分数随溶液
的各种形态粒子的物质的量分数随溶液 变化的关系如图所示,用
变化的关系如图所示,用 “调
“调 沉淀除杂”的理论范围为
沉淀除杂”的理论范围为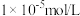 时沉淀完全)
时沉淀完全)
(5)试剂a的作用是
(6)流程中可以循环利用的物质是
(7)
 、
、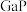 、
、 可用于制取第三代半导体材料,熔点如表所示,分析其变化原因:
可用于制取第三代半导体材料,熔点如表所示,分析其变化原因:| 物质 |  | 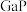 |  |
| 熔点 | 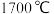 | 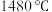 | 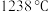 |
您最近一年使用:0次
2022-04-22更新
|
545次组卷
|
3卷引用:辽宁省锦州市2022届高三第一次质量检测化学试题
解题方法
6 . Al2O3可以从铝土矿中获得,铝土矿的主要成分为Al2O3,含Fe2O3、SiO2等杂质。经过“酸溶法”或“碱溶法”等都可以去掉杂质得到Al2O3。19世纪后期,美国的霍尔和法国的埃鲁先后独立发明了电解Al2O3法生产铝。2Al2O3 4Al+3O2↑[冰晶石(Na3AlF6)作助熔剂,降低氧化铝熔点]
4Al+3O2↑[冰晶石(Na3AlF6)作助熔剂,降低氧化铝熔点]
(1)上述涉及到Al、Na、O、F、Si、Fe六种元素中,不是主族元素的是___________ ,Al3+电子排布式___________ ,O原子的未成对电子数___________ 。
(2)制造“中国芯”芯片的核心元素Si位于元素周期表第___________ 周期第___________ 族。冰晶石(Na3AlF6)晶体中阴、阳离子各一种,阴离子符号___________ 。
(3)用“>”或“<”填空:
(4)用离子晶体的知识解释Al2O3比Na2O熔点高的原因_________ 。
(5)其实电解法生产铝有很多弊端,科技工作者不断创新。下面一种新型直接从铝土矿中提取铝的方法
I.Al2O3(s)+AlCl3(g)+3C(s) 3 AlCl(g)+ 3CO(g) -1486kJ
3 AlCl(g)+ 3CO(g) -1486kJ
II.3 AlCl(g) 2 Al(l)+ AlCl3(g) +140 kJ
2 Al(l)+ AlCl3(g) +140 kJ
①反应I中的还原产物是___________ ;若有0.6gC反应,电子转移数目为___________
②结合反应I、II分析,请说出这种提炼方法2条优点___________ ___________ 。
 4Al+3O2↑[冰晶石(Na3AlF6)作助熔剂,降低氧化铝熔点]
4Al+3O2↑[冰晶石(Na3AlF6)作助熔剂,降低氧化铝熔点](1)上述涉及到Al、Na、O、F、Si、Fe六种元素中,不是主族元素的是
(2)制造“中国芯”芯片的核心元素Si位于元素周期表第
(3)用“>”或“<”填空:
原子半径 | 非金属性 | 熔点 |
| Al | O | 二氧化硅 |
(4)用离子晶体的知识解释Al2O3比Na2O熔点高的原因
(5)其实电解法生产铝有很多弊端,科技工作者不断创新。下面一种新型直接从铝土矿中提取铝的方法
I.Al2O3(s)+AlCl3(g)+3C(s)
 3 AlCl(g)+ 3CO(g) -1486kJ
3 AlCl(g)+ 3CO(g) -1486kJII.3 AlCl(g)
 2 Al(l)+ AlCl3(g) +140 kJ
2 Al(l)+ AlCl3(g) +140 kJ①反应I中的还原产物是
②结合反应I、II分析,请说出这种提炼方法2条优点
您最近一年使用:0次
解题方法
7 . 已知:碳、氮、氢、氧四种元素可形成多种化合物,且有非常重要的用途。
(1)C、N、H电负性的大小顺序为_____________ 。
(2)甲烷与二氧化氮可发生如下反应:CH4(g)+2NO2(g)=CO2(g)+N2(g)+2H2O(g) ,若反应中有2mol C-H键断裂,则形成的π键共有_________ mol。
(3)F2与NH3在一定条件下可形成NF3,NF3分子的空间构型为___________ 形 。
(4)现已合成出一种硬度比金刚石还大的晶体氮化碳,其化学式为___________ 。其硬度比金刚石大的主要原因是______________ 。
(5)配合物Y的结构如图所示,Y中含有___________________ (填序号)。

A.非极性共价键
B.配位键
C.极性键
D.氢键
E.金属键
Y中碳原子的杂化方式有___________________________________ 。
写出镍(Ni)原子的价电子排布式_________________________ 。
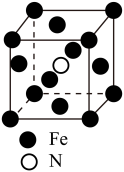
(6)氨气与铁在一定条件下发生置换反应,一种产物的晶胞结构如下图所示,若该立方体晶胞的棱长为a pm,则该晶体的密度为_________ g/cm3(NA为阿伏加德罗常数的值)。
(1)C、N、H电负性的大小顺序为
(2)甲烷与二氧化氮可发生如下反应:CH4(g)+2NO2(g)=CO2(g)+N2(g)+2H2O(g) ,若反应中有2mol C-H键断裂,则形成的π键共有
(3)F2与NH3在一定条件下可形成NF3,NF3分子的空间构型为
(4)现已合成出一种硬度比金刚石还大的晶体氮化碳,其化学式为
(5)配合物Y的结构如图所示,Y中含有

A.非极性共价键
B.配位键
C.极性键
D.氢键
E.金属键
Y中碳原子的杂化方式有
写出镍(Ni)原子的价电子排布式
(6)氨气与铁在一定条件下发生置换反应,一种产物的晶胞结构如下图所示,若该立方体晶胞的棱长为a pm,则该晶体的密度为

您最近一年使用:0次



