名校
1 . 某活动小组用碳素钢进行了如下活动:
(1)常温下,可以用铁质容器盛放冷的浓硫酸,其原因是_______ 。
(2)称取碳素钢6g放入15mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用_______ (选填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液
C.浓氨水 D.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,溴水褪色,由此推知混合气体Y中含有_______ ,其化学方程式为:_______ ,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g,由此推知气体Y中该气体的体积分数为_______ 。
(1)常温下,可以用铁质容器盛放冷的浓硫酸,其原因是
(2)称取碳素钢6g放入15mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用
A.KSCN溶液和氯水 B.铁粉和KSCN溶液
C.浓氨水 D.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,溴水褪色,由此推知混合气体Y中含有
您最近一年使用:0次
2 . 金属腐蚀原理的应用
(1)将铝片浸入浓硫酸或浓硝酸时,铝片表面产生___________ ,从而阻止铝进一步被氧化。可以用___________ 运输冷的浓硝酸或浓硫酸。
(2)铁在___________ 的混合液中发蓝、发黑,使铁表面形成一层___________ ,可防止铁被腐蚀。
(3)生活中常用的“暖宝宝”是利用___________ 原理制造的。
(1)将铝片浸入浓硫酸或浓硝酸时,铝片表面产生
(2)铁在
(3)生活中常用的“暖宝宝”是利用
您最近一年使用:0次
3 . 2021年是国际化学年十周年纪念,中国的宣传口号是“化学一我们的生活,我们的未来”。
(1)高纯度单晶硅是典型的无机非金属材料,它的发现和使用曾引起计算机的一场“革命”。下列有关硅材料的说法正确的是_______(填字母)。
(2)工业上常用金属钠冶炼钛,是利用金属钠的强_______ 性。
(3)常温下,可用铁或铝制器皿盛放浓硝酸,是因为_______ 。
(4)纯碱和小苏打均为常见的厨房用品。兴趣小组同学用如图装置比较纯碱(Na2CO3)和小苏打(NaHCO3)的热稳定性。实验过程中可以观察到烧杯_______ (填“I”或“II”)中澄清石灰水变浑浊。加热后试管中发生反应的化学方程式为_______ 。

(5)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘:NaIO3+NaHSO3→NaHSO4+Na2SO4+I2+H2O(未配平)。配平该方程式_______ 。
(1)高纯度单晶硅是典型的无机非金属材料,它的发现和使用曾引起计算机的一场“革命”。下列有关硅材料的说法正确的是_______(填字母)。
| A.晶体硅用于制作半导体材料 | B.硅在常温下化学性比较活泼 |
| C.玻璃属于硅酸盐材料 | D.玛瑙的主要成分是硅单质 |
(3)常温下,可用铁或铝制器皿盛放浓硝酸,是因为
(4)纯碱和小苏打均为常见的厨房用品。兴趣小组同学用如图装置比较纯碱(Na2CO3)和小苏打(NaHCO3)的热稳定性。实验过程中可以观察到烧杯

(5)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘:NaIO3+NaHSO3→NaHSO4+Na2SO4+I2+H2O(未配平)。配平该方程式
您最近一年使用:0次
4 . 根据所学知识,回答下列问题:
(1)“元时,南安有黄长者,为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。”泥土能将红糖变白糖,其表现的性质是_______ 。
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是_______ 。
(3)欲使3 mol VO2+全部转化为VO ,则需要氧化剂KClO3(还原产物为Cl-)至少
,则需要氧化剂KClO3(还原产物为Cl-)至少_______ mol。
(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是_______ (用化学方程式表示)。
(5)下列变化为化学变化的是_______ (填标号)。
A.CaCl2的潮解 B.钠的焰色反应 C.常温下,Fe遇浓硫酸钝化
(1)“元时,南安有黄长者,为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。”泥土能将红糖变白糖,其表现的性质是
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是
(3)欲使3 mol VO2+全部转化为VO
 ,则需要氧化剂KClO3(还原产物为Cl-)至少
,则需要氧化剂KClO3(还原产物为Cl-)至少(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是
(5)下列变化为化学变化的是
A.CaCl2的潮解 B.钠的焰色反应 C.常温下,Fe遇浓硫酸钝化
您最近一年使用:0次
名校
解题方法
5 . 利用下列实验研究铁与浓硫酸的反应(夹持装置已略去,气密性已检验)。
(1)实验Ⅰ中体现了浓硫酸的_______ (填“氧化性”或“还原性”)。
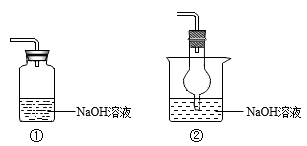
(2)下列装置中,能用于实验Ⅱ中尾气吸收的是_______ (填序号)。
(3)实验Ⅱ中,能够证明生成了SO2的证据是_______ 。
(4)实验Ⅰ和Ⅱ中,实验现象不同的原因是_______ 。
| 实验Ⅰ | 实验Ⅱ |
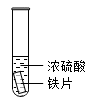 | 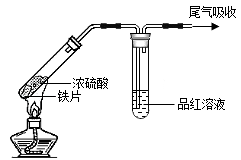 |
| 铁片表面迅速变暗,之后无明显变化 | 加热后产生大量气体,品红溶液褪色 |
(2)下列装置中,能用于实验Ⅱ中尾气吸收的是

(3)实验Ⅱ中,能够证明生成了SO2的证据是
(4)实验Ⅰ和Ⅱ中,实验现象不同的原因是
您最近一年使用:0次
2021-01-19更新
|
336次组卷
|
4卷引用:江苏省徐州市第三十五中学2020-2021学年高二10月月考化学试题
江苏省徐州市第三十五中学2020-2021学年高二10月月考化学试题湖南省武冈市第二中学2020-2021学年高一下学期开学考试化学试题北京市中国农业大学附属中学2019-2020学年高一上学期期末考试化学试题(已下线)4.1.2 硫酸的工业制备 浓硫酸的性质-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)
解题方法
6 . 铁是人体内必需的微量元素,铁的化学性质较活泼,能与很多物质发生反应。完成下列填空:
(1)常温下由于浓硫酸能使铁_______ ,因此浓硫酸可用铁槽车运输。
(2)写出铁与水蒸气反应的化学方程式_______ 。
(3)写出铁与氯气恰好完全反应的化学方程式_______ 。将产物溶于水,能得到_______ 颜色的溶液,其产物中的阳离子可以用_______ 溶液检验,写出其离子方程式_______ 。
(1)常温下由于浓硫酸能使铁
(2)写出铁与水蒸气反应的化学方程式
(3)写出铁与氯气恰好完全反应的化学方程式
您最近一年使用:0次
7 . 铁及其化合物在工农业生产、环境保护等领域中有着重要的作用。
(1)酸性条件下,硫酸亚铁可将MnO2还原为MnSO4,该反应的离子方程式为:_____________ 。
(2)分析表明,铁在浓硫酸中发生钝化时,生成的氧化物中Fe、O两种元素的质量比为28∶11,则其化学式为______________ 。
(3)铁及其化合物可用于消除环境污染。常温下,硫酸亚铁能将SO2转化为 ,总反应为2SO2+O2+2H2O=2H2SO4,其中一个反应为4Fe2++O2+4H+=4Fe3++2H2O,则另一个反应的离子方程式为
,总反应为2SO2+O2+2H2O=2H2SO4,其中一个反应为4Fe2++O2+4H+=4Fe3++2H2O,则另一个反应的离子方程式为____________________ 。
常温下,用氧缺位铁酸锌ZnFe2Oy可以消除NOx污染,使NOx转变为N2,同时ZnFe2Oy转变为ZnFe2O4。若2 mol ZnFe2Oy与足量NO2反应可生成0.5 mol N2,则y=____________ 。
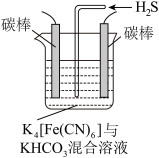
(4)工业上常采用如图所示电解装置,利用铁的化合物将气态废弃物中的硫化氢转化为可利用的硫。通电电解,然后通入H2S时发生反应的离子方程式为:2[Fe(CN)6]3-+2 +H2S=2[Fe(CN)6]4-+2H
+H2S=2[Fe(CN)6]4-+2H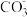 +S↓。电解时,阳极的电极反应式为
+S↓。电解时,阳极的电极反应式为___________ ;电解过程中阴极区溶液的pH______________ (填“变大”、“变小”或“不变”)。
(1)酸性条件下,硫酸亚铁可将MnO2还原为MnSO4,该反应的离子方程式为:
(2)分析表明,铁在浓硫酸中发生钝化时,生成的氧化物中Fe、O两种元素的质量比为28∶11,则其化学式为
(3)铁及其化合物可用于消除环境污染。常温下,硫酸亚铁能将SO2转化为
 ,总反应为2SO2+O2+2H2O=2H2SO4,其中一个反应为4Fe2++O2+4H+=4Fe3++2H2O,则另一个反应的离子方程式为
,总反应为2SO2+O2+2H2O=2H2SO4,其中一个反应为4Fe2++O2+4H+=4Fe3++2H2O,则另一个反应的离子方程式为常温下,用氧缺位铁酸锌ZnFe2Oy可以消除NOx污染,使NOx转变为N2,同时ZnFe2Oy转变为ZnFe2O4。若2 mol ZnFe2Oy与足量NO2反应可生成0.5 mol N2,则y=

(4)工业上常采用如图所示电解装置,利用铁的化合物将气态废弃物中的硫化氢转化为可利用的硫。通电电解,然后通入H2S时发生反应的离子方程式为:2[Fe(CN)6]3-+2
 +H2S=2[Fe(CN)6]4-+2H
+H2S=2[Fe(CN)6]4-+2H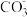 +S↓。电解时,阳极的电极反应式为
+S↓。电解时,阳极的电极反应式为
您最近一年使用:0次



