名校
1 . 某活动小组用碳素钢进行了如下活动:
(1)常温下,可以用铁质容器盛放冷的浓硫酸,其原因是_______ 。
(2)称取碳素钢6g放入15mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用_______ (选填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液
C.浓氨水 D.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,溴水褪色,由此推知混合气体Y中含有_______ ,其化学方程式为:_______ ,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g,由此推知气体Y中该气体的体积分数为_______ 。
(1)常温下,可以用铁质容器盛放冷的浓硫酸,其原因是
(2)称取碳素钢6g放入15mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用
A.KSCN溶液和氯水 B.铁粉和KSCN溶液
C.浓氨水 D.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,溴水褪色,由此推知混合气体Y中含有
您最近半年使用:0次
2 . 金属腐蚀原理的应用
(1)将铝片浸入浓硫酸或浓硝酸时,铝片表面产生___________ ,从而阻止铝进一步被氧化。可以用___________ 运输冷的浓硝酸或浓硫酸。
(2)铁在___________ 的混合液中发蓝、发黑,使铁表面形成一层___________ ,可防止铁被腐蚀。
(3)生活中常用的“暖宝宝”是利用___________ 原理制造的。
(1)将铝片浸入浓硫酸或浓硝酸时,铝片表面产生
(2)铁在
(3)生活中常用的“暖宝宝”是利用
您最近半年使用:0次
3 . 请列举铁与硝酸反应的各种情况,写出相关的离子方程式_______ 。
您最近半年使用:0次
4 . 2021年是国际化学年十周年纪念,中国的宣传口号是“化学一我们的生活,我们的未来”。
(1)高纯度单晶硅是典型的无机非金属材料,它的发现和使用曾引起计算机的一场“革命”。下列有关硅材料的说法正确的是_______(填字母)。
(2)工业上常用金属钠冶炼钛,是利用金属钠的强_______ 性。
(3)常温下,可用铁或铝制器皿盛放浓硝酸,是因为_______ 。
(4)纯碱和小苏打均为常见的厨房用品。兴趣小组同学用如图装置比较纯碱(Na2CO3)和小苏打(NaHCO3)的热稳定性。实验过程中可以观察到烧杯_______ (填“I”或“II”)中澄清石灰水变浑浊。加热后试管中发生反应的化学方程式为_______ 。

(5)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘:NaIO3+NaHSO3→NaHSO4+Na2SO4+I2+H2O(未配平)。配平该方程式_______ 。
(1)高纯度单晶硅是典型的无机非金属材料,它的发现和使用曾引起计算机的一场“革命”。下列有关硅材料的说法正确的是_______(填字母)。
| A.晶体硅用于制作半导体材料 | B.硅在常温下化学性比较活泼 |
| C.玻璃属于硅酸盐材料 | D.玛瑙的主要成分是硅单质 |
(3)常温下,可用铁或铝制器皿盛放浓硝酸,是因为
(4)纯碱和小苏打均为常见的厨房用品。兴趣小组同学用如图装置比较纯碱(Na2CO3)和小苏打(NaHCO3)的热稳定性。实验过程中可以观察到烧杯

(5)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘:NaIO3+NaHSO3→NaHSO4+Na2SO4+I2+H2O(未配平)。配平该方程式
您最近半年使用:0次
名校
5 . I.原电池是化学电源的雏形。
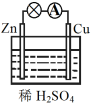
(1)如图连接好装置后,负极材料是_______ (填“Zn”或“Cu”)。
(2)相应原电池的总反应方程式为_______ 。
(3)下列化学反应可通过原电池装置,实现化学能直接转化为电能的是_______ (填序号)。
①2NaOH+H2SO4=Na2SO4 +2H2O ②Cu+2Fe 3+=Cu2++2Fe2+ ③C2H5OH+3O2 2CO2 +3H2O
2CO2 +3H2O
II.根据原电池原理,结合装置图,按要求解答问题:

(4)若X为Zn,Y为硫酸铜溶液,溶液中的Cu2+移向_______ (填“Cu”或“X”)电极。
(5)若X为银,Y为硝酸银溶液,则X的电极方程式_______
(6)若X为Fe,Y为浓硝酸,则Cu电极电极方程式是_______ 。

(1)如图连接好装置后,负极材料是
(2)相应原电池的总反应方程式为
(3)下列化学反应可通过原电池装置,实现化学能直接转化为电能的是
①2NaOH+H2SO4=Na2SO4 +2H2O ②Cu+2Fe 3+=Cu2++2Fe2+ ③C2H5OH+3O2
 2CO2 +3H2O
2CO2 +3H2OII.根据原电池原理,结合装置图,按要求解答问题:

(4)若X为Zn,Y为硫酸铜溶液,溶液中的Cu2+移向
(5)若X为银,Y为硝酸银溶液,则X的电极方程式
(6)若X为Fe,Y为浓硝酸,则Cu电极电极方程式是
您最近半年使用:0次
名校
6 . Ⅰ.图象具有直观、线索清晰、引导性强等特点,有利于提高统筹思维和概括能力。图是氮元素的化合价与部分常见含氮物质的关系。

请回答下列问题:
(1)丙的化学式为_______
(2)写出实验室制备甲的化学方程式:_______ ;收集甲物质的常用方法是_______
(3)若己物质的水溶液呈浅绿色,向该溶液中加入稀硫酸,溶液变黄色,同时生成丙,写出该过程中发生反应的离子方程式:_______
(4)丁是一种有颜色的气体,写出丁与水反应生成丙和戊的化学方程式,并用双线桥表示电子转移的情况:_______
(5)常温下,戊的浓溶液可以用干燥的铁罐车运输,原因是_______
Ⅱ.将等物质的量的 、
、 混合于2L的固定体积的密闭容器中,在一定条件下反应合成氨,经5min后达到平衡,其中
混合于2L的固定体积的密闭容器中,在一定条件下反应合成氨,经5min后达到平衡,其中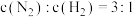 ;若将混合气体中氨气分离,恰好能与250mL2mol/L的稀硫酸溶液反应生成正盐;
;若将混合气体中氨气分离,恰好能与250mL2mol/L的稀硫酸溶液反应生成正盐;
(6)原容器中 的物质的量是
的物质的量是_______
(7)5min后容器中 的物质的量浓度
的物质的量浓度_______
(8) 的转化率是
的转化率是_______

请回答下列问题:
(1)丙的化学式为
(2)写出实验室制备甲的化学方程式:
(3)若己物质的水溶液呈浅绿色,向该溶液中加入稀硫酸,溶液变黄色,同时生成丙,写出该过程中发生反应的离子方程式:
(4)丁是一种有颜色的气体,写出丁与水反应生成丙和戊的化学方程式,并用双线桥表示电子转移的情况:
(5)常温下,戊的浓溶液可以用干燥的铁罐车运输,原因是
Ⅱ.将等物质的量的
 、
、 混合于2L的固定体积的密闭容器中,在一定条件下反应合成氨,经5min后达到平衡,其中
混合于2L的固定体积的密闭容器中,在一定条件下反应合成氨,经5min后达到平衡,其中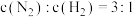 ;若将混合气体中氨气分离,恰好能与250mL2mol/L的稀硫酸溶液反应生成正盐;
;若将混合气体中氨气分离,恰好能与250mL2mol/L的稀硫酸溶液反应生成正盐;(6)原容器中
 的物质的量是
的物质的量是(7)5min后容器中
 的物质的量浓度
的物质的量浓度(8)
 的转化率是
的转化率是
您最近半年使用:0次
名校
解题方法
7 . 回答下列问题:
(1)将一支充有12mLNO2气体的试管倒置于水槽中,充分反应后,下列图示正确的是____ ,NO2气体与水发生反应的化学方程式是____ ,若要让试管内充满气体则需要通入氧气的体积是____ mL。
A.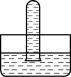 B.
B. 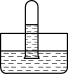 C.
C.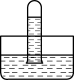 D.
D.
(2)常温下,铁制品____ (填“能”或者“不能”)盛装浓硝酸,原因是____ 。
(3)浓硝酸保存在___ 色试剂瓶里,原因___ (用方程室表示)。
(1)将一支充有12mLNO2气体的试管倒置于水槽中,充分反应后,下列图示正确的是
A.
 B.
B.  C.
C. D.
D.
(2)常温下,铁制品
(3)浓硝酸保存在
您最近半年使用:0次
名校
8 . 化学是一门实用性很强的科学。根据题意填空:
(1)古代锻造刀剑时,将炽热的刀剑快速投入水中“淬火”,反应为:3Fe+4H2O(g) Fe3O4+4H2.该反应中H2O作
Fe3O4+4H2.该反应中H2O作___________ (填“氧化剂”或“还原剂”);
(2)常温条件下,可以用铁罐盛装浓硫酸和浓硝酸,是因为常温下,浓硫酸和浓硝酸可以使铁发生___________ ;
(3)人们使用量最大的传统硅酸盐产品有水泥、玻璃和___________ ;
(4)浓硫酸可以干燥氢气、氧气、氯气、二氧化硫等气体,这体现了浓硫酸具有___________ ;
(5)某学习小组为了探究碳与浓H2SO4反应的产物,将浓H2SO4和木炭反应产生的气体进行了实验:当把产生的气体通入足量的澄清石灰水,产生白色沉淀。该小组认为气体中含有CO2,你认为该结论:___________ (填“正确”或“不正确”)。
(1)古代锻造刀剑时,将炽热的刀剑快速投入水中“淬火”,反应为:3Fe+4H2O(g)
 Fe3O4+4H2.该反应中H2O作
Fe3O4+4H2.该反应中H2O作(2)常温条件下,可以用铁罐盛装浓硫酸和浓硝酸,是因为常温下,浓硫酸和浓硝酸可以使铁发生
(3)人们使用量最大的传统硅酸盐产品有水泥、玻璃和
(4)浓硫酸可以干燥氢气、氧气、氯气、二氧化硫等气体,这体现了浓硫酸具有
(5)某学习小组为了探究碳与浓H2SO4反应的产物,将浓H2SO4和木炭反应产生的气体进行了实验:当把产生的气体通入足量的澄清石灰水,产生白色沉淀。该小组认为气体中含有CO2,你认为该结论:
您最近半年使用:0次
9 . 硝酸的化学性质
(1)酸的通性
写出下列反应的离子方程式:
①硝酸和氢氧化钠反应:_________________________ 。
②硝酸和氧化钠反应:_________________________ 。
③硝酸和碳酸钙反应:_________________________ 。
(2)不稳定性:见光或受热易分解,化学方程式为_________________________________ 。
长期存放的浓硝酸呈黄色是因为其分解生成的____ 溶于硝酸中,实验室常将浓硝酸保存在____ 试剂瓶中,并放在____ 处。
(3)强氧化性
①和金属(Cu)反应的实验探究
写出上述反应的化学方程式:_________ ;_________ 。
②与Fe、Al反应
常温下浓硝酸可使铁、铝表面形成致密的氧化膜而____ ,保护内部金属不再与酸反应,所以可以用____ 制容器或____ 制容器盛放浓硝酸。加热时,铁、铝可以与浓硝酸反应。
③与非金属反应
写出碳与浓硝酸在加热时反应的化学方程式:____ 。
(1)酸的通性
写出下列反应的离子方程式:
①硝酸和氢氧化钠反应:
②硝酸和氧化钠反应:
③硝酸和碳酸钙反应:
(2)不稳定性:见光或受热易分解,化学方程式为
长期存放的浓硝酸呈黄色是因为其分解生成的
(3)强氧化性
①和金属(Cu)反应的实验探究
| 实验操作 |  两支试管中分别加入2 mL浓硝酸和稀硝酸 |
| 实验现象 | 浓硝酸反应比较 |
| 实验结论 | 硝酸无论浓、稀都有 |
写出上述反应的化学方程式:
②与Fe、Al反应
常温下浓硝酸可使铁、铝表面形成致密的氧化膜而
③与非金属反应
写出碳与浓硝酸在加热时反应的化学方程式:
您最近半年使用:0次
名校
10 . 根据所学知识,回答下列问题:
(1)《本草纲目》对白酒(俗称烧酒)的制造过程有如下叙述:“烧酒非古法也,自元时创始,其法用浓酒和糟入甑,蒸令气上,用器承滴露”,“凡酸坏之酒,皆可蒸烧”,“以烧酒复烧二次……价值数倍也”。文中涉及的操作方法是___ 。
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是___ 。
(3)欲使3molVO2+全部转化为VO ,则需要氧化剂KClO3(还原产物为Cl-)至少
,则需要氧化剂KClO3(还原产物为Cl-)至少___ mol。
(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是___ (用化学方程式表示)。
(5)下列变化为化学变化的是___ (填标号)。
A.CaCl2的潮解
B.钠的焰色反应
C.常温下,Fe遇浓硫酸钝化
(1)《本草纲目》对白酒(俗称烧酒)的制造过程有如下叙述:“烧酒非古法也,自元时创始,其法用浓酒和糟入甑,蒸令气上,用器承滴露”,“凡酸坏之酒,皆可蒸烧”,“以烧酒复烧二次……价值数倍也”。文中涉及的操作方法是
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是
(3)欲使3molVO2+全部转化为VO
 ,则需要氧化剂KClO3(还原产物为Cl-)至少
,则需要氧化剂KClO3(还原产物为Cl-)至少(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是
(5)下列变化为化学变化的是
A.CaCl2的潮解
B.钠的焰色反应
C.常温下,Fe遇浓硫酸钝化
您最近半年使用:0次



