解题方法
1 . 实验室用固体烧碱配制480mL0.1mol⋅L−1NaOH溶液。
(1)配制上述溶液时需称量NaOH固体的质量为__________ g(保留两位小数)
(2)配制过程中不需要使用下列仪器中的_______ (填仪器序号),其中还缺少的玻璃仪器是_________ 、___________ (填仪器名称)。_______ 。
A.用适量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量蒸馏水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加蒸馏水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加蒸馏水,直到液面接近刻度线1~2cm处
(4)在容量瓶内确定溶液体积的过程中,当液面离容量瓶颈部的刻度线1~2cm时的做法是_______
(5)下列的实验操作可能导致配制的溶液浓度偏高的是(填序号)_______ 。
①称量NaOH固体时,砝码生锈
②移液时,未洗涤烧杯和玻璃棒
③定容时俯视容量瓶刻度线
④摇匀后液面低于刻度线,继续加水至刻度线
⑤容量瓶内有少量水
(1)配制上述溶液时需称量NaOH固体的质量为
(2)配制过程中不需要使用下列仪器中的
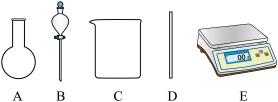
A.用适量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量蒸馏水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加蒸馏水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加蒸馏水,直到液面接近刻度线1~2cm处
(4)在容量瓶内确定溶液体积的过程中,当液面离容量瓶颈部的刻度线1~2cm时的做法是
(5)下列的实验操作可能导致配制的溶液浓度偏高的是(填序号)
①称量NaOH固体时,砝码生锈
②移液时,未洗涤烧杯和玻璃棒
③定容时俯视容量瓶刻度线
④摇匀后液面低于刻度线,继续加水至刻度线
⑤容量瓶内有少量水
您最近一年使用:0次
解题方法
2 . 某学生欲用下列装置制取纯净FeCl3固体。其中A是Cl2的发生装置,C、D为气体净化装置,E硬质玻璃管中装有细铁丝网,F为干燥的空广口瓶,烧杯G为尾气吸收装置。
(1)该装置中有一明显错误是____________ (填字母)。
(2)D中所装试剂为_____________ ,C装置的作用是___________________ 。
(3)A中发生反应的化学方程式是__________________ ,G中发生反应的离子方程式是________________ 。
(4)若用100mL 12mol/L盐酸与足量MnO2充分反应,生成的Cl2体积(标准状况)________________ (填“大于”“小于”或“等于”)6.72 L。
(5)用所制取的FeCl3固体制成Fe(OH)3胶体,区分胶体和溶液常用________ ,分离胶体和溶液常用的方法叫__________ 。

(1)该装置中有一明显错误是
(2)D中所装试剂为
(3)A中发生反应的化学方程式是
(4)若用100mL 12mol/L盐酸与足量MnO2充分反应,生成的Cl2体积(标准状况)
(5)用所制取的FeCl3固体制成Fe(OH)3胶体,区分胶体和溶液常用
您最近一年使用:0次
解题方法
3 . 利用铁元素价类二维图可以多角度研究含铁物质的性质及转化关系,请完成下列问题。__________ 。
A.Fe B. C.
C.
(2)下列说法正确的是___________ 。 粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为
粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为__________ ,
(4)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:___________ 。
(5)人体血红蛋白分子中含有 ,正是这些
,正是这些 使血红蛋白分子具有载氧功能。亚硝酸钠(
使血红蛋白分子具有载氧功能。亚硝酸钠( )可将人体血红蛋白中的
)可将人体血红蛋白中的 转化为
转化为 ,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中
,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中 发生
发生__________ 反应,说明亚硝酸钠具有__________ 性;误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有__________ 性。
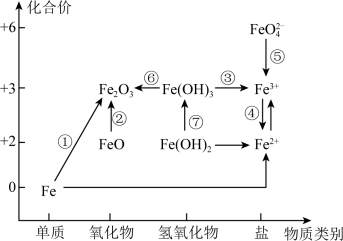
A.Fe B.
 C.
C.
(2)下列说法正确的是
A. 是碱性氧化物
是碱性氧化物
B.铁与高温水蒸气的反应可实现上述转化①
C.FeO是一种黑色粉末,不稳定,在空气中受热,迅速发生转化②
(3)取少量 粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为
粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为(4)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
(5)人体血红蛋白分子中含有
 ,正是这些
,正是这些 使血红蛋白分子具有载氧功能。亚硝酸钠(
使血红蛋白分子具有载氧功能。亚硝酸钠( )可将人体血红蛋白中的
)可将人体血红蛋白中的 转化为
转化为 ,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中
,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中 发生
发生
您最近一年使用:0次
解题方法
4 . I.根据物质的组成、结构、性质等进行分类,可预测物质的性质及变化:
现有下列九种物质:①HCl气体②固体Cu③乙醇④CO2⑤熔融NaCl⑥Al2O3固体⑦硫酸溶液⑧NaHCO3固体⑨BaSO4固体。按照不同的依据对其进行分类:
(1)所给状态能导电的是________ ,属于电解质的是_______ ;(均填序号)。
(2)属于酸式盐的物质为___________ (填序号),其电离方程式为___________ 。
Ⅱ.物质的量是联系宏观和微观的桥梁:
(3)40.5g某金属氧化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为___________ 。
(4)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为___________ 。
(5)在同温同压下,等质量的CO和CO2.其体积之比为___________ ,密度之比为___________ 。
现有下列九种物质:①HCl气体②固体Cu③乙醇④CO2⑤熔融NaCl⑥Al2O3固体⑦硫酸溶液⑧NaHCO3固体⑨BaSO4固体。按照不同的依据对其进行分类:
(1)所给状态能导电的是
(2)属于酸式盐的物质为
Ⅱ.物质的量是联系宏观和微观的桥梁:
(3)40.5g某金属氧化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为
(4)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为
(5)在同温同压下,等质量的CO和CO2.其体积之比为
您最近一年使用:0次
5 . 类比是研究物质性质的常用方法之一、下列类比正确的是
①Cu与 能化合生成
能化合生成 ,则Fe与
,则Fe与 能化合生成
能化合生成
②Mg在空气中燃烧生成MgO,则Na在空气中燃烧生成
③ 可以治疗胃酸过多,则NaOH也可以治疗胃酸过多
可以治疗胃酸过多,则NaOH也可以治疗胃酸过多
④Fe可以置换出 溶液中的铜,则Al也可以置换出
溶液中的铜,则Al也可以置换出 溶液中的铜
溶液中的铜
①Cu与
 能化合生成
能化合生成 ,则Fe与
,则Fe与 能化合生成
能化合生成
②Mg在空气中燃烧生成MgO,则Na在空气中燃烧生成

③
 可以治疗胃酸过多,则NaOH也可以治疗胃酸过多
可以治疗胃酸过多,则NaOH也可以治疗胃酸过多④Fe可以置换出
 溶液中的铜,则Al也可以置换出
溶液中的铜,则Al也可以置换出 溶液中的铜
溶液中的铜| A.①④ | B.②③ | C.①③ | D.②④ |
您最近一年使用:0次
6 . 常温常压下,用等质量的CH4、CO2、O2、SO2分别吹出四个气球,其中气体为CH4的是
|
|
|
|
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 将 通入
通入 溶液至饱和的过程中,始终未观察到溶液中出现浑浊,若再通入另一种气体
溶液至饱和的过程中,始终未观察到溶液中出现浑浊,若再通入另一种气体 ,则产生白色沉淀,制备气体
,则产生白色沉淀,制备气体 的试剂不能是
的试剂不能是
 通入
通入 溶液至饱和的过程中,始终未观察到溶液中出现浑浊,若再通入另一种气体
溶液至饱和的过程中,始终未观察到溶液中出现浑浊,若再通入另一种气体 ,则产生白色沉淀,制备气体
,则产生白色沉淀,制备气体 的试剂不能是
的试剂不能是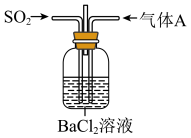
A. 和 和 | B.大理石和稀盐酸 |
C. 和浓硝酸 和浓硝酸 | D. 和浓盐酸 和浓盐酸 |
您最近一年使用:0次
2024-04-27更新
|
64次组卷
|
14卷引用:天津市第一中学2023-2024学年高一下学期5月第五章单元检测(月考)化学试题
天津市第一中学2023-2024学年高一下学期5月第五章单元检测(月考)化学试题【区级联考】北京市西城区2018-2019学年高一第一学期期末考试化学试题【全国百强校】四川省成都外国语学校2018-2019学年高一下学期入学考试化学试题四川省威远中学2018-2019学年高一下学期期中考试化学试题鲁科版(2019)高一必修第一册第三章B 素养拓展区 过综合 章末素养综合检测江西省上饶市铅山县第一中学2020-2021学年上学期高一联考(自招班)化学试题山西省阳泉市第一中学校2022-2023学年高一下学期期中考试化学试题 天津市滨海新区田家炳中学2023-2024学年高三上学期第二次月考化学试题安徽省淮北市第一中学2023-2024学年高一下学期3月月考化学试题云南省大理白族自治州祥云祥华中学2023-2024学年高一下学期3月月考化学试题河北安平中学2020届高三上学期第二次月考化学试题(已下线)小题必刷19 硫及其化合物——2021年高考化学一轮复习小题必刷(通用版)(已下线)化学(上海A卷)-学易金卷:2023年高考第一次模拟考试卷(已下线)专题突破卷04?非金属及其化合物?-2024年高考化学一轮复习考点通关卷(新教材新高考)
解题方法
8 . “灌钢法”是我国古代劳动人民对钢铁冶炼技术的重大贡献,陶弘景在《本草经集注》中提到“钢铁是杂炼生鍒作刀镰者”。“灌钢法”主要是将生铁和熟铁(含碳量约0.1%)混合加热,生铁熔化灌入熟铁,再锻打成钢。下列说法错误的是
| A.钢是以铁为主的含碳合金 |
| B.钢的含碳量越高,硬度和脆性越大 |
| C.生铁由于含碳量高,熔点比纯铁高 |
D.冶炼铁的原料之一赤铁矿的主要成分为 ,俗称铁红 ,俗称铁红 |
您最近一年使用:0次
9 . (Ⅰ)已知A为常见的金属单质。B俗称磁性氯化铁。根据如图所示的关系:
B:_______ D:_______ 。
(2)写出③的离子方程式:_______ 。
(3)写出④的化学方程式:_______ 。
(4)写出⑤的化学方程式:_______ 。
(5)写出E→F的现象_______ 。
写出E→F的化学方程式_______ 。
(Ⅱ)某兴趣小组同学为探究黑木耳中的含铁量,进行如下实验。已知:
ⅰ.黑木耳富含蛋白质、糖类、卵磷脂、铁及一些还原性物质等。每100克黑木耳含铁高达185毫克。
ⅱ.紫色的 溶液在酸性条件下有强氧化性,其还原产物是无色的
溶液在酸性条件下有强氧化性,其还原产物是无色的 。
。
ⅲ. 与铁氰化钾(
与铁氰化钾(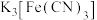 )溶液反应生成蓝色沉淀。
)溶液反应生成蓝色沉淀。
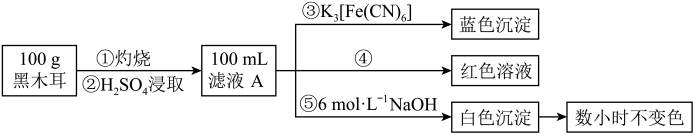
为确定黑木耳中含有铁元素,甲同学设计实验方案如图。_______ 。
(7)步骤④检验 所用试剂是
所用试剂是_______ 溶液。
(8)下列有关上述实验得出的结论正确的是_______ (填字母符号)。
a.黑木耳中一定含 和
和
b.滤液A中一定含 和
和
c.白色沉淀中一定含
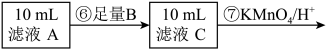
为测定黑木耳中铁元素的含量,乙同学设计实验方案如下。
(10)步骤⑦中观察到的实验现象是_______ ,反应的离子方程式是_______ 。

B:
(2)写出③的离子方程式:
(3)写出④的化学方程式:
(4)写出⑤的化学方程式:
(5)写出E→F的现象
写出E→F的化学方程式
(Ⅱ)某兴趣小组同学为探究黑木耳中的含铁量,进行如下实验。已知:
ⅰ.黑木耳富含蛋白质、糖类、卵磷脂、铁及一些还原性物质等。每100克黑木耳含铁高达185毫克。
ⅱ.紫色的
 溶液在酸性条件下有强氧化性,其还原产物是无色的
溶液在酸性条件下有强氧化性,其还原产物是无色的 。
。ⅲ.
 与铁氰化钾(
与铁氰化钾(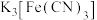 )溶液反应生成蓝色沉淀。
)溶液反应生成蓝色沉淀。为确定黑木耳中含有铁元素,甲同学设计实验方案如图。
(7)步骤④检验
 所用试剂是
所用试剂是(8)下列有关上述实验得出的结论正确的是
a.黑木耳中一定含
 和
和
b.滤液A中一定含
 和
和
c.白色沉淀中一定含

为测定黑木耳中铁元素的含量,乙同学设计实验方案如下。
| A.Na | B.Zn | C.Fe | D.Cu |
(10)步骤⑦中观察到的实验现象是
您最近一年使用:0次
解题方法
10 . 按要求填空
(1)实验室要配制240mL 0.1mol/L 溶液,请回答:配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、天平、量筒、
溶液,请回答:配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、天平、量筒、_______ 、_______
(2)用托盘天平称取碳酸钠固体,其质量为_______
(3)下列主要操作步骤的正确顺序是_______ (填序号)。
①称取一定质量的 ,放入烧杯中,用适量蒸馏水溶解;
,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会造成所配溶液的物质的量浓度_______ (填“偏高”或“偏低”或“无影响”下同)。
定容前,容量瓶中有少量蒸馏水,结果所配溶液的物质的量浓度_______ 。定容时必须使溶液的凹液面与刻度相平,若仰视会使结果浓度_______ 。
(1)实验室要配制240mL 0.1mol/L
 溶液,请回答:配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、天平、量筒、
溶液,请回答:配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、天平、量筒、(2)用托盘天平称取碳酸钠固体,其质量为
(3)下列主要操作步骤的正确顺序是
①称取一定质量的
 ,放入烧杯中,用适量蒸馏水溶解;
,放入烧杯中,用适量蒸馏水溶解;②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会造成所配溶液的物质的量浓度
定容前,容量瓶中有少量蒸馏水,结果所配溶液的物质的量浓度
您最近一年使用:0次