名校
1 . 已知锌与稀盐酸反应放热,某学生为了探究反应过程中的速率变化,用排水集气法收集反应放出的氢气。所用稀盐酸浓度有1.00mol·L-1、2.00mol·L-1两种浓度,每次实验稀盐酸的用量为25.00mL,锌有细颗粒与粗颗粒两种规格,用量为6.50g。实验温度为298K、308K。
(1)完成以下实验设计(填写表格中空白项),并在实验目的一栏中填出对应的实验编号:
(2)实验①记录如下(换算成标况):
①计算在30s~40s范围内盐酸的平均反应速率ν(HCl)=_________ (忽略溶液体积变化)。
②反应速率最大的时间段(如0s~10s)为_________ ,可能原因是_________ ;
(3)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在盐酸溶液中分别加入等体积的下列溶液以减慢反应速率,在不影响产生H2气体总量的情况下,你认为他上述做法中可行的是_________(填相应字母);
(4)某化学研究小组的同学为比较Fe3+和Cu2+对H2O2分解的催化效果,设计了图所示的实验。_________ 现象,比较得出比较Fe3+和Cu2+对H2O2分解的催化效果结论。
②某同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_________ 。
(1)完成以下实验设计(填写表格中空白项),并在实验目的一栏中填出对应的实验编号:
| 编号 | T/K | 锌规格 | 盐酸浓度/mol·L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (I)实验①和②探究盐酸浓度对该反应速率的影响; (II)实验①和 (III)实验①和 |
| ② | 298 | 粗颗粒 | 1.00 | |
| ③ | 308 | 粗颗粒 | 2.00 | |
| ④ | 298 | 细颗粒 | 2.00 |
| 时间(s) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 氢气体积(mL) | 16.8 | 39.2 | 67.2 | 224 | 420 | 492.8 | 520.8 | 543.2 | 554.4 | 560 |
②反应速率最大的时间段(如0s~10s)为
(3)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在盐酸溶液中分别加入等体积的下列溶液以减慢反应速率,在不影响产生H2气体总量的情况下,你认为他上述做法中可行的是_________(填相应字母);
| A.NaNO3溶液 | B.NaCl溶液 | C.CuSO4溶液 | D.Na2CO3 |

②某同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是
您最近一年使用:0次
2022-11-11更新
|
1508次组卷
|
6卷引用:清单04 化学反应的速率和限度(考点清单)(讲+练)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)
(已下线)清单04 化学反应的速率和限度(考点清单)(讲+练)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)广东省潮州市饶平县第二中学2021-2022学年高一下学期期中化学试题(已下线)专题07 化学反应的速率和限度(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)第六章 化学反应与能量(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)云南省昆明市官渡区第三中学2022-2023学年高一下学期期中考试化学试题(已下线)第六章 化学反应与能量【单元测试A卷】
解题方法
2 . 某实验小组,要检验淀粉的水解程度,设计以下实验操作过程:
①取少量淀粉加水制成溶液;②加热;③加入碱液,中和至碱性;④加入银氨溶液;⑤加入几滴稀硫酸;⑥再加热(水浴);⑦加入几滴碘水。
甲、乙、丙三个同学分别做了以下三个实验,指出他们的实验目的或现象。
(1)甲:①→⑤→②→③→④→⑥;现象:无银镜产生。
甲同学的实验目的是___________ 。
(2)乙:①→⑤→②→③→④→⑥;现象:有银镜产生;①→⑤→②→⑦;现象:溶液变蓝。乙同学的实验目的是___________ 。
(3)丙:①→⑤→②→⑦;现象:___________ 。
丙同学的实验目的是证明淀粉已完全水解。
①取少量淀粉加水制成溶液;②加热;③加入碱液,中和至碱性;④加入银氨溶液;⑤加入几滴稀硫酸;⑥再加热(水浴);⑦加入几滴碘水。
甲、乙、丙三个同学分别做了以下三个实验,指出他们的实验目的或现象。
(1)甲:①→⑤→②→③→④→⑥;现象:无银镜产生。
甲同学的实验目的是
(2)乙:①→⑤→②→③→④→⑥;现象:有银镜产生;①→⑤→②→⑦;现象:溶液变蓝。乙同学的实验目的是
(3)丙:①→⑤→②→⑦;现象:
丙同学的实验目的是证明淀粉已完全水解。
您最近一年使用:0次
2022-03-02更新
|
307次组卷
|
2卷引用:课前-7.4.1 糖类-人教2019必修第二册
3 . 下列实验装置和原理能达到实验目的的是
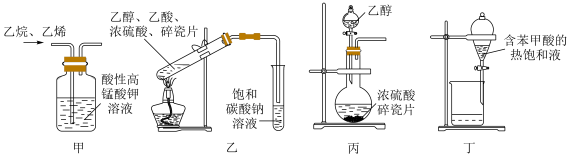
| A.装置甲可用于除去乙烷中乙烯 | B.装置乙可用于制取少量乙酸乙酯 |
| C.装置丙可用于制取少量乙烯 | D.装置丁可用于除去苯甲酸中的难溶性杂质 |
您最近一年使用:0次
4 . 某同学设想用如图装置来验证浓硫酸的某些性质,其中不能达到目的的是
| 实验目的 | A.吸水性 | B.脱水性 |
| 装置 |
|
|
| 实验目的 | C.溶解放热 | D.强氧化性 |
| 装置 |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 侯氏制碱法中制取 的原理为
的原理为 。下列实验装置合理、操作规范,能达到实验目的的是
。下列实验装置合理、操作规范,能达到实验目的的是
 的原理为
的原理为 。下列实验装置合理、操作规范,能达到实验目的的是
。下列实验装置合理、操作规范,能达到实验目的的是| 选项 | A | B |
| 目的 | 制取 | 除去 中的 中的 |
| 操作 |
|
|
| 选项 | C | D |
| 目的 | 制备 | 分离出 |
| 操作 |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 钢铁的电化学腐蚀原理___________ ;
(2)实验现象:a装置右边的小试管中液面________ ;b装置中右边小试管中液面_________ 。
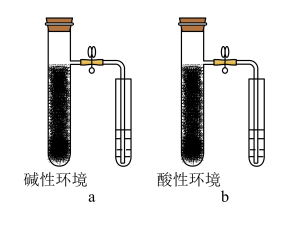
(2)实验现象:a装置右边的小试管中液面
您最近一年使用:0次
24-25高三上·全国·课前预习
7 . 某化学兴趣小组在实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取SO2并完成相关性质探究(不考虑水蒸气)。
(1)有同学认为制得的SO2中可能混有杂质,其化学式为___________ 和___________ ,原因是___________ 。
(2)为验证气体成分,兴趣小组同学设计了下图所示装置进行了实验探究。___________ ,装置C中品红溶液的作用是___________ ;
②装置D中加入的试剂为___________ ;
③装置G中可能出现的现象为___________ ;
④装置H的作用为___________ 。
(1)有同学认为制得的SO2中可能混有杂质,其化学式为
(2)为验证气体成分,兴趣小组同学设计了下图所示装置进行了实验探究。
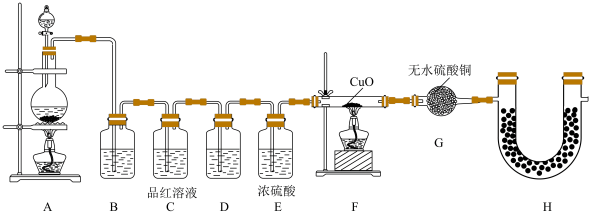
②装置D中加入的试剂为
③装置G中可能出现的现象为
④装置H的作用为
您最近一年使用:0次
8 . 下列实验处理可行的有几项
①将CH3CH(OH)CHO与NaOH的醇溶液共热制备CH3CH=CH2
②向丙烯醛(CH2=CHCHO)中加入溴水,观察橙色褪去,能证明结构中存在碳碳双键
③实验时手指不小心沾上苯酚,立即用乙醇冲洗,再用水冲洗
④用溴水除去混在苯中的己烯,分液得到纯净的苯
⑤利用重结晶法可以提纯含有少量NaCl的苯甲酸
⑥在分别盛有少量苯和四氯化碳的试管中加碘水后振荡,可根据现象区分苯和四氯化碳
⑦向含有苯酚的苯中加入碳酸钠溶液,反应后分液,可除去苯中的少量苯酚
⑧用碳酸钠溶液可区分乙醇、甲苯、乙酸、溴乙烷和苯
⑨煤油的主要成分为烃类物质,可用来保存金属钠
①将CH3CH(OH)CHO与NaOH的醇溶液共热制备CH3CH=CH2
②向丙烯醛(CH2=CHCHO)中加入溴水,观察橙色褪去,能证明结构中存在碳碳双键
③实验时手指不小心沾上苯酚,立即用乙醇冲洗,再用水冲洗
④用溴水除去混在苯中的己烯,分液得到纯净的苯
⑤利用重结晶法可以提纯含有少量NaCl的苯甲酸
⑥在分别盛有少量苯和四氯化碳的试管中加碘水后振荡,可根据现象区分苯和四氯化碳
⑦向含有苯酚的苯中加入碳酸钠溶液,反应后分液,可除去苯中的少量苯酚
⑧用碳酸钠溶液可区分乙醇、甲苯、乙酸、溴乙烷和苯
⑨煤油的主要成分为烃类物质,可用来保存金属钠
| A.3 | B.4 | C.5 | D.6 |
您最近一年使用:0次
9 . 炔烃的结构和性质
(1)炔烃
炔烃的官能团是___________ ,一般只含有一个官能团时通式为___________ (n≥2)。炔烃的物理性质的递变规律与烷烃和烯烃的___________ ,沸点随分子中碳原子数的递增而___________ ,常温下,碳原子数不大于___________ 的炔烃为气态。
(2)乙炔的物理性质
乙炔(俗称___________ )是最简单的炔烃。乙炔是___________ 色、___________ 的气体,___________ 溶于水,___________ 溶于有机溶剂。
(3)乙炔的表示方法及结构特点
分子式:___________ ,电子式:___________ ,结构式:___________ ,结构简式:___________ ,键线式:___________ 。
乙炔分子为___________ 形结构,相邻两个键之间的夹角为___________ ,碳原子采取___________ 杂化。
(4)乙炔的化学性质
(i)实验探究(课本P35)
为减小电石与水反应的速率,可用___________ 代替水作反应试剂。
(ii)化学性质
①氧化反应
a.乙炔的燃烧:___________ 。
b.可使酸性KMnO4溶液___________ 。
②加成反应
a.乙炔与溴的反应:___________ (1,2-二溴乙烯);___________ (1,1,2,2-四溴乙烷)。
b.乙炔与氢气的反应(1:1):___________ 。
c.乙炔与HCl的反应(1:1):___________ 。
d.乙炔与H2O的反应:___________ 。
③加聚反应:___________ ,聚乙炔可用于制备___________ 材料。
(1)炔烃
炔烃的官能团是
(2)乙炔的物理性质
乙炔(俗称
(3)乙炔的表示方法及结构特点
分子式:
乙炔分子为
(4)乙炔的化学性质
(i)实验探究(课本P35)
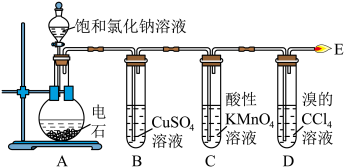
| 实验现象 | 结论或化学方程式 | |
| A | 反应 | |
| B | 有 | 乙炔中的杂质气体 |
| C | 溶液紫红色褪去 | |
| D | 溶液橙红色褪去 | |
| E | 火焰 | CH≡CH |
(ii)化学性质
①氧化反应
a.乙炔的燃烧:
b.可使酸性KMnO4溶液
②加成反应
a.乙炔与溴的反应:
b.乙炔与氢气的反应(1:1):
c.乙炔与HCl的反应(1:1):
d.乙炔与H2O的反应:
③加聚反应:
您最近一年使用:0次
10 . 回答下列问题:
(1)甲同学利用下列装置来进行铜跟浓硫酸反应实验。_______ 。
②乙同学认为,若要用铜制取硫酸铜,可以先用铜和氧气反应生成氧化铜,然后利用氧化铜和稀硫酸反应可以得到硫酸铜。若要制取硫酸铜,请你从环境保护和节约资源的角度分析,比较甲同学和乙同学制取硫酸铜的方法中更合理的是_______ ,原因是 _______ 。
(2)丙同学利用下图的方法实验室制取并验证 某些性质,并将实验情况记录在表中,请完成以下表格:
某些性质,并将实验情况记录在表中,请完成以下表格:
(1)甲同学利用下列装置来进行铜跟浓硫酸反应实验。
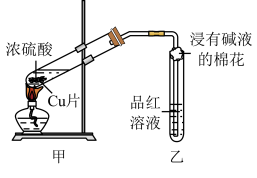
②乙同学认为,若要用铜制取硫酸铜,可以先用铜和氧气反应生成氧化铜,然后利用氧化铜和稀硫酸反应可以得到硫酸铜。若要制取硫酸铜,请你从环境保护和节约资源的角度分析,比较甲同学和乙同学制取硫酸铜的方法中更合理的是
(2)丙同学利用下图的方法实验室制取并验证
 某些性质,并将实验情况记录在表中,请完成以下表格:
某些性质,并将实验情况记录在表中,请完成以下表格: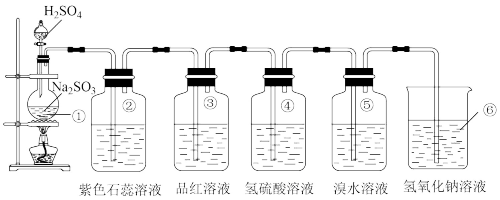
| 装置序号 | 实验现象或作用 | 实验结论或化学方程式 |
| ① | 有气泡产生 | 化学方程式为: |
| ② | 紫色石蕊试液变 | 证明 溶于水显酸性 溶于水显酸性 |
| ③ | 品红溶液褪色 | 证明 具有 具有 |
| ④ | 溶液变浑浊 | 证明 具有 具有 |
| ⑤ | 溴水褪色 | 证明 具有 具有 |
| ⑥ | 吸收尾气 | 证明 属于 属于 |
您最近一年使用:0次
2023-01-25更新
|
822次组卷
|
4卷引用:清单01 硫及其化合物的性质(考点清单)(讲+练)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)
(已下线)清单01 硫及其化合物的性质(考点清单)(讲+练)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)山东省济南市深泉外国语学校2022-2023学年高一上学期期末考试化学试题(已下线)专题01 硫及其化合物的性质及转化(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)(已下线)猜想03 气体的制取、无机实验探究、无机综合应用(考题猜想)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)