解题方法
1 . 下列设计的实验方案能达到实验目的的是
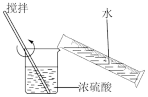
| A.制备银氨溶液:向2%的氨水中逐滴加入足量的2%AgNO3溶液 |
| B.除去MgCl2溶液中少量FeCl3:向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌,充分反应后过滤 |
| C.比较Ag2CO3与AgCl溶度积大小:向浓度均为0.1mol·L-1的Na2CO3和NaCl的混合溶液中滴加0.1mol·L-1AgNO3溶液,观察现象 |
| D.验证Fe3+与I-的反应有一定限度:向5mL0.1mol·L-1KI溶液中滴入0.1mol·L-1FeCl3溶液5~6滴,加2mLCCl4振荡,静置后取上层清液滴加KSCN溶液,观察现象 |
您最近一年使用:0次
名校
2 . 实验装置不能达到实验目的的是
| A | B | C | D |
|
|
|
|
| 稀释浓硫酸 | 制备并检验 气体 气体 | 用该装置制备少量白色的 沉淀 沉淀 | 吸收NO中的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-12-30更新
|
889次组卷
|
12卷引用:湖南省绥宁县第一中学2022-2023学年高一下学期学科知识竞赛化学试题
湖南省绥宁县第一中学2022-2023学年高一下学期学科知识竞赛化学试题福建省厦门第一中学2021-2022学年高一上学期12月月考化学试题(已下线)解密11 化学实验(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)湖北省襄阳市第一中学2021-2022学年高一下学期3月月考化学试题山西省榆次第一中学校2021-2022学年高一下学期期中线上测试化学试题辽宁省东北师范大学连山实验高中2021-2022学年高一下学期第一次线上考试化学试题(已下线)仿真卷02-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)化学(人教版2019B卷)-学易金卷:2022-2023学年高一下学期期中考前必刷卷河南省驻马店市2022-2023学年高一下学期4月期中考试化学试题新疆塔城地区第一高级中学2022-2023学年高一下学期5月期中考试化学试题安徽省安庆市第九中学2022-2023学年高一下学期期中考试化学试题陕西省咸阳市三原县北城中学2023-2024学年高一下学期第一次月考化学试题
2010高三·湖北·竞赛
解题方法
3 . 化学实验兴趣小组在实验室进行氢气在氯气中的燃烧实验。
(1)设计如下图所示装置I制备和收集干燥纯净的氯气以备后续实验;

烧瓶中发生反应的离子方程式为_______ ;
请根据实验目的将装置I中虚线框内装置补充完整并在括号内注明所需试剂;_________
(2)在右图所示装置Ⅱ中,在试管中先加入过量铁粉,再滴入少量CuSO4溶液,最后加入一定量稀盐酸,塞上胶塞,观察到有大量气泡产生。

①检查制取氢气装置气密性的操作方法是____________
②当点燃氢后,将导管伸入盛有氯气的集气瓶中,观察到的现象是____________
(3)当氢气停止燃烧后,取出导管,同学们进行了分组探究实验。A组同学发现制氢气后的试管中还有较多固体剩余,同学们将足量氯气通入试管中,发现固体全部消失,但未观察到有气泡产生,请解释可能原因(用离子方程式表示);_______ 、________ 、_______ 、____ ;B组同学向集气瓶中注入适量水,用力振荡后,向其中加入少量Na2S2O3溶液,发现溶液中没有出现黄色沉淀,但再向溶液中滴入稀盐酸酸化的氯化钡溶液后,生成了白色沉淀。[已知Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O],同学们分析是由于集气瓶中还有少量氯气残留的缘故。可以解释该实验现象的两个离子方程式是:①_____________ ②____________
(1)设计如下图所示装置I制备和收集干燥纯净的氯气以备后续实验;

烧瓶中发生反应的离子方程式为
请根据实验目的将装置I中虚线框内装置补充完整并在括号内注明所需试剂;
(2)在右图所示装置Ⅱ中,在试管中先加入过量铁粉,再滴入少量CuSO4溶液,最后加入一定量稀盐酸,塞上胶塞,观察到有大量气泡产生。

①检查制取氢气装置气密性的操作方法是
②当点燃氢后,将导管伸入盛有氯气的集气瓶中,观察到的现象是
(3)当氢气停止燃烧后,取出导管,同学们进行了分组探究实验。A组同学发现制氢气后的试管中还有较多固体剩余,同学们将足量氯气通入试管中,发现固体全部消失,但未观察到有气泡产生,请解释可能原因(用离子方程式表示);
您最近一年使用:0次
4 . 研究性学习小组设计了如下图所示实验装置(部分夹持装置已省略)制备NO,并进行NO的检验和性质探究实验。

已知:NO在 溶液中发生反应
溶液中发生反应 (棕色),该反应可以用于检验NO。
(棕色),该反应可以用于检验NO。
(1)仪器a的名称是_______ 。装置A内发生主要反应的离子方程式为_______ 。
(2)实验开始前,向装置中通入一段时间 的目的是
的目的是_______ 。
(3)装置B、C中蒸馏水和无水 的作用分别是
的作用分别是_______ 、_______ 。
(4)装置D中Fe粉与NO以物质的量之比 发生反应,生成
发生反应,生成 和另一种固体产物。该固体产物的化学式为
和另一种固体产物。该固体产物的化学式为_______ 。
(5)进行实验时,装置E中的实验现象为_______ 。

已知:NO在
 溶液中发生反应
溶液中发生反应 (棕色),该反应可以用于检验NO。
(棕色),该反应可以用于检验NO。(1)仪器a的名称是
(2)实验开始前,向装置中通入一段时间
 的目的是
的目的是(3)装置B、C中蒸馏水和无水
 的作用分别是
的作用分别是(4)装置D中Fe粉与NO以物质的量之比
 发生反应,生成
发生反应,生成 和另一种固体产物。该固体产物的化学式为
和另一种固体产物。该固体产物的化学式为(5)进行实验时,装置E中的实验现象为
您最近一年使用:0次
名校
解题方法
5 . 乙烯是一种重要的化工原料,某同学设计实验探究工业制备乙烯的原理和乙烯的主要化学性质,实验装置如图所示(已知A装置可产生乙烯气体)。
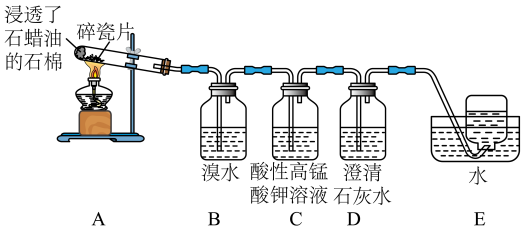
(1)乙烯的电子式为___________ ,其分子空间结构为___________
(2)用化学方程式解释B装置中的实验现象:___________ 。
(3)C装置中的现象是___________ ,其发生反应的反应类型是___________ 。
(4)查阅资料可知。乙烯与酸性高锰酸钾溶液反应产生二氧化碳,则除去甲烷中乙烯的方法是___________
(5)工业上利用乙烯水化制备乙醇,其对应的化学方程式为___________ ;反应类型为___________

(1)乙烯的电子式为
(2)用化学方程式解释B装置中的实验现象:
(3)C装置中的现象是
(4)查阅资料可知。乙烯与酸性高锰酸钾溶液反应产生二氧化碳,则除去甲烷中乙烯的方法是___________
| A.将气体通入水中 | B.将气体通过装溴水的洗气瓶 |
| C.将气体通过装酸性高锰酸钾溶液的洗气瓶 | D.将气体通入氢氧化钠溶液中 |
您最近一年使用:0次
2022-05-16更新
|
946次组卷
|
3卷引用:甘肃省武威第七中学2021-2022学年高一下学期学科竞赛化学试题
解题方法
6 . 某合作学习小组在实验室进行了由食盐制备纯碱的实验探究。请回答下列实验方案中的有关问题:
(1)制备原理:饱和氯化钠与碳酸氢铵反应得碳酸氢钠晶体,碳酸氢钠分解得到纯碱。反应为___ (写化学方程式)。
制备碳酸氢钠有以下三种方案,其中最好的方案是___ (填方案代号)。
方案A:分别将二氧化碳和氨气通入饱和食盐水中;
方案B:将二氧化碳通入含大量氨的饱和食盐水中;
方案C:将氨气通入含二氧化碳的饱和食盐水中。
(2)制备流程:
配制含氨的饱和食盐水→配制二氧化碳→制备碳酸氢钠→制备碳酸钠
实验中使用的部分简易装置如图所示:

其中装置乙的作用为___ ,装置丙的作用为___ ;实验中在装置乙丙之间还应连接制备碳酸氢钠的装置,且反应温度控制在30-35℃,请在答题卡上方框内画出该装置的简易图示___ 。实验的最后一步是将碳酸氢钠晶体转移到___ 中,加热至无水蒸气逸出既得碳酸钠。
(3)实验探究:制备碳酸氢钠的温度要控制在30-35℃,其理由是____ 。
本方法制得的纯碱中可能含有氯化钠,请设计检验实验方案,完成表中内容。
(1)制备原理:饱和氯化钠与碳酸氢铵反应得碳酸氢钠晶体,碳酸氢钠分解得到纯碱。反应为
制备碳酸氢钠有以下三种方案,其中最好的方案是
方案A:分别将二氧化碳和氨气通入饱和食盐水中;
方案B:将二氧化碳通入含大量氨的饱和食盐水中;
方案C:将氨气通入含二氧化碳的饱和食盐水中。
(2)制备流程:
配制含氨的饱和食盐水→配制二氧化碳→制备碳酸氢钠→制备碳酸钠
实验中使用的部分简易装置如图所示:

其中装置乙的作用为
(3)实验探究:制备碳酸氢钠的温度要控制在30-35℃,其理由是
本方法制得的纯碱中可能含有氯化钠,请设计检验实验方案,完成表中内容。
| 实验步骤 | 实验现象与结论 |
您最近一年使用:0次
7 . 已知反应:Na2SO3 +S Na2S2O3(硫代硫酸钠)。常温下在溶液中析出的晶体为Na2S2O3·5H2O。 该晶体于40~45 °C熔化,48 °C分解;易溶于水,不溶于乙醇,如图是有关物质的溶解度曲线。
Na2S2O3(硫代硫酸钠)。常温下在溶液中析出的晶体为Na2S2O3·5H2O。 该晶体于40~45 °C熔化,48 °C分解;易溶于水,不溶于乙醇,如图是有关物质的溶解度曲线。
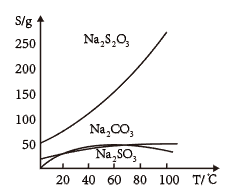
I.现按如下方法制备Na2S2O3·5H2O:将硫化钠和碳酸钠按反应要求比例一并放入三颈瓶中,注入150 mL蒸馏水使其溶解,在分液漏斗中注入浓盐酸,在仪器a中加入亚硫酸钠固体,并按下图安装好装置。

(1)仪器a的名称为_______ ,仪器 b中可放入的是_______ (填字母代号)。
A. BaCl2溶液 B.浓H2SO4 C.酸性KMnO4溶液 D. NaOH溶液
(2)打开分液漏斗活塞,注入浓盐酸使反应产生的二氧化硫气体较均匀地通入Na2S和Na2CO3的混合溶液中,然后用磁力搅拌器搅动并加热,反应原理为:①Na2CO3 +SO2=Na2SO3 + CO2;②_______ ;③_______ ;
④Na2SO3 +S =Na2S2O3。随着二氧化硫气体的通入,可观察到溶液中有大量浅黄色固体析出,继续通二氧化硫气体,反应约半小时。当溶液中pH接近或不小于7时,即可停止通气和加热。溶液pH要控制不小于7的理由是_______ (用文字和相关离子方程式表示)。
II.分离Na2S2O3·5H2O并标定溶液的浓度:
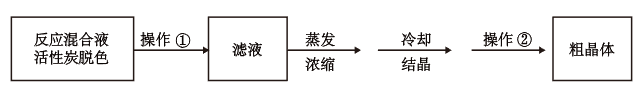
(3)为减少产品的损失,操作①为_______ ,操作②是抽滤洗涤干燥 ,其中洗涤操作是用_______ (填试剂)作洗涤剂。
(4)蒸发时温度不宜过高,其原因是_______ 。
(5)称取一定质量的产品配制成硫代硫酸钠溶液并用间接碘量法标定该溶液的浓度:用分析天平准确称取基准物质K2Cr2O7 0.5880 g。平均分成三份,分别放入三个锥形瓶中。加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I- +Cr2O +14H+= 3I2 +2Cr3+ +7H2O,再加入几滴淀粉溶液,立即用所配的Na2S2O3溶液滴定,发生反应:I2+2S2O
+14H+= 3I2 +2Cr3+ +7H2O,再加入几滴淀粉溶液,立即用所配的Na2S2O3溶液滴定,发生反应:I2+2S2O =2I- +S4O
=2I- +S4O ,滴定终点的现象为
,滴定终点的现象为_______ ,三次所消耗Na2S2O3溶液的平均体积为20.00 mL,则所标定的硫代硫酸钠溶液的浓度为_______ mol/L。
 Na2S2O3(硫代硫酸钠)。常温下在溶液中析出的晶体为Na2S2O3·5H2O。 该晶体于40~45 °C熔化,48 °C分解;易溶于水,不溶于乙醇,如图是有关物质的溶解度曲线。
Na2S2O3(硫代硫酸钠)。常温下在溶液中析出的晶体为Na2S2O3·5H2O。 该晶体于40~45 °C熔化,48 °C分解;易溶于水,不溶于乙醇,如图是有关物质的溶解度曲线。
I.现按如下方法制备Na2S2O3·5H2O:将硫化钠和碳酸钠按反应要求比例一并放入三颈瓶中,注入150 mL蒸馏水使其溶解,在分液漏斗中注入浓盐酸,在仪器a中加入亚硫酸钠固体,并按下图安装好装置。

(1)仪器a的名称为
A. BaCl2溶液 B.浓H2SO4 C.酸性KMnO4溶液 D. NaOH溶液
(2)打开分液漏斗活塞,注入浓盐酸使反应产生的二氧化硫气体较均匀地通入Na2S和Na2CO3的混合溶液中,然后用磁力搅拌器搅动并加热,反应原理为:①Na2CO3 +SO2=Na2SO3 + CO2;②
④Na2SO3 +S =Na2S2O3。随着二氧化硫气体的通入,可观察到溶液中有大量浅黄色固体析出,继续通二氧化硫气体,反应约半小时。当溶液中pH接近或不小于7时,即可停止通气和加热。溶液pH要控制不小于7的理由是
II.分离Na2S2O3·5H2O并标定溶液的浓度:

(3)为减少产品的损失,操作①为
(4)蒸发时温度不宜过高,其原因是
(5)称取一定质量的产品配制成硫代硫酸钠溶液并用间接碘量法标定该溶液的浓度:用分析天平准确称取基准物质K2Cr2O7 0.5880 g。平均分成三份,分别放入三个锥形瓶中。加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I- +Cr2O
 +14H+= 3I2 +2Cr3+ +7H2O,再加入几滴淀粉溶液,立即用所配的Na2S2O3溶液滴定,发生反应:I2+2S2O
+14H+= 3I2 +2Cr3+ +7H2O,再加入几滴淀粉溶液,立即用所配的Na2S2O3溶液滴定,发生反应:I2+2S2O =2I- +S4O
=2I- +S4O ,滴定终点的现象为
,滴定终点的现象为
您最近一年使用:0次
解题方法
8 . 下图是中学化学实验中出现频率较高的装置,它是由物质制备、生成物性质检验和尾气处理三部分组成。请你用中学化学常见试剂设计一个实验,通过乙中的反应和丙中的实验现象,得出三种物质性质递变的结论。试将试剂名称、丙中的实验现象及由此得出的实验结论填入下列空白处。

(1)所用试剂的名称:甲_______ ,乙_______ ,丙_______ 。
(2)丙中现象:_______ 。丙中反应的化学方程式:_______ 。
(3)实验结论:_______ 。

(1)所用试剂的名称:甲
(2)丙中现象:
(3)实验结论:
您最近一年使用:0次
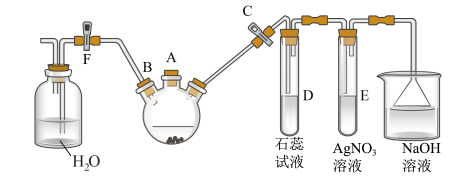
9 . 实验室用下图所示装置制备溴苯_______ 。
(2)D试管内出现的现象为:_______ E试管内出现的现象为:_______ 。
(3)待三口烧瓶中的反应即将结束时(此时气体明显减少),打开F活塞,关闭C活塞,可以看到的现象是_______ 。
(4)反应完毕后的混合物中产物溴苯在上层还是下层_______ ?如何分离_______ ?
(2)D试管内出现的现象为:
(3)待三口烧瓶中的反应即将结束时(此时气体明显减少),打开F活塞,关闭C活塞,可以看到的现象是
(4)反应完毕后的混合物中产物溴苯在上层还是下层
您最近一年使用:0次
解题方法
10 . 下列实验操作及现象均正确的是
| 选项 | 实验目的 | 实验操作 | 实验现象 |
| A | 探究硼酸和碳酸的酸性强弱 | 将足量硼酸滴入Na2CO3溶液中 | 有气泡产生 |
| B | 验证铜和浓硫酸反应的产物中有硫酸铜生成 | 直接向反应后的试管中加入蒸馏水 | 溶液变蓝 |
| C | 探究维生素C可以还原Fe3+ | 向盛有FeCl3溶液的试管中滴加适量浓维生素C溶液 | 溶液由黄色变为浅绿色 |
| D | 探究Fe3+和I-之间的反应为可逆反应 | 向氯化铁溶液中滴入少量 KI溶液,将反应后的溶液两等分,向其中一份滴入KSCN溶液,另一份滴淀粉溶液 | 一份溶液显血红色,另一份溶液显蓝色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次