1 . 下列事实中,不能用化学平衡移动原理解释的是
A.棕色的 体系加压后,颜色先变深后逐渐变浅 体系加压后,颜色先变深后逐渐变浅 |
| B.在配制硫酸亚铁溶液时往往要加入少量铁粉 |
| C.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 |
| D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
您最近一年使用:0次
2 . 表中实验操作、现象与结论对应关系正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向NaAlO2溶液中滴加NaHCO3溶液 | 出现白色沉淀 | NaAlO2与NaHCO3水解相互促进 |
| B | 常温下,用pH计分别测定相同浓度的NaClO溶液和CH3COONa溶液的酸碱性 | NaClO溶液pH较大 | 酸性:HClO<CH3COOH |
| C | 向AgNO3溶液中依次滴加NaCl、KI溶液 | 依次出现白色、黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| D | 白铁皮(镀锌铁)出现刮痕后浸泡在饱和食盐水中,一段时间后滴入几滴K2[Fe(CN)6]溶液 | 无明显现象 | 该过程未发生原电池反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 下列表达式书写不正确的是
A. 的水解方程式: 的水解方程式: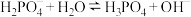 |
B.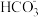 的电离方程式: 的电离方程式: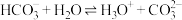 |
C.CaCO3的沉淀溶解平衡表达式: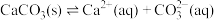 |
D.表示H2燃烧热的热化学方程式:2H2(g)+O2(g)=2H2O(l)  kJ⋅mol kJ⋅mol |
您最近一年使用:0次
4 . 糖类、油脂和蛋白质均为维持人体生命活动所需的营养物质。下列说法正确的是
| A.糖类都只含碳、氢两种元素 |
| B.工业上利用油脂制取肥皂 |
| C.蛋白质能在一定条件下水解生成葡萄糖 |
| D.糖类、油脂和蛋白质都属于高分子化合物 |
您最近一年使用:0次
名校
解题方法
5 . 规范操作是实验的基本要求。下列操作规范的是
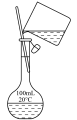 |  | 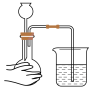 | 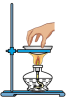 |
| A.转移溶液 | B.加热液体 | C.检查气密性 | D.移走蒸发皿 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 过氧化钙晶体(CaO2·8H2O)在常温下为白色,能溶于酸,难溶于水、乙醇,是一种温和的氧化剂,常用作鱼类长途运输的增氧剂等。
(1)过氧化钙晶体可用下列方法制备:CaCl2+H2O2+2NH3+8H2O=CaO2·8H2O↓+2NH4Cl。
用下图制取装置制备过氧化钙晶体:

①装置A中发生反应的化学方程式为______________________________ 。
②仪器X的名称为________ 。
③为提高CaO2·8H2O的产率,装置B的温度需控制在0 ℃,可采取的方法是__________________________________ 。
(2)测定产品中CaO2·8H2O含量的实验步骤如下:
步骤一:准确称取0.500 0 g产品于有塞锥形瓶中,加入适量蒸馏水和过量的KI晶体,再滴入2 mol·L-1的硫酸溶液,充分反应。
步骤二:向上述锥形瓶中加入几滴淀粉溶液,逐滴加入浓度为0.200 mol·L-1的Na2S2O3溶液至反应完全,滴定至终点,消耗Na2S2O3溶液的体积为20.00 mL。
求产品中CaO2·8H2O的质量分数____ 。(写出计算过程)
已知:CaO2·8H2O +2KI+2H2SO4=CaSO4+K2SO4+I2+10H2O;I2+2S2O =2I-+S4O
=2I-+S4O 。
。
(1)过氧化钙晶体可用下列方法制备:CaCl2+H2O2+2NH3+8H2O=CaO2·8H2O↓+2NH4Cl。
用下图制取装置制备过氧化钙晶体:

①装置A中发生反应的化学方程式为
②仪器X的名称为
③为提高CaO2·8H2O的产率,装置B的温度需控制在0 ℃,可采取的方法是
(2)测定产品中CaO2·8H2O含量的实验步骤如下:
步骤一:准确称取0.500 0 g产品于有塞锥形瓶中,加入适量蒸馏水和过量的KI晶体,再滴入2 mol·L-1的硫酸溶液,充分反应。
步骤二:向上述锥形瓶中加入几滴淀粉溶液,逐滴加入浓度为0.200 mol·L-1的Na2S2O3溶液至反应完全,滴定至终点,消耗Na2S2O3溶液的体积为20.00 mL。
求产品中CaO2·8H2O的质量分数
已知:CaO2·8H2O +2KI+2H2SO4=CaSO4+K2SO4+I2+10H2O;I2+2S2O
 =2I-+S4O
=2I-+S4O 。
。
您最近一年使用:0次
名校
解题方法
7 . 先进的甲醇蒸气重整—变压吸附技术可得到高浓度CO2和H2混合气,化学反应原理是CH3OH+H2O CO2+3H2,其能量变化如图所示。下列说法错误的是
CO2+3H2,其能量变化如图所示。下列说法错误的是
 CO2+3H2,其能量变化如图所示。下列说法错误的是
CO2+3H2,其能量变化如图所示。下列说法错误的是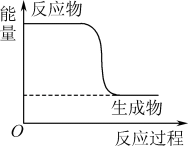
| A.CH3OH转变成H2的过程是一个吸收能量的过程 |
| B.反应物的总能量大于生成物的总能量 |
| C.形成H—H键放出能量 |
| D.断开H—C键吸收能量 |
您最近一年使用:0次
名校
解题方法
8 . 电化学“大气固碳”方法是我国科学家研究发现的,相关装置如图所示。下列说法错误的是

| A.放电时电极A为负极,该电池只可选用无水电解液 |
B.充电时,电极B上发生的反应是 |
C.充电时 的移动方向是从电极B移向电极A 的移动方向是从电极B移向电极A |
| D.放电时,电路中每通过1mol电子,正极区质量增加40g |
您最近一年使用:0次
2023-12-24更新
|
2296次组卷
|
15卷引用:广东省深圳市富源学校2023-2024学年高二上学期模拟预测化学试题
广东省深圳市富源学校2023-2024学年高二上学期模拟预测化学试题广东省部分名校2023-2024学年高三上学期联合质量检测化学试题福建省厦门外国语学校2023-2024学年高二上学期期末模拟考试化学试题新疆乌鲁木齐市第101中学2023-2024学年高二上学期1月期末化学试题云南省昆明市第三中学2023-2024学年高二上学期1月期末化学试题湖南省常德市第一中学2023-2024学年高二上学期期末考试化学试题(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)2024届辽宁省实验中学高三下学期考前模拟训练(五模)化学试卷山西省忻州市名校2023-2024学年高三上学期联合质量检测化学试卷(已下线)题型11 新型电化学装置分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)选择题11-15(已下线)T10-电化学基础(已下线)选择题6-10河北省保定市高碑店市崇德实验中学2023-2024学年高三上学期1月考试化学试题
名校
解题方法
9 . 草酸 是一种易溶于水的二元有机弱酸,常用作还原剂、沉淀剂等,可与酸性
是一种易溶于水的二元有机弱酸,常用作还原剂、沉淀剂等,可与酸性 溶液发生反应:
溶液发生反应: 。
。
(1)探究外界条件对反应速率的影响。
①完成此实验设计,其中:
___________ ,
___________ 。
②对比实验1、2可探究___________ 对反应速率的影响。
(2)某兴趣小组用草酸及草酸盐的性质测定硬水中钙离子的浓度。
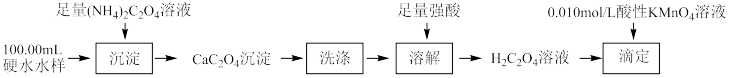
根据消耗酸性 标准溶液的体积即可测定硬水样品中
标准溶液的体积即可测定硬水样品中 的浓度。
的浓度。
①实验过程提及的下列仪器,在使用之前一定要润洗的是___________ (填字母)。
A.容量瓶 B.烧杯 C.锥形瓶 D.滴定管
②滴定过程中___________ (填“需要”或“不需要”)另加指示剂,如何判断滴定终点___________ 。
③本实验滴定管起点和终点的液面位置如图所示,则滴定过程中消耗的 标准溶液为
标准溶液为___________  。该硬水样品中
。该硬水样品中 的浓度为
的浓度为___________  。
。

④下列不当操作会使测得的硬水样品 的浓度偏高的是
的浓度偏高的是___________ (填字母)
A.滴定管未用标准溶液润洗 B.草酸钙 沉淀洗涤不充分
沉淀洗涤不充分
C.滴定前仰视读数并记录数据 D.盛放草酸溶液的锥形瓶没有干燥
 是一种易溶于水的二元有机弱酸,常用作还原剂、沉淀剂等,可与酸性
是一种易溶于水的二元有机弱酸,常用作还原剂、沉淀剂等,可与酸性 溶液发生反应:
溶液发生反应: 。
。(1)探究外界条件对反应速率的影响。
| 实验编号 | 所加试剂及用量/mL | 条件 | 溶液颜色褪至 无色所需时间/min | |||
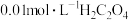 溶液 溶液 | 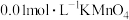 溶液 溶液 |  稀 稀 | 水 | 温度℃ | ||
| 1 | 12.0 | 2.0 | 3.0 | 3.0 | 20 |  |
| 2 | 6.0 | 2.0 | 3.0 |  | 20 |  |
| 3 |  | 2.0 | 3.0 | 9.0 | 30 |  |


②对比实验1、2可探究
(2)某兴趣小组用草酸及草酸盐的性质测定硬水中钙离子的浓度。

根据消耗酸性
 标准溶液的体积即可测定硬水样品中
标准溶液的体积即可测定硬水样品中 的浓度。
的浓度。①实验过程提及的下列仪器,在使用之前一定要润洗的是
A.容量瓶 B.烧杯 C.锥形瓶 D.滴定管
②滴定过程中
③本实验滴定管起点和终点的液面位置如图所示,则滴定过程中消耗的
 标准溶液为
标准溶液为 。该硬水样品中
。该硬水样品中 的浓度为
的浓度为 。
。
④下列不当操作会使测得的硬水样品
 的浓度偏高的是
的浓度偏高的是A.滴定管未用标准溶液润洗 B.草酸钙
 沉淀洗涤不充分
沉淀洗涤不充分C.滴定前仰视读数并记录数据 D.盛放草酸溶液的锥形瓶没有干燥
您最近一年使用:0次
2023-12-17更新
|
124次组卷
|
2卷引用:广东省深圳市富源学校2023-2024学年高二上学期模拟预测化学试题
名校
解题方法
10 . 羰基硫广泛应用在农药制备工业,是一种重要的有机合成中间体。利用 和
和 反应可以合成COS,回答下列问题:
反应可以合成COS,回答下列问题:
(1)由 和
和 合成
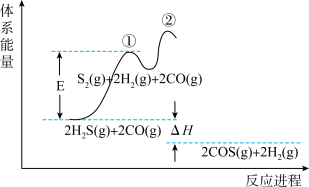
合成 的反应分两步进行,其能量变化如图所示。
的反应分两步进行,其能量变化如图所示。
①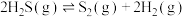
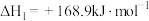
②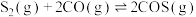
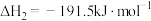
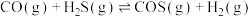 的
的
___________ 。决定COS生成速率的步骤是___________ (填“①”或“②”)。
(2)在恒压、CO和 的起始浓度一定的条件下,催化反应相同时间,测得各容器中CO的转化率与温度的关系如图所示:
的起始浓度一定的条件下,催化反应相同时间,测得各容器中CO的转化率与温度的关系如图所示: 段曲线变化的原因是
段曲线变化的原因是_______ ;能提高 平衡转化率的措施有
平衡转化率的措施有_______ (填序号)。
A.适当升温 B.及时分离COS C.降低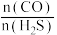 投料比 D.选择高效催化剂
投料比 D.选择高效催化剂
(3)在某温度下,向 的密闭容器中通入
的密闭容器中通入 和
和 各
各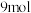 ,发生反应
,发生反应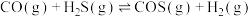 ,
, ,平衡时
,平衡时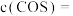
___________ 。若保持温度不变,再向容器中加入 和
和 ,平衡移动的方向为
,平衡移动的方向为_______ (填“正反应方向”“逆反应方向”或“不移动”)。
(4)实验测得该反应的速率方程为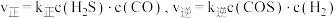 ,k为速率常数(受温度影响),则化学平衡常数
,k为速率常数(受温度影响),则化学平衡常数
___________ (用 、
、 表达),平衡后升高温度,
表达),平衡后升高温度, 增大的倍数
增大的倍数___________ (填“>”“<”或“=”) 增大的倍数。
增大的倍数。
 和
和 反应可以合成COS,回答下列问题:
反应可以合成COS,回答下列问题:(1)由
 和
和 合成
合成 的反应分两步进行,其能量变化如图所示。
的反应分两步进行,其能量变化如图所示。①
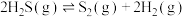
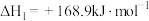
②
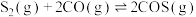
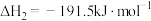
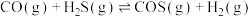 的
的
(2)在恒压、CO和
 的起始浓度一定的条件下,催化反应相同时间,测得各容器中CO的转化率与温度的关系如图所示:
的起始浓度一定的条件下,催化反应相同时间,测得各容器中CO的转化率与温度的关系如图所示: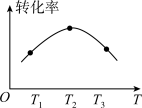
 段曲线变化的原因是
段曲线变化的原因是 平衡转化率的措施有
平衡转化率的措施有A.适当升温 B.及时分离COS C.降低
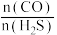 投料比 D.选择高效催化剂
投料比 D.选择高效催化剂(3)在某温度下,向
 的密闭容器中通入
的密闭容器中通入 和
和 各
各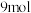 ,发生反应
,发生反应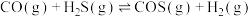 ,
, ,平衡时
,平衡时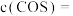
 和
和 ,平衡移动的方向为
,平衡移动的方向为(4)实验测得该反应的速率方程为
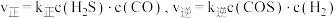 ,k为速率常数(受温度影响),则化学平衡常数
,k为速率常数(受温度影响),则化学平衡常数
 、
、 表达),平衡后升高温度,
表达),平衡后升高温度, 增大的倍数
增大的倍数 增大的倍数。
增大的倍数。
您最近一年使用:0次
2023-12-13更新
|
194次组卷
|
4卷引用:广东省深圳市富源学校2023-2024学年高二上学期模拟预测化学试题



