名校
1 . 几种氧化物的化学键中离子键成分的百分数如下表所示:
根据表格信息,可推知:前四周期元素组成的离子晶体中,离子键成分的百分数最高的是
氧化物 |
|
|
|
|
离子键成分的百分数/ | 62 | 50 | 41 | 33 |
A.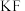 | B. | C. | D. |
您最近一年使用:0次
2024-04-21更新
|
273次组卷
|
3卷引用:第三章晶体结构与性质(B卷)
2 . 现有一种由正离子An+、Bm+和负离子X—组成的无机固体电解质,该物质在高温相为无序结构,低温相为有序结构,两者的结构如图,下列说法错误的是
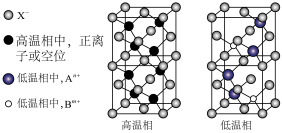
| A.n=2,m=1 | B.高温相中X—的堆积方式和氯化钠中Cl—的堆积方式相同 |
| C.低温相中An+的配位数为4 | D.高温相的良好导电性与其结构中存在大量的空位有关 |
您最近一年使用:0次
2024-04-13更新
|
753次组卷
|
4卷引用:第三章晶体结构与性质(B卷)
名校
3 . 前四周期元素W、X、Y、Z的原子序数依次增大,且互相不同周期不同族。其中W是宇宙中含量最多的元素;X元素基态原子最高能级的不同轨道都有电子,并且自旋方向相同:Y元素基态原子最外层电子数等于其能层数:Z元素基态原子核外未成对电子数同周期最多。下列说法正确的是
| A.Y元素最高价氧化物对应的水化物为强碱 | B.基态X原子核外电子有7种空间运动状态 |
C.基态原子中未成对电子数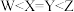 | D.Z形成的两种含氧酸根在溶液中存在着化学平衡 |
您最近一年使用:0次
23-24高二下·全国·单元测试
解题方法
4 . 如图,石墨晶体结构的每一层里平均每个最小的正六边形占有碳原子数目为
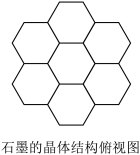

| A.2 | B.3 | C.4 | D.6 |
您最近一年使用:0次
23-24高二下·全国·单元测试
5 . 早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过_______ 方法区分晶体、准晶体和非晶体。
(2)Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有_______ 个铜原子。
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有
您最近一年使用:0次
23-24高二下·全国·单元测试
6 . 你认为下列说法中正确的是
| A.氢键存在于分子之间,不存在于分子之内 |
| B.对于组成和结构相似的分子,其范德华力随着相对分子质量的增大而增大 |
| C.NH3极易溶于水而CH4难溶于水的原因只是因为NH3是极性分子,CH4是非极性分子 |
| D.冰熔化时只破坏范德华力 |
您最近一年使用:0次
23-24高二下·全国·单元测试
解题方法
7 . 下列说法中,正确的是
| A.由分子构成的物质中一定含有共价键 |
| B.离子化合物中一定含有金属元素 |
| C.正四面体结构的分子中的键角一定是109°28′ |
| D.不同的原子的化学性质可能相同 |
您最近一年使用:0次
23-24高二下·全国·单元测试
8 . 有机物K在工业生产中有着重要的应用,其合成路线如下:
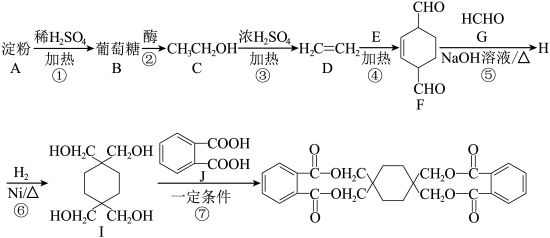
已知:i.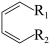 +||
+||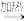
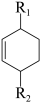
ii.H3CCHO+3HCHO
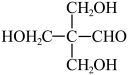
回答下列问题:
(1)葡萄糖的分子式为_____ ,有机物E的结构简式为_____ 。
(2)③的反应类型_____ ,有机物H中的含氧官能团名称为_____ 。
(3)反应⑦的条件为_____ 。
(4)有机物F与足量H2催化加氢后的产物与有机物J形成聚酯的化学方程式_____ 。
(5)有机物F满足下列条件的同分异构体有_____ 种。
①含有苯环,且苯环上有2个取代基
②可以和FeCl3溶液发生显色反应
③1mol的有机物和足量Na反应可产生1molH2
(6)根据上述流程,请设计由乙醇合成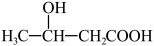 的流程:
的流程:_____ 。
(7)有机物E与M互为同分异构体,则M中含有两个甲基、碳碳双键和羧基的结构有_____ 种。

已知:i.
 +||
+||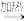

ii.H3CCHO+3HCHO


回答下列问题:
(1)葡萄糖的分子式为
(2)③的反应类型
(3)反应⑦的条件为
(4)有机物F与足量H2催化加氢后的产物与有机物J形成聚酯的化学方程式
(5)有机物F满足下列条件的同分异构体有
①含有苯环,且苯环上有2个取代基
②可以和FeCl3溶液发生显色反应
③1mol的有机物和足量Na反应可产生1molH2
(6)根据上述流程,请设计由乙醇合成
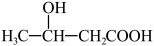 的流程:
的流程:(7)有机物E与M互为同分异构体,则M中含有两个甲基、碳碳双键和羧基的结构有
您最近一年使用:0次
名校
解题方法
9 . 新冠肺炎疫情防控,消毒用品必不可少。试回答下列问题:
(1)过氧乙酸(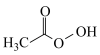 )也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有
)也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有___________ ,分子中 键和
键和 键的个数比为
键的个数比为___________ 。
(2)生活中常用的手消毒凝胶,其主要有效成分是三氮羟基二苯醚和乙醇,其中三氯羟基二苯醚是一种广谱抗菌剂,高效、安全。三氯羟基二苯醚的结构简式如图所示。

①组成三氯羟基二苯醚的四种元素H、C、O、Cl的电负性从大到小的顺序为___________ ;基态氯原子的价电子排布图为___________ ,最高能级的原子轨道电子云轮廓图形状为___________ 。
②三氯羟基二苯醚的熔点:55~57℃,沸点:120℃,常态为白色或灰白色晶状粉末,稍有酚臭味,不溶于水,易溶于碱液和有机溶剂,三氯羟基二苯醚属于___________ 晶体。
③乙醇与甲醚 的分子式相同,但二者的沸点分别为78.4℃、-24.8℃,乙醇沸点高于甲醚的原因是
的分子式相同,但二者的沸点分别为78.4℃、-24.8℃,乙醇沸点高于甲醚的原因是___________ 。
(3)Na、K等活泼金属在 中燃烧得到的
中燃烧得到的 、
、 具有强氧化性,也常做消毒剂。已知
具有强氧化性,也常做消毒剂。已知 的晶胞如图所示:
的晶胞如图所示:
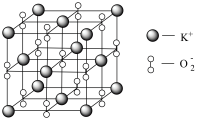
设阿伏加德罗常数的值为 ,晶胞的参数为a nm。晶胞的密度为
,晶胞的参数为a nm。晶胞的密度为___________  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
(1)过氧乙酸(
 )也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有
)也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有 键和
键和 键的个数比为
键的个数比为(2)生活中常用的手消毒凝胶,其主要有效成分是三氮羟基二苯醚和乙醇,其中三氯羟基二苯醚是一种广谱抗菌剂,高效、安全。三氯羟基二苯醚的结构简式如图所示。

①组成三氯羟基二苯醚的四种元素H、C、O、Cl的电负性从大到小的顺序为
②三氯羟基二苯醚的熔点:55~57℃,沸点:120℃,常态为白色或灰白色晶状粉末,稍有酚臭味,不溶于水,易溶于碱液和有机溶剂,三氯羟基二苯醚属于
③乙醇与甲醚
 的分子式相同,但二者的沸点分别为78.4℃、-24.8℃,乙醇沸点高于甲醚的原因是
的分子式相同,但二者的沸点分别为78.4℃、-24.8℃,乙醇沸点高于甲醚的原因是(3)Na、K等活泼金属在
 中燃烧得到的
中燃烧得到的 、
、 具有强氧化性,也常做消毒剂。已知
具有强氧化性,也常做消毒剂。已知 的晶胞如图所示:
的晶胞如图所示:
设阿伏加德罗常数的值为
 ,晶胞的参数为a nm。晶胞的密度为
,晶胞的参数为a nm。晶胞的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
10 . 湿法冶炼是以赤铜矿(Cu2O)精矿为主要原料,通过浸出、置换、电解等流程制备高纯度铜的工艺。
已知:Cu2O晶胞为立方体形,边长为4.26×10−8 cm。
(1)根据图示,每个Cu2O晶胞中含O原子的数目为_______ 个。

(2)计算Cu2O晶体的密度ρ=_______ g/cm3.(结果保留两位小数)
(3)测定晶体结构最常用的仪器为
(4)赤铜矿在稀硫酸中浸出,得到硫酸铜溶液,该反应的离子方程式为_______ 。
已知:Cu2O晶胞为立方体形,边长为4.26×10−8 cm。
(1)根据图示,每个Cu2O晶胞中含O原子的数目为

(2)计算Cu2O晶体的密度ρ=
(3)测定晶体结构最常用的仪器为
| A.质谱仪 | B.核磁共振仪 | C.红外光谱仪 | D.X射线衍射仪 |
您最近一年使用:0次








