名校
解题方法
1 . 化学反应在发生物质变化的同时伴随有能量的变化,是人类获取能量的重要途径,请回答下列问题。
(1)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:___________ (选填“吸热”或“放热)反应。
(2)在容积为 的恒容密闭容器中投入等物质的量的
的恒容密闭容器中投入等物质的量的 和
和 ,进行反应:
,进行反应: 。
。 、
、 的物质的量随时间变化关系如下图所示。
的物质的量随时间变化关系如下图所示。___________ (填“a”、“b”、“c”或“d”);用同一物质表示反应速率时,a、c两点的正反应速率: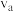
___________ 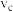 。(填“大于”、“小于”或“等于”,下同),该反应达到平衡时,
。(填“大于”、“小于”或“等于”,下同),该反应达到平衡时, 的转化率
的转化率___________ 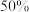 。
。
(3)甲烷燃料电池装置如图所示,通入 的电极为电池的
的电极为电池的___________ (填“正极”或“负极”),通入氧气一端电极反应方程式为___________ ,当有 电子转移时,消耗
电子转移时,消耗 的物质的量是
的物质的量是___________ 。
(1)硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:

(2)在容积为
 的恒容密闭容器中投入等物质的量的
的恒容密闭容器中投入等物质的量的 和
和 ,进行反应:
,进行反应: 。
。 、
、 的物质的量随时间变化关系如下图所示。
的物质的量随时间变化关系如下图所示。
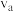
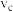 。(填“大于”、“小于”或“等于”,下同),该反应达到平衡时,
。(填“大于”、“小于”或“等于”,下同),该反应达到平衡时, 的转化率
的转化率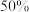 。
。(3)甲烷燃料电池装置如图所示,通入
 的电极为电池的
的电极为电池的 电子转移时,消耗
电子转移时,消耗 的物质的量是
的物质的量是
您最近一年使用:0次
名校
解题方法
2 . 化学与生活、生产、科技、环境等密切相关。下列说法正确的是
A.常温下 的雨水称为酸雨 的雨水称为酸雨 | B. 是应用最为广泛的半导体材料 是应用最为广泛的半导体材料 |
C.玻璃的主要成分是 和 和 | D.豆科植物的根瘤菌将氮气转化为氨属于氮的固定 |
您最近一年使用:0次
名校
解题方法
3 . 硫元素的单质及其化合物在人类生产和生活中发挥着重要的作用。下列说法正确的是
A.硫在加热的条件下与 反应生成Fe2S3 反应生成Fe2S3 |
| B.SO2能使酸性KMnO4溶液褪色,证明了SO2具有漂白性 |
| C.常温下,硫化氢是一种有毒、有害的气体,吸入硫化氢可能对呼吸系统产生严重危害 |
| D.硫酸型酸雨在空气中放置一段时间pH变大 |
您最近一年使用:0次
4 . 化学与生活密切相关。下列说法正确的是
| A.太阳能电池的主要材料是高纯度的二氧化硅 |
| B.二氧化硫是一种有毒气体,不能用作食品添加剂 |
| C.液氨汽化时放出大量热,故液氨可用作制冷剂 |
| D.次氯酸钠具有强氧化性,能够起到消毒、杀菌的作用 |
您最近一年使用:0次
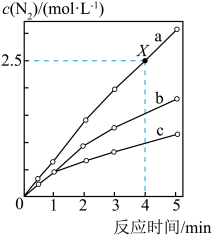
5 . 相同条件下,在固定容积的密闭容器中选用不同的催化剂(a、b、c)发生反应:4NH3(g)+6NO(g) 5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
 5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
5N2(g)+6H2O(g),反应产生N2的物质的量浓度随时间变化如图所示。下列说法错误的是
| A.催化剂的催化效率:a>b>c |
| B.X点时,NH3的化学反应速率为0.5 mol·L-1·min-1 |
| C.使用催化剂a、b、c达到平衡时NO的转化率相等 |
| D.若在恒容绝热的密闭容器中发生该反应,当K值不变时,说明反应已经达到平衡 |
您最近一年使用:0次
6 . 下列有关离子键和金属键的叙述错误的是
| A.离子键和金属键都没有饱和性和方向性 |
| B.金属导电是因为在外加电场作用下产生自由电子 |
| C.物质中可能只存在阳离子,而不存在阴离子 |
| D.在以离子键为主的化学键中常含有共价键成分,例如Mg与O形成的离子键中共价键的成分大于Na与F形成的离子键 |
您最近一年使用:0次
2024-03-28更新
|
117次组卷
|
3卷引用:甘肃省兰州第一中学2023-2024学年高二下学期4月期中考试化学试题
名校
7 . 实验室存放的浓硫酸的标签如图所示,回答下列问题:
(1)该浓硫酸的物质的量浓度为___________  。
。
(2)某实验需用 的稀硫酸。实验室配制该浓度的稀硫酸时,下列仪器不需要的是
的稀硫酸。实验室配制该浓度的稀硫酸时,下列仪器不需要的是___________ (填标号)。
A. 容量瓶 B.胶头滴管 C.托盘天平 D.量筒 E.玻璃棒 F.漏斗
容量瓶 B.胶头滴管 C.托盘天平 D.量筒 E.玻璃棒 F.漏斗
(3)利用上述玻璃仪器配制需要的 稀硫酸时,需要量取的浓硫酸的体积为
稀硫酸时,需要量取的浓硫酸的体积为___________ mL(保留三位有效数字)。
(4)当配制过程中出现以下情况时,请判断对所配溶液浓度的影响,用“偏高”、“偏低”或“无影响”回答。
①容量瓶用蒸馏水洗净后,没烘干就直接使用___________
②定容时仰视读数___________
③溶解后未经冷却就移液___________
(5)从配制好的稀硫酸中取出 ,则取出的
,则取出的 溶液中硫酸的浓度为
溶液中硫酸的浓度为___________  ,若将此
,若将此 溶液加水稀释至
溶液加水稀释至 ,则稀释后硫酸的浓度为
,则稀释后硫酸的浓度为___________  。
。
净含量: 密度:  质量分数:98% 注意事项:密封保存 |
 。
。(2)某实验需用
 的稀硫酸。实验室配制该浓度的稀硫酸时,下列仪器不需要的是
的稀硫酸。实验室配制该浓度的稀硫酸时,下列仪器不需要的是A.
 容量瓶 B.胶头滴管 C.托盘天平 D.量筒 E.玻璃棒 F.漏斗
容量瓶 B.胶头滴管 C.托盘天平 D.量筒 E.玻璃棒 F.漏斗(3)利用上述玻璃仪器配制需要的
 稀硫酸时,需要量取的浓硫酸的体积为
稀硫酸时,需要量取的浓硫酸的体积为(4)当配制过程中出现以下情况时,请判断对所配溶液浓度的影响,用“偏高”、“偏低”或“无影响”回答。
①容量瓶用蒸馏水洗净后,没烘干就直接使用
②定容时仰视读数
③溶解后未经冷却就移液
(5)从配制好的稀硫酸中取出
 ,则取出的
,则取出的 溶液中硫酸的浓度为
溶液中硫酸的浓度为 ,若将此
,若将此 溶液加水稀释至
溶液加水稀释至 ,则稀释后硫酸的浓度为
,则稀释后硫酸的浓度为 。
。
您最近一年使用:0次
名校
8 . 某研究性学习小组探究了铜参与的某些氧化还原反应。回答下列问题:
(1)铜与浓硝酸反应的装置如图( 在碱性溶液中发生歧化反应):
在碱性溶液中发生歧化反应):
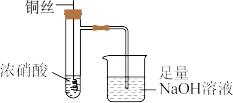
①此装置的优点有___________ 。
②用离子方程式解释NaOH溶液的作用:___________ 。
(2)探究铜与 的反应:
的反应:
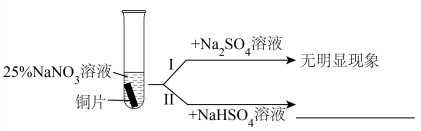
①实验Ⅱ中的现象为___________ 。
②实验Ⅰ、Ⅱ中现象不同的原因是___________ 。
(3)探究铜片与足量浓硫酸的反应(经检测所得“固体”中含有 和遇水变蓝色的物质X):
和遇水变蓝色的物质X):
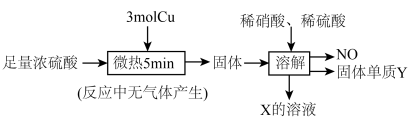
①生成NO的反应的离子方程式为___________ 。
②物质X在生产生活中的用途为___________ 。
③“固体”中 和物质X的物质的量之比为
和物质X的物质的量之比为___________ 。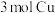 完全反应时消耗
完全反应时消耗 的物质的量为
的物质的量为___________ mol。
(1)铜与浓硝酸反应的装置如图(
 在碱性溶液中发生歧化反应):
在碱性溶液中发生歧化反应):
①此装置的优点有
②用离子方程式解释NaOH溶液的作用:
(2)探究铜与
 的反应:
的反应:
①实验Ⅱ中的现象为
②实验Ⅰ、Ⅱ中现象不同的原因是
(3)探究铜片与足量浓硫酸的反应(经检测所得“固体”中含有
 和遇水变蓝色的物质X):
和遇水变蓝色的物质X):
①生成NO的反应的离子方程式为
②物质X在生产生活中的用途为
③“固体”中
 和物质X的物质的量之比为
和物质X的物质的量之比为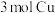 完全反应时消耗
完全反应时消耗 的物质的量为
的物质的量为
您最近一年使用:0次
名校
9 . 二甲醚( )是一种重要的清洁燃料,可代替氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚,发生的反应为
)是一种重要的清洁燃料,可代替氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚,发生的反应为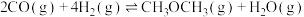 。下列说法正确的是
。下列说法正确的是
 )是一种重要的清洁燃料,可代替氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚,发生的反应为
)是一种重要的清洁燃料,可代替氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚,发生的反应为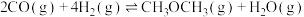 。下列说法正确的是
。下列说法正确的是
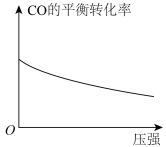
| A.CO的平衡转化率随压强的变化如图所示 |
B.该反应中,每消耗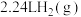 ,同时生成 ,同时生成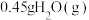 |
C.加入合适的催化剂,有利于提高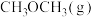 的平衡产率 的平衡产率 |
| D.保持其他条件不变,仅适当升高温度,该反应的活化分子百分数一定增大 |
您最近一年使用:0次
2023-11-30更新
|
64次组卷
|
2卷引用:甘肃省白银市靖远县2023-2024学年高二上学期11月期中联考化学试题
名校
解题方法
10 . 钠是一种非常活泼、具有广泛应用的金属。回答下列问题:
(1)钠原子的结构示意图为___________ ,在化学反应中容易___________ (填“得到”或“失去”)电子。
(2)钠的一种常见淡黄色氧化物,常用作呼吸面具的供氧剂。该物质与 反应的化学反应方程式为
反应的化学反应方程式为___________ 。
(3)观察法也是学习化学的重要方法,金属钠放置在空气中观察到下列现象。
银白色固体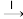 变灰暗
变灰暗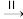 变白色
变白色 出现液滴
出现液滴 白色晶体
白色晶体
①反应Ⅰ后固体变灰暗,该固体的化学式为___________ ,将少量灰暗色固体投入 溶液中,观察到的实验现象为
溶液中,观察到的实验现象为___________ 。
②反应Ⅱ后得到的固体为NaOH,NaOH在水中的电离方程式为___________ 。
③反应Ⅳ,主要是液滴与空气中的___________ (填名称)发生反应,下列属于白色晶体用途的是___________ (填字母)。
A.制肥皂 B.造纸 C.烘焙蛋糕 D.用于治疗胃酸过多症
(1)钠原子的结构示意图为
(2)钠的一种常见淡黄色氧化物,常用作呼吸面具的供氧剂。该物质与
 反应的化学反应方程式为
反应的化学反应方程式为(3)观察法也是学习化学的重要方法,金属钠放置在空气中观察到下列现象。
银白色固体
 变灰暗
变灰暗 变白色
变白色 出现液滴
出现液滴 白色晶体
白色晶体①反应Ⅰ后固体变灰暗,该固体的化学式为
 溶液中,观察到的实验现象为
溶液中,观察到的实验现象为②反应Ⅱ后得到的固体为NaOH,NaOH在水中的电离方程式为
③反应Ⅳ,主要是液滴与空气中的
A.制肥皂 B.造纸 C.烘焙蛋糕 D.用于治疗胃酸过多症
您最近一年使用:0次
2023-11-16更新
|
103次组卷
|
5卷引用:甘肃省永昌县第一高级中学2023-2024学年高一上学期期中考试化学试题



