解题方法
1 . 写出钠与水反应的现象以及对现象的解释:
(1)现象:_______ ;对现象的解释:_______ ;
(2)现象:_______ ;对现象的解释:_______ ;
(3)现象:_______ ;对现象的解释:_______ ;
(4)现象:_______ ;对现象的解释:_______ ;
(1)现象:
(2)现象:
(3)现象:
(4)现象:
您最近一年使用:0次
2 . 回答下列问题
(1)能够使化学平衡移动的因素有________ 、________ 、________ 。
(2)可逆反应A(g)+2B(g) 2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡
2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡______ 移动(填正向、逆向、不),B的转化率_______ , v(正) ________ 。(填增大、减小、不变)。
(1)能够使化学平衡移动的因素有
(2)可逆反应A(g)+2B(g)
 2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡
2C(g)(正反应为放热反应),在一定条件下达到平衡,若升高温度,化学平衡
您最近一年使用:0次
3 . 回答下列问题:
(1)现有可逆反应A(气)+B(气) 3C(气),图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:
3C(气),图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:
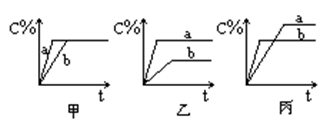
①若乙图中的a曲线表示200℃时的情况,b曲线表示100℃时的情况,则此可逆反应的正反应是____ 热反应。
②若丙图中两条曲线分别表示不同压强下的情况,则____ 曲线是表示压强较大的情况。
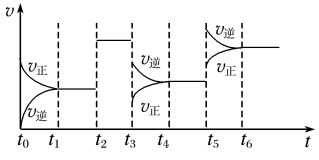
(2)图中Z表示在密闭容器中反应:2SO2+O2 2SO3 ΔH<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,t3至t4过程中改变的条件可能是
2SO3 ΔH<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,t3至t4过程中改变的条件可能是____ ;t5至t6过程中改变的条件可能是____ ;写出t1至t2阶段平衡体系中反应平衡常数的表达式K=____ 。
(3)如图表示平衡时SO2的体积分数随压强和温度变化的曲线,则:
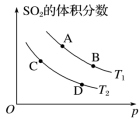
①温度关系:T1____ T2(填“>”“<”或“=”,下同)。
②平衡常数关系:K(A)____ K(D)。
(1)现有可逆反应A(气)+B(气)
 3C(气),图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:
3C(气),图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:
①若乙图中的a曲线表示200℃时的情况,b曲线表示100℃时的情况,则此可逆反应的正反应是
②若丙图中两条曲线分别表示不同压强下的情况,则
(2)图中Z表示在密闭容器中反应:2SO2+O2
 2SO3 ΔH<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,t3至t4过程中改变的条件可能是
2SO3 ΔH<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,t3至t4过程中改变的条件可能是
(3)如图表示平衡时SO2的体积分数随压强和温度变化的曲线,则:

①温度关系:T1
②平衡常数关系:K(A)
您最近一年使用:0次
4 . 根据下列四种电化学装置图,回答下列问题:
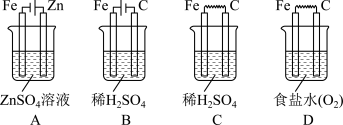
(1)装置名称:A____ 。
(2)装置A中Fe是____ 极;装置B中Fe是____ 极;装置D中Fe是____ 极。
(3)装置B、C相比较,其反应速率的大小关系是___ 。

(1)装置名称:A
(2)装置A中Fe是
(3)装置B、C相比较,其反应速率的大小关系是
您最近一年使用:0次
5 . 填空
(1)用双线桥法表示氧化还原反应2KMnO4 K2MnO4+MnO2+O2↑电子转移的方向和数目
K2MnO4+MnO2+O2↑电子转移的方向和数目_____ 。
(2)在这个反应6Fe2++ +14H+=6Fe3++2Cr3++7H2O中氧化剂为
+14H+=6Fe3++2Cr3++7H2O中氧化剂为_______ ,还原剂为_______ ,_______ 元素被还原,氧化产物是_______ ;氧化性强弱为:_______ >_______ 。
(3)写出下列反应的离子方程式。
①铜与硝酸银溶液的反应:_______ 。
②Na和H2O的反应:_______ 。
(1)用双线桥法表示氧化还原反应2KMnO4
 K2MnO4+MnO2+O2↑电子转移的方向和数目
K2MnO4+MnO2+O2↑电子转移的方向和数目(2)在这个反应6Fe2++
 +14H+=6Fe3++2Cr3++7H2O中氧化剂为
+14H+=6Fe3++2Cr3++7H2O中氧化剂为(3)写出下列反应的离子方程式。
①铜与硝酸银溶液的反应:
②Na和H2O的反应:
您最近一年使用:0次
名校
6 .  代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
①等质量的 和
和 两种气体,其体积之比为1∶1
两种气体,其体积之比为1∶1
②与 所含H原子数目相同的
所含H原子数目相同的 的质量为
的质量为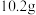
③在标准状况时,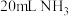 与
与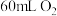 所含的原子个数之比为1∶3
所含的原子个数之比为1∶3
④常温常压下,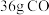 与
与 的混合气体占体积为
的混合气体占体积为 ,该混合气体的密度是
,该混合气体的密度是 密度的18倍
密度的18倍
⑤若用 石墨能写a个字,则平均每个字约含有
石墨能写a个字,则平均每个字约含有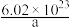 个碳原子
个碳原子
⑥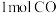 和
和 的混合气体中含有的质子数为
的混合气体中含有的质子数为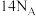
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是①等质量的
 和
和 两种气体,其体积之比为1∶1
两种气体,其体积之比为1∶1②与
 所含H原子数目相同的
所含H原子数目相同的 的质量为
的质量为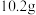
③在标准状况时,
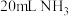 与
与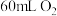 所含的原子个数之比为1∶3
所含的原子个数之比为1∶3④常温常压下,
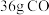 与
与 的混合气体占体积为
的混合气体占体积为 ,该混合气体的密度是
,该混合气体的密度是 密度的18倍
密度的18倍⑤若用
 石墨能写a个字,则平均每个字约含有
石墨能写a个字,则平均每个字约含有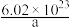 个碳原子
个碳原子⑥
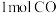 和
和 的混合气体中含有的质子数为
的混合气体中含有的质子数为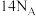
| A.①②⑥ | B.②③⑤ | C.①③④ | D.②⑤⑥ |
您最近一年使用:0次
2022-10-14更新
|
355次组卷
|
2卷引用:甘肃省张掖市高台县第一中学2021-2022学年高一上学期期中考试化学试题
7 . 下列叙述正确的是
①氯元素在自然界中既以化合态存在,也以游离态(单质)存在
②为了防止贮存液氯的钢瓶被腐蚀,钢瓶在装氯之前必须彻底干燥
③将有色鲜花放入盛有干燥氯气的集气瓶中,盖上玻璃片鲜花褪色,证明氯气具有漂白性
④常温下,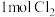 与足量
与足量 溶液反应,转移电子的物质的量为
溶液反应,转移电子的物质的量为
⑤向次氯酸钙溶液中通入适量 可增强漂白效果
可增强漂白效果
⑥向某溶液中加入稀硝酸酸化的硝酸银溶液,若产生白色沉淀,则说明原溶液中含有
①氯元素在自然界中既以化合态存在,也以游离态(单质)存在
②为了防止贮存液氯的钢瓶被腐蚀,钢瓶在装氯之前必须彻底干燥
③将有色鲜花放入盛有干燥氯气的集气瓶中,盖上玻璃片鲜花褪色,证明氯气具有漂白性
④常温下,
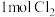 与足量
与足量 溶液反应,转移电子的物质的量为
溶液反应,转移电子的物质的量为
⑤向次氯酸钙溶液中通入适量
 可增强漂白效果
可增强漂白效果⑥向某溶液中加入稀硝酸酸化的硝酸银溶液,若产生白色沉淀,则说明原溶液中含有

| A.①②③ | B.②③④ | C.②⑤⑥ | D.④⑤⑥ |
您最近一年使用:0次
2022-10-14更新
|
560次组卷
|
3卷引用:甘肃省张掖市高台县第一中学2021-2022学年高一上学期期中考试化学试题
8 . 碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。请回答下列问题:
已知:①CO(g)+2H2(g)=CH3OH(g) ΔH1=-99.0kJ•mol-1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g)=CO(g)+H2O(g) ΔH3=+41.0kJ•mol-1
(1)反应①熵变ΔS____ 0,该反应自发进行的条件是____ (填“低温”“高温”或“任意温度”)。
(2)CH3OH的燃烧热为726kJ•mol-1,计算16g甲醇燃烧放出的热量为____ kJ。
(3)反应CO2(g)+H2(g)=CO(g)+H2O(l)的ΔH____ ΔH3(填“>”“<”“=”)。
(4)根据盖斯定律计算反应②的ΔH2=____ kJ•mol-1,上述①②③反应中符合如图能量变化的是____ (填序号)。
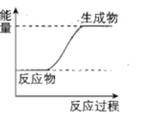
已知:①CO(g)+2H2(g)=CH3OH(g) ΔH1=-99.0kJ•mol-1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g)=CO(g)+H2O(g) ΔH3=+41.0kJ•mol-1
(1)反应①熵变ΔS
(2)CH3OH的燃烧热为726kJ•mol-1,计算16g甲醇燃烧放出的热量为
(3)反应CO2(g)+H2(g)=CO(g)+H2O(l)的ΔH
(4)根据盖斯定律计算反应②的ΔH2=

您最近一年使用:0次
9 . 氯水的成分中含有H2O,Cl2,HClO,H+,Cl-,ClO-等,这些微粒中,溶液呈淡黄绿色是含有_____ (填微粒符号,下同),能与硝酸银溶液产生白色沉淀的是____ ,具有漂白性的是____ ,能与碳酸钠溶液反应的是____ 。
您最近一年使用:0次
2022-09-21更新
|
115次组卷
|
2卷引用:甘肃省兰州市教育局第四片区2021-2022学年高一上学期期中考试化学试题
解题方法
10 . 氮及其化合物在生产生活中有广泛应用。
(1)已知:CO可将部分氮的氧化物还原为N2。
反应Ⅰ:2CO(g)+2NO(g) N2(g)+2CO2(g) ΔH1=-746 kJ·mol-1
N2(g)+2CO2(g) ΔH1=-746 kJ·mol-1
反应Ⅱ:4CO(g)+2NO2(g) N2(g)+4CO2(g) ΔH2=-1200 kJ·mol-1
N2(g)+4CO2(g) ΔH2=-1200 kJ·mol-1
写出CO将NO2还原为NO的热化学方程式:_______ 。
(2)利用微生物燃料电池进行废水处理,实现碳氮联合转化。其工作原理如图所示,其中M、N为厌氧微生物电极。
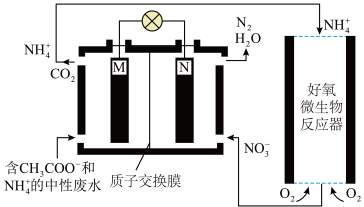
①M极是_______ 极,电极反应方程式:_______ ;
②电池工作时,H+移动方向_______ ;
③相同条件下,N、M两极生成的气体体积之比为_______ ;
④好氧微生物反应器中发生的反应为:_______ 。
(1)已知:CO可将部分氮的氧化物还原为N2。
反应Ⅰ:2CO(g)+2NO(g)
 N2(g)+2CO2(g) ΔH1=-746 kJ·mol-1
N2(g)+2CO2(g) ΔH1=-746 kJ·mol-1反应Ⅱ:4CO(g)+2NO2(g)
 N2(g)+4CO2(g) ΔH2=-1200 kJ·mol-1
N2(g)+4CO2(g) ΔH2=-1200 kJ·mol-1写出CO将NO2还原为NO的热化学方程式:
(2)利用微生物燃料电池进行废水处理,实现碳氮联合转化。其工作原理如图所示,其中M、N为厌氧微生物电极。

①M极是
②电池工作时,H+移动方向
③相同条件下,N、M两极生成的气体体积之比为
④好氧微生物反应器中发生的反应为:
您最近一年使用:0次



